Das Immunsystem gegen den Tumor mobil machen
Seit Jahren steigt die Krebsneuerkrankungsrate kontinuierlich an. Parallel dazu ist ein Rückgang der Krebssterblichkeit zu verzeichnen – eine Entwicklung, die eindrucksvoll die Fortschritte der Krebsmedizin demonstriert. So sind bei verschiedenen Tumoren die Heilungsraten deutlich gestiegen, bei anderen Krebsformen hat sich die Überlebenszeit erheblich verlängert und die Zahl der sogenannten Langzeitüberlebenden nimmt stetig zu. Ist eine Heilung nicht möglich, kann zumindest bei einigen Tumoren ein Übergang in eine chronische Erkrankung realisiert werden.
Diese Entwicklung dürfte sich durch die Krebsimmuntherapie weiter fortsetzen. Ziel dieser neuen Strategie in der Onkologie ist es, das körpereigene Abwehrsystem wieder in die Lage zu versetzen, entartete Zellen als solche zu erkennen, zu bekämpfen und so den Körper im Kampf gegen den Tumor zu unterstützen.
Die Tricks der Tumorzellen
Denn Tumorzellen bilden sich Tag für Tag in großer Zahl in unserem Körper. Sie werden normalerweise durch das Immunsystem erkannt und eliminiert, so dass sich keine Krebsgeschwulst bilden kann. Allerdings gibt es Tumorzellen, die sich dem Immunsystem entziehen können. Dies ist nach Angaben der Deutschen Krebsgesellschaft über verschiedene Mechanismen möglich:
Tumorzellen können sich tarnen, indem sie keine tumortypischen Erkennungsmerkmale mehr auf ihrer Oberfläche zeigen. Sie können außerdem sogar Merkmale exprimieren, die eigentlich für gesunde Gewebe charakteristisch sind.
Bösartig veränderte Zellen können das Immunsystem direkt manipulieren oder schwächen. Das Immunsystem kann die Tumorzellen noch als schädigend erkennen, aber nicht mehr angreifen. Über diesen Mechanismus können Tumorzellen die Aktivität von T-Lymphozyten mindern.
Die Zellen können außerdem Botenstoffe bilden, die die Reifung oder die Aktivität von Immunzellen hemmen. Eine andere Möglichkeit ist die Mobilisierung regulatorischer T-Zellen, die unerwünschte Immunreaktionen unterdrücken.
Krebszellen können außerdem Zellen in ihrer Umgebung dazu nutzen, das Immunsystem zu schwächen, indem sie beispielsweise die Vermehrung unreifer Knochenmarkszellen, sogenannter myeloider Suppressorzellen, stimulieren, die die Aktivität von T-Zellen reduzieren.
Über solche Strategien können sich Krebszellen der Immunabwehr entziehen, was aber nicht bedeutet, dass sich Krebs als Folge eines Immundefekts oder einer Immunschwäche ausbildet. Ziel der Krebsimmuntherapie ist, die Tarnung der Krebszellen zu durchbrechen, ihnen quasi die Tarnkappe zu entreißen, so dass es ihnen nicht mehr möglich ist, das Immunsystem auszutricksen.
Strategien der Enttarnung
Checkpoint-Inhibitoren: Eine Möglichkeit, wie Krebszellen sich tarnen, ist sehr gut untersucht und wird bereits therapeutisch genutzt: die Bildung spezifischer Krebsantigene, die als Signalstoffe Schaltstellen des Immunsystems, die sogenannten Checkpoints, blockieren können. Bei den Checkpoints handelt es sich um Kontrollstationen, die die Funktion des Immunsystems überwachen. Dies geschieht über Checkpoint-Rezeptoren auf der Oberfläche der Zellen des Immunsystems. Ihre Gegenspieler – die Checkpoint-Liganden – sind auf der Oberfläche von körpereigenen Zellen exprimiert. Die Interaktion zwischen den Checkpoint-Rezeptoren und -Liganden ist für das Erkennen von Selbst und Fremd durch das Immunsystem verantwortlich. Wird eine Zelle als fremd und damit als potenziell schädigend erkannt, folgt in aller Regel eine Immunreaktion zu ihrer Vernichtung.
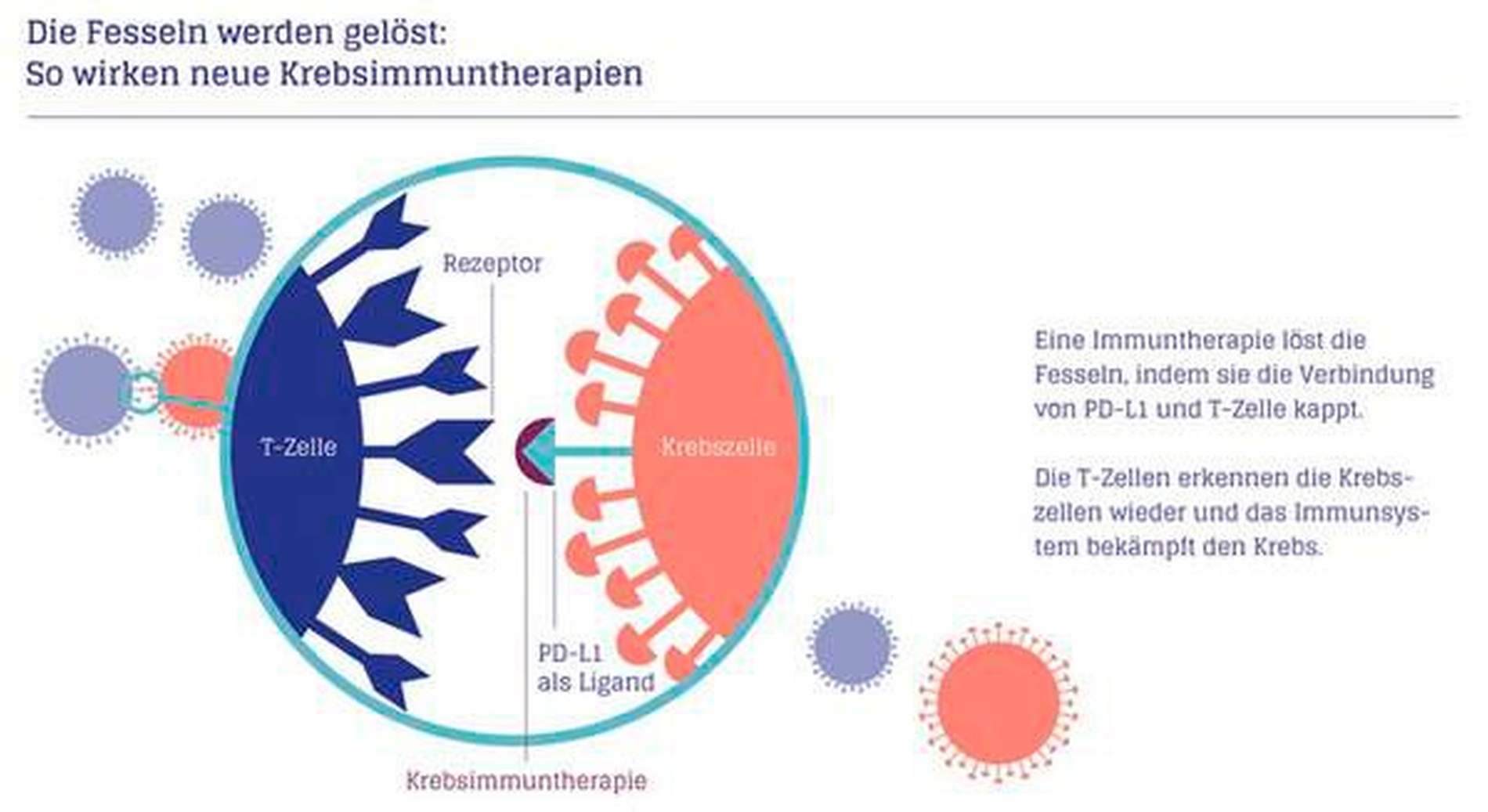
Entziehen können sich Tumorzellen der Immunabwehr zum Beispiel, indem sie den „Programmed Death Ligand 1“, kurz PD-L1 exprimieren. Der Ligand interagiert mit dem Rezeptor PD-1 auf Immunzellen, die dadurch deaktiviert werden. PD-L1 wirkt somit wie eine Art Stoppschild auf das Immunsystem, die Krebszelle unterliegt nicht mehr der Immunkontrolle.
Durch die Entwicklung spezifischer Immun-Checkpoint-Inhibitoren, die PD-1-Inhibitoren, die ihrerseits mit dem PD-1-Rezeptor interagieren, kann jedoch die durch die Tumorzelle gesetzte Blockade gelöst, respektive das Setzen der Blockade verhindert werden. Eine Art Weiterentwicklung sind die PD-L1-Inhibitoren. Diese greifen nicht primär am Rezeptor, sondern an den von Tumorzellen freigesetzten Krebsantigenen PD-L1 an und verhindern damit die Blockade der Immunzellen.
Vertreter beider Wirkstoffgruppen sind bereits erfolgreich in der klinischen Anwendung. Beispiele sind der Hautkrebs, das Lungen-, das Blasen- und das Nierenzellkarzinom. So wurde beispielsweise in Studien beim nicht kleinzelligen Lungenkarzinom (NSCLC) gezeigt, dass durch eine Krebsimmuntherapie die Überlebenschancen der Patienten statistisch signifikant verbessert werden können. Erforscht wird die neue Antitumor-Strategie außerdem beim Lymphom, beim Sarkom sowie beim Darm-, Eierstock- und Prostatakrebs. Die Krebsimmuntherapeutika werden bislang lediglich bei Patienten mit fortgeschrittener Tumorerkrankung eingesetzt und das zudem als Monotherapie. In Studien wird jedoch auch bereits die Anwendung als Kombinationstherapie zusammen mit einer Chemotherapie oder mit einer sogenannten zielgerichteten Therapie (Targeted Therapy) untersucht.
Allerdings sprechen der Deutschen Krebsgesellschaft zufolge nicht alle Patienten mit Hautkrebs, Nierenzell- oder Lungenkarzinom gleich gut auf eine Immuntherapie an. Warum die Krebszellen unterschiedlich reagieren, ist aber bisher nicht eindeutig geklärt. Die Krebsimmuntherapie wird in aller Regel ambulant durchgeführt, wobei die Wirkstoffe je nach Tumor alle zwei bis drei Wochen als Infusion oder über einen Port verabreicht werden.
Zwischen Experiment und klinischer Anwendung
Die Behandlung ist im Allgemeinen gut verträglich, als häufigste Nebenwirkungen werden Müdigkeit, Hautausschläge, Fieber, Appetitlosigkeit, Übelkeit und möglicherweise auch Autoimmunreaktionen angegeben. Die Nebenwirkungen sind jedoch meist moderat und gut zu beherrschen, die Krebsimmuntherapie gilt als deutlich besser verträglich im Vergleich zu einer Chemotherapie.
CAR-T-Zellen
Eine andere Strategie, den Tumor für das Immunsystem zu enttarnen, wird mit der Entwicklung von CAR-T-Zellen versucht. Das Verfahren ist hochkomplex: Zunächst werden dem Patienten T-Lymphozyten aus dem Blut entnommen. Bei einem gentechnischen Eingriff wird den Zellen dann ein chimärer Antigenrezeptor (Chimeric Antigen Receptor, kurz CAR) eingeführt. Die so gebildeten CAR-T-Zellen werden dem Patienten intravenös rückinfundiert, informiert die Deutsche Gesellschaft für Hämatologie und Onkologie (DGHO).
Die CAR-T-Zellen sind in der Lage, spezifische Antigene auf den Krebszellen zu erkennen, mit ihnen zu interagieren und eine charakteristische T-Zell-Immunantwort auszulösen, durch die die Krebszellen zerstört werden. Diese Therapie ist allerdings nicht ungefährlich, warnt die DGHO: „Es kann zu einem lebensbedrohlichen, sogenannten Zytokin-Release-Syndrom kommen mit zum Teil schweren neurologischen Komplikationen.“ Andererseits bietet diese zelluläre Immuntherapie wahrscheinlich Potenzial für weitere Behandlungsfortschritte bei hämatologischen und auch soliden Malignomen.
Therapeutische Impfung
Noch experimentell ist der Ansatz der „therapeutischen Impfung gegen Krebs“. Dabei wird versucht, das Immunsystem gezielt gegen Tumorantigene „aufzuhetzen“. Die Bezeichnung „therapeutische Impfung“ signalisiert, dass das Verfahren nicht wie eine herkömmliche Schutzimpfung vorbeugend eingesetzt wird, sondern erst, wenn sich bereits ein Tumor gebildet hat.
„Geimpft“ werden die Patienten dabei mit Teilen von Krebszellen oder auch mit Immunzellen, die außerhalb des Körpers mit Tumorantigenen beladen und vermehrt werden. Die Zellen tragen dann Tumorantigene, also Merkmale, die typisch für Krebszellen sind und auf gesunden Körperzellen gar nicht oder nur in anderer Form vorkommen, auf ihrer Oberfläche. Die Forscher hoffen, dass die Konfrontation des Immunsystems mit einer größeren Menge der Tumorantigene dazu führt, dass eine effektivere Immunantwort gegen den Tumor erfolgt.
Dendritische Zellen
Bei einem weiteren – ebenfalls noch experimentellen – Ansatz werden spezielle Immunzellen, die dendritischen Zellen, als Helfershelfer eingesetzt. Die dendritischen Zellen nehmen üblicherweise Antigene auf, präsentieren diese anderen Immunzellen und stimulieren damit die Immunantwort auf ein bestimmtes Antigen. Getestet wird in den pharmazeutischen Labors deshalb unter anderem, ob das Immunsystem Tumorantigene eventuell besser erkennt, wenn sie von den eigenen dendritischen Zellen präsentiert werden.
Die „Dendritische Zelltherapie“ ist sehr aufwendig, da die Immunzellen den Patienten entnommen, mit den Tumorantigenen „beladen“ und dann reinfundiert werden müssen. Zurück im Körper sollen sie weitere Immunzellen aktivieren und damit eine spezifische Immunantwort gegen die Tumorantigene hervorrufen.
Versucht wird außerdem, Immunzellen des Patienten, die für die Zerstörung von schädigenden Fremdzellen im Organismus verantwortlich zeichnen, wie etwa die sogenannten Killerzellen, im Labor durch spezielle Botenstoffe – die Zytokine – zu vermehren und über solche Zytokin-induzierten Killerzellen die Immunreaktion gegen den Tumor zu stimulieren.
Derzeit sind weitere Verfahren in Erprobung, von denen die Forscher sich Fortschritte einer Immuntherapie bei Krebserkrankungen versprechen. Das Prinzip besteht in aller Regel darin, über verschiedenste Strategien Immunzellen des Patienten so zu verändern, dass sie nach der Reinfusion Immunreaktionen gegen den Tumor stimulieren.
Aus Sicht der Zahnmedizin
Krebsprävention bei oropharyngealen Karzinomen durch HPV
Derzeit sind über 200 verschiedene Varianten des vor allem sexuell übertragenen Humanen Papillomavirus (HPV) bekannt, von denen nur wenige (unter anderem HPV 16, 18, 31, 33, 35) ein onkogenes Potenzial haben. Hier sind vor allem die anogenitale Region (anale (bis zu 95 Prozent durch HPV verursacht) und Cervixkarzinome (bis zu 70 Prozent durch HPV verursacht)) betroffen, wobei HPV auch eine Rolle bei der Entstehung oropharyngealer Krebserkrankungen zu spielen scheint. Derzeit sind HPV-Impfungen ein wichtiges Mittel bei der Prävention von HPV-Infektionen und anderer HPV-vermittelter Pathologien. Die prophylaktischen Impfstoffe wirken primär durch die Stimulierung der Antikörper-vermittelten Immunität. Sie induzieren neutralisierende Antikörper, die in der Lage sind, HPV zu erkennen und zu inaktivieren, bevor das Virus Wirtszellen infiziert. Allerdings haben die derzeit verfügbaren HPV-Impfungen keinen Effekt bei bereits bestehenden Infektionen.
Impfen gegen oropharyngeale Karzinome? | Foto: MEV
Impfen gegen oropharyngeale Karzinome?
Aktuelle Studien gehen von einem signifikanten Anstieg von durch HPV verursachten oropharyngealen Karzinomen (OPC) aus. So prognostizieren einige Autoren, dass bis 2030 ungefähr die Hälfte aller OPC mit HPV assoziiert sein wird, wobei bei den häufig jüngeren, gesünderen Patienten die klassischen Risikofaktoren Rauchen und Alkoholabusus weitaus weniger vorliegen. Es handelt sich hier vor allem um Manifestationen an den Tonsillen und an der Zunge.
Angesichts der Tatsache, dass die meisten HPV-bezogenen OPC (rund 90 Prozent) durch HPV Typ 16 verursacht werden, ein Typ, der sowohl in den Cervarix®- als auch in den Gardasil®-Impfstoffen enthalten ist, könnte man erwarten, dass diese Impfstoffe auch die oropharyngeale HPV16/18-Infektion verhindern könnten. Da jedoch die Prävention einer oropharyngealen HPV-Infektion durch HPV-Impfung bisher nicht in randomisierten Studien untersucht wurde, ist der Wert der Impfung als prophylaktische Maßnahme für OPC noch unbewiesen. Dies liegt zum einen darin begründet, dass die Assoziation zwischen einer HPV-Infektion und Malignomen im oropharyngealen Bereich noch nicht ausreichend lang bekannt ist. Weiterhin ist es unklar, ob bei einer HPV-Infektion potenziell maligne Vorläuferläsionen vorliegen, die bei asymptomatischen Patienten zudem nur schwer zu untersuchen wären. Allerdings deuten erste Studien sehr wohl darauf hin, dass die Impfung auch bei OPC wirksam ist.
Ausblick
Für den Gebärmutterhalskrebs sind Impfung und Screening inzwischen gut etabliert. Bei einer vermutlich zunehmenden Inzidenz von HPV-assoziierten oropharyngealen Karzinomen wird die Impfung beider Geschlechter hoffentlich zu einer Verringerung der Inzidenz führen. Auch wenn die Kosten und insbesondere die Kosten-Effektivität nicht geklärt ist, sollten eine präventive Impfung für HPV weltweit gefördert werden.
Univ.-Prof. Dr. Dr. Monika Daubländer
Leitende Oberärztin der Poliklinik für Zahnärztliche Chirurgie
Universitätsmedizin der Johannes Gutenberg-Universität Mainz
Poliklinik für Zahnärztliche Chirurgie
Augustusplatz 2, 55131 Mainz
daublaen@uni-mainz.de
PD Dr. Dr. Peer W. Kämmerer
Klinik und Poliklinik für Mund-, Kiefer- und Plastische Gesichtschirurgie der Universität Rostock,
Schillingallee 35, 18057 Rostock
Quellen und weitere Informationen: