Die implantologische Versorgung der Einzelzahnlücke
Mitte des 20. Jahrhunderts stellte der schwedische Orthopäde Per-Ingvar Brånemark († 2014) bei Tierversuchen zur Erforschung der Blutzirkulation bei der Knochenheilung zufällig fest, dass sich Titan bei Kontakt mit dem Knochen dem Anschein nach fest mit diesem verbindet. Das entdeckte Phänomen nannte Brånemark „Osseointegration“. In der Folgezeit stellte er ein interdisziplinäres Team zusammen, um weiter auf diesem Gebiet zu forschen – das Ziel war die Entwicklung künstlicher Zahnwurzeln.
1965 war es dann soweit: Brånemark inserierte einem Patienten mit vorgeschädigtem Kiefer die ersten Zahnimplantate aus Titan. Der Erfolg war erstaunlich: Die Implantate blieben über 40 Jahre in situ – bis zum Tod des Patienten. Trotz dieser vielversprechenden Ergebnisse blieb man in der schwedischen Zahnärzteschaft zunächst skeptisch gegenüber Brånemarks Forschungen. Erst Anfang der 1980er-Jahre, anlässlich einer wissenschaftlichen Vorstellung des Prinzips der Osseointegration von Titanimplantaten im kanadischen Toronto, wurde ihm – nun auch gleich international – die verdiente Anerkennung zuteil [Brånemark, 1983; Brånemark et al., 1983].
Seitdem nimmt der Anteil an dentalen Implantaten kontinuierlich zu und hat sich laut der Fünften Deutschen Mundgesundheitsstudie (DMS V) zwischen 1997 und 2014 verzehnfacht [Cholmakow-Bodechtel et al., 2016]. Die hohen Überlebensraten von mehr als 93 Prozent nach zehn Jahren [Pjetursson et al., 2012; Moraschini et al., 2015] sind ein Beleg für die Nachhaltigkeit dieses Trends. Vor allem bei gesunden Nachbarzähnen stellen Implantate für die Versorgung der Einzelzahnlücke eine echte Alternative zu Klebe- und konventionellen Kronenbrücken dar.
Indikationen der implantologischen Versorgung
Beim Beratungsgespräch mit dem Patienten sollten kritische Faktoren, die einer erfolgreichen Osseointegration entgegenwirken, erkannt und angesprochen werden. Risikofaktoren lassen sich zweckmäßig in allgemeine, temporäre und lokale Faktoren unterteilen. Zu den allgemeinen Risikofaktoren zählen beispielsweise schwerwiegende systemische Erkrankungen des Knochens und deren intravenöse Therapie mit Bisphosphonaten, des Stoffwechsels, der Blutgerinnung, des Immunsystems oder des Kreislaufsystems. Zusätzlich zählen zu dieser Kategorie auch ein Diabetes mellitus, eine Hochdosisbestrahlung im Kopf-Hals-Bereich oder ein Nikotinabusus. In Abhängigkeit von der Ausprägung kann dabei eine absolute oder eine relative Kontraindikation bestehen. Zu den temporären Risikofaktoren zählt beispielsweise eine unbehandelte Parodontitis. Lokal können pathologische Habits wie ein ausgeprägter Bruxismus oder ein starker Knochenabbau die implantatprothetische Versorgung einschränken. Hierzu zählt auch die vorhandene Lückenbreite. Als Richtwert für die Versorgung einer Schaltlücke sollte eine Breite von ungefähr 7 mm vorliegen. Diese kann im Zweifel auch anhand von Situationsmodellen beurteilt werden.
Generell lässt sich festhalten, dass das Spektrum der absoluten Kontraindikationen durch die wachsenden Kenntnisse in der modernen Implantologie schrumpft, im Gegenzug der Umfang am notwendigen Management von Risikofaktoren jedoch zunimmt. Regelmäßige Anpassungen der (Kontra-)Indikationen erfolgen anhand der aktuellen Literatur und Leitlinien. Für den implantierenden Zahnarzt ist es deshalb ratsam, sich regelmäßig über den aktuellen Stand der Empfehlungen auf dem Laufenden zu halten.
Selbst wenn alle Risikofaktoren adäquat berücksichtigt sind und die Behandlung vollumfänglich lege artis erfolgt ist, können sowohl technische Komplikationen wie Schraubenlockerungen und Keramik-Frakturen als auch biologische Komplikationen wie eine Periimplantitis im Ergebnis auftreten [Pjetursson et al., 2007; Pjetursson et al., 2012; Marrone et al., 2013; Sailer et al., 2018]. Auf diese Behandlungssituationen sollte der implantierende Zahnarzt vorbereitet sein.
Digitale Techniken in Planung und Umsetzung
Die korrekte dreidimensionale (3-D) Insertion eines Zahnimplantats ist eine der wichtigsten Voraussetzungen für einen langfristigen Behandlungserfolg [Beretta et al., 2014; Tahmaseb et al., 2014]. Dabei sorgt die 3-D-Bildgebung für eine bessere Vorhersagbarkeit der Ergebnisse. Mit der Einführung der Digitalen Volumentomografie (DVT) konnten Kosten, Größe, Komplexität und Strahlendosis der Geräte im Vergleich zur Computertomografie (CT) maßgeblich reduziert werden [Guerrero et al., 2006; Bornstein et al., 2014; Nasseh und Al-Rawi, 2018]. Die resultierenden DICOM-Datensätze (DICOM – Digital Imaging and Communications in Medicine) ermöglichen es, präoperativ ein prothetisches Ziel mit den anatomischen Informationen wie den Weichgeweben und dem darunter liegenden Knochen zu kombinieren. Dafür sind zusätzlich die Oberflächendaten der intraoralen Ausgangssituation und ein Wax-up/ Set-up der prothetischen Planung als digitale Datensätze notwendig. Diese können über labortechnische Zwischenschritte wie die Digitalisierung zugehöriger Gipsmodelle mit Laborscannern oder direkt mittels intraoraler Scanner (IOS) gewonnen werden. Auch das Wax-up/Set-up kann sowohl über den konventionellen als auch über den digitalen Weg erstellt werden.
Die gewonnenen Daten werden in der Regel als „Standard Triangle/Tessellation Language“ (STL)-Datensätze exportiert und für die Erstellung eines virtuellen 3-D-Patienten in einer Implantatplanungssoftware (IPS) genutzt. Nach der erfolgreichen Überlagerung der DICOM- und der STL-Daten in der IPS kann das Implantat mit Blick auf das prothetische Ziel idealisiert im Knochen ausgerichtet werden. Dadurch werden auch gegebenenfalls notwendige Knochen- und Weichgewebsaugmentationen bereits vor dem chirurgischen Eingriff absehbar und können entsprechend eingeplant werden. Die virtuell geplante Implantatposition kann mithilfe der dynamischen oder der statischen Navigation und klinisch geringen Abweichungen von < 2 mm auf den Patienten übertragen werden [Tahmaseb et al., 2018; Pellegrino et al., 2021]. Das beschriebene Vorgehen wird auch als Backward-Planning bezeichnet.
Im Folgenden wird die implantologische Versorgung der Einzelzahnlücke exemplarisch anhand eines Fallbeispiels erläutert. Dabei werden auch weiterführende Informationen zu Alternativen und wissenschaftlichen Hintergründen gegeben.
Die Implantation am Fallbeispiel
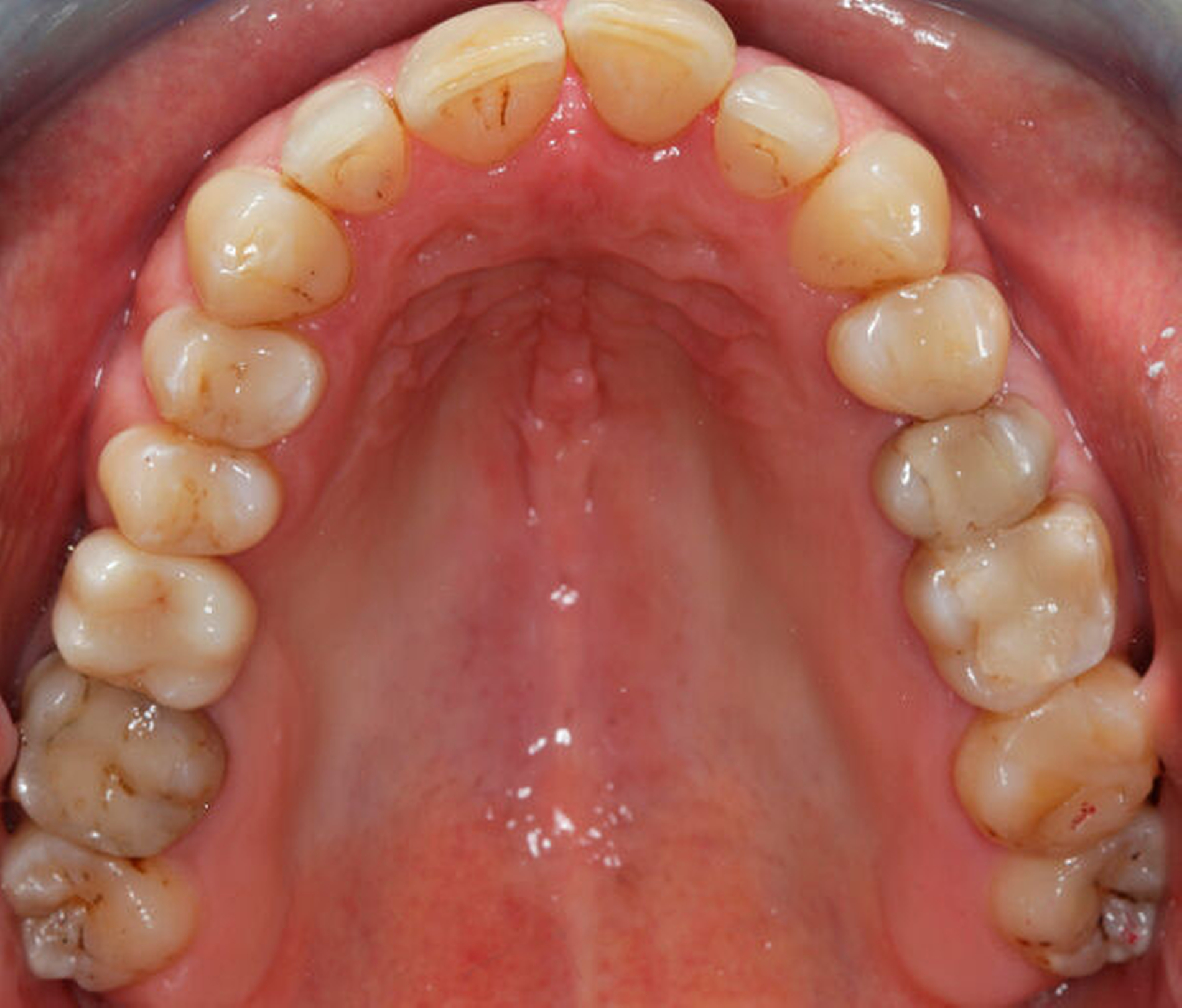
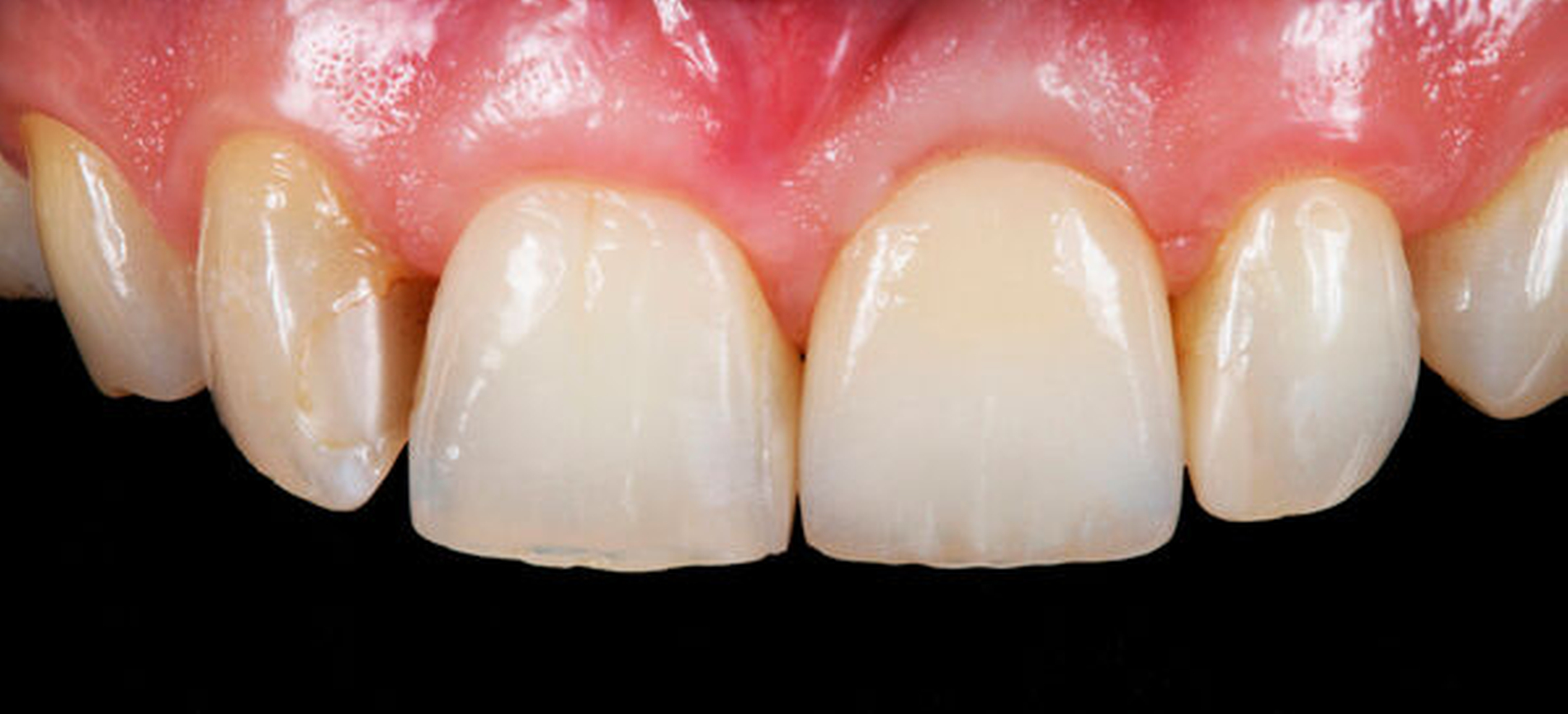
Das Fallbeispiel beschreibt das Vorgehen bei einem 38-jährigen, gesunden Patienten mit einer Einzelzahnlücke in Regio 16 (Abbildung 1). Laut Anamnese lagen keine Kontraindikationen für eine Implantation vor. Es bestand eine suffiziente Mundhygiene. Alle notwendigen Vorbehandlungen waren abgeschlossen. Das Implantat konnte wie geplant inseriert und nach Abschluss einer dreimonatigen Einheilzeit mit einer transokklusal verschraubten monolithischen Keramikkrone aus Lithiumdisilikat versorgt werden. Seit der Implantation im Mai 2019 wurden keine Komplikationen dokumentiert.
Intraorale Ausgangssituation und Wax-up
Zunächst erfolgten analoge Abformungen mit Rim-Lock-Löffeln des zu implantierenden Oberkiefers (Vinylpolyethersilikon: EXA‘lence, GC Corporation, Tokio, Japan) und des Unterkiefers (Alginat rosa, Omnident Dental-Handelsgesellschaft mbH, Rodgau Nieder-Roden). Zur Kieferrelation wurde die habituelle Okklusion verschlüsselt (LuxaBite, DMG Chemisch-Pharmazeutische Fabrik GmbH, Hamburg). Das prothetische Ziel wurde mithilfe eines analogen und vom Oberkiefermodell abnehmbaren Wax-ups definiert. Dieses sollte in seiner Ausdehnung und Funktion der zukünftigen implantatgetragenen Versorgung entsprechen und für die Planung genutzt werden können. Für das Backward-Planning wurden die Modelle und das Wax-up mithilfe eines Laborscanners (D2000, 3Shape A/S, Kopenhagen, Dänemark) digitalisiert. Die Oberflächendaten wurden als STL-Datensätze exportiert, um diese später für die Erstellung eines virtuellen 3-D-Kiefers in einer IPS zu nutzen.
Der hier beschriebene Workflow mit einer Kombination aus konventionellen und digitalen Methoden ist für jede Praxis auch ohne digitale Ausstattung umsetzbar. Des Weiteren können die angefertigten Modelle für die Einprobe und das Anpassen der Bohrschablone genutzt werden. Ungeachtet dessen stellt ein voll digitaler Workflow mithilfe eines intraoralen Scanners (IOS) eine gute Alternative dar. Mittlerweile stehen diverse IOS unterschiedlicher Anbieter zur Verfügung. Deren Genauigkeit ist für diagnostische Zwecke und kurzspannige Scans vergleichbar mit der konventioneller Abformungen [Abduo und Elseyoufi, 2018].
Wichtig ist, dass eine Veränderung der intraoralen klinischen Situation nach der erfolgten Abformung dringend vermieden werden sollte, um eine möglichst genaue Überlagerung in der IPS und die anschließende Passung der Bohrschablone nicht zu gefährden.
Röntgenologische Bildgebung
Für die dreidimensionale Beurteilung des Knochenangebots wurde zunächst ein digitales Volumentomogramm (Veraviewpocs 3D R100, J. Morita Europe GmbH, Dietzenbach) angefertigt. Der zugehörige Datensatz wurde für die ausstehende Planung in der IPS als DICOM-Datensatz exportiert. DICOM ist ein Standardformat für die Speicherung und Übertragung medizinischer Bilddaten. Für eine möglichst genaue Überlagerung mit den STL-Datensätzen der intraoralen Ausgangssituation und des Wax-ups sollte die Anfertigung des Tomogramms zeitnah zu den Abformungen erfolgen. Auch hier gilt es, die klinische Situation zwischen der Röntgenaufnahme und der Operation möglichst nicht mehr zu verändern.
Alternativ sollte mit Blick auf den Strahlenschutz und das „ALARA“-Prinzip (As Low As Reasonably Achievable) die Anfertigung von Orthopantomogrammen (OPGs) mit entsprechenden Referenzkörpern (beispielsweise metallische Kugeln oder Bohrhülsen), deren geometrische Maße bekannt sind, in Erwägung gezogen werden. Dieses Verfahren wurde bereits über viele Jahre – auch vor der Einführung der DVT – für die präimplantologische Diagnostik in der Zahnmedizin angewandt. Es eignet sich jedoch nicht für die Verwendung im digitalen Workflow und in modernen IPS. Darüber hinaus kann es nachteilig sein, dass sich anatomisch kritische Strukturen mit der zweidimensionalen Bildgebung der OPGs schlechter beurteilen lassen [Jacobs und Quirynen, 2014].
Überlagerung der Datensätze (Matching)
Die Überlagerung der STL- und der DICOM-Datensätze in einer IPS wird auch als Matching bezeichnet. Es ist notwendig, da die Zeichenschärfe der DICOM-Daten für die Herstellung einer passgenauen Bohrschablone nicht ausreichend ist. Das Matching erfolgte im dargestellten Patientenfall über eine manuelle Auswahl dreier markanter korrespondierender Punkte auf den dreidimensionalen Datensätzen der intraoralen Ausgangssituation (STL), des Wax-ups (STL) und des Tomogramms (DICOM) in der IPS (SMOP, SwissmedaAG, Baar, Schweiz, Abbildung 2). Aufgrund der Qualität der vorliegenden Datensätze erfolgte die Überlagerung problemlos.
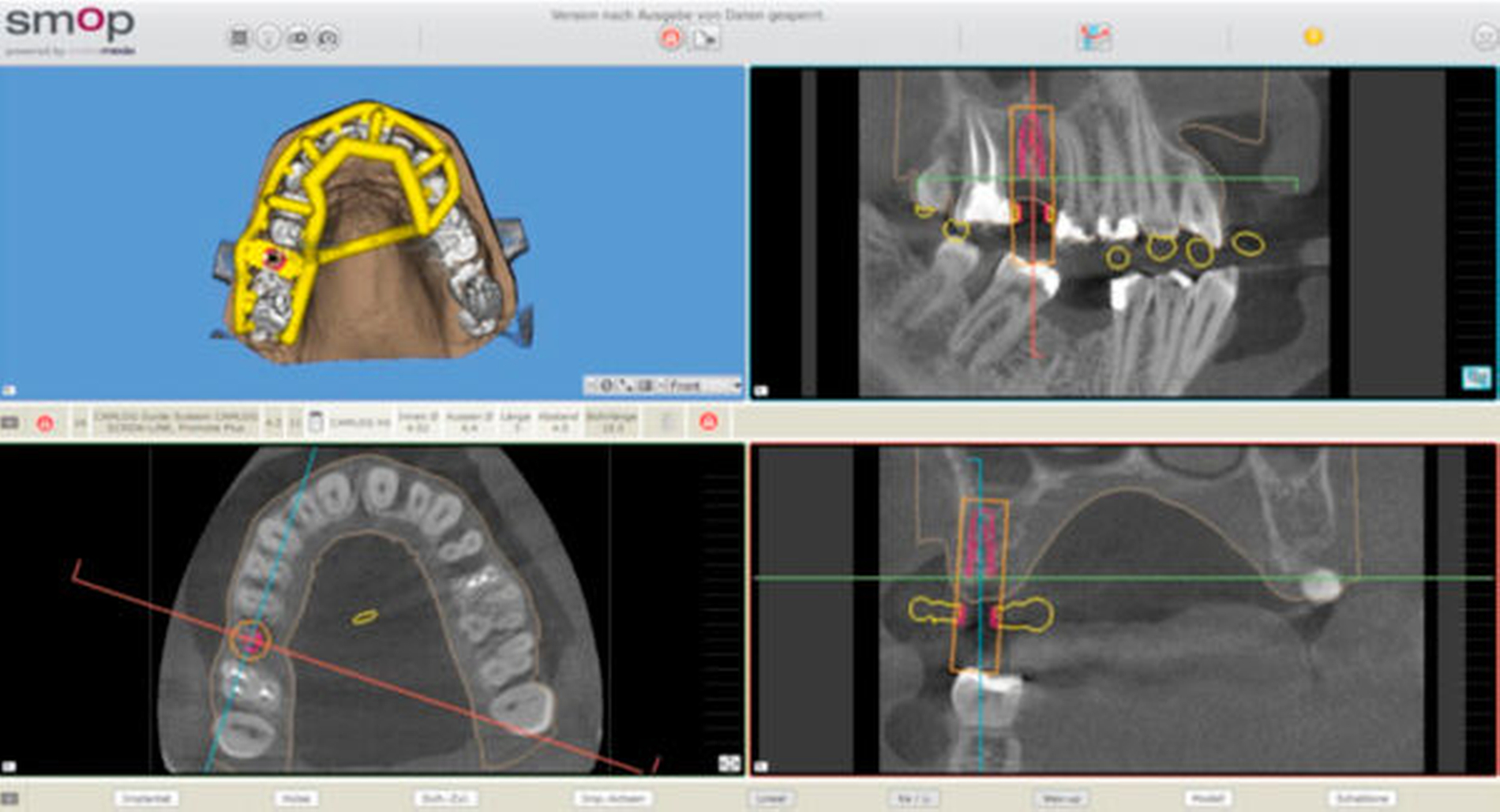
Für eine möglichst exakte Überlagerung der Datensätze sollten alle Dimensionen betrachtet werden. Die Punkte sollten möglichst leicht identifizierbar sein (beispielsweise Höckerspitzen oder -abhänge) und möglichst weit auseinanderliegen (Verteilung der Punkte oral vs. vestibulär und/oder mesial vs. distal). Je nach IPS kann die Auswahl von mehr als drei korrespondierenden Punkten notwendig sein. Streustrahlen zum Beispiel durch künstliche Kronen oder Brücken können die Auswahl der Punkte in einem Tomogramm wesentlich erschweren. Ist ein hohes Maß an Artefakten zu erwarten, sollte die Verwendung von Referenzkörpern in Erwägung gezogen werden.
Nach Abschluss des vermeintlich erfolgreichen Matchings sollte dieses nochmal kritisch durch den Implantologen beurteilt und – falls nötig – manuell korrigiert werden. Hierbei können erhebliche Abweichungen auffallen, die die Übertragung der virtuellen Implantatposition auf die reelle klinische Situation negativ beeinflussen können.
Implantatpositionierung
In der IPS wurde das Implantat in Regio 16 unterhalb des geplanten Zahnersatzes eingefügt. Aufgrund des verfügbaren Knochenangebots wurde für den vorgestellten Patientenfall aus der Datenbank der IPS das Implantat CAMLOG SCREW-LINE Promote plus (CAMLOG Vertriebs GmbH, Wimsheim) mit einem Durchmesser von 4,3 mm und einer Länge von 11 mm ausgewählt (Abbildung 2). Die angestrebte transokklusale Verschraubung bedingte die Ausrichtung des Schraubenkanals mittig in der Okklusalfläche des Wax-ups. Bei Frontzähnen empfiehlt sich für eine transokklusale Verschraubung deren Ausrichtung palatinal der Inzisalkante.
Prinzipiell können das Implantatsystem, der Durchmesser und die Länge entsprechend der individuellen Patientensituation und den Vorlieben des Behandlers angepasst werden. In den Datenbanken der unterschiedlichen IPS sind maßstabsgetreue Werte der Implantate vieler Hersteller hinterlegt. Zu beachten ist, dass diese Datenbanken regelmäßig über Software-Updates gepflegt werden müssen. Ansonsten kann es vorkommen, dass das gewünschte Implantat nicht in der Datenbank enthalten ist.
Mit Blick auf die Positionierung sollten orientierend folgende Sicherheitsabstände eingehalten werden:
Implantat zu Zahn: circa 1,5 mm
Implantat zu Implantat: circa 3 mm
Abstand zu anatomisch kritischen Strukturen: circa 2 mm [Tahmaseb et al., 2018; Pellegrino et al., 2021]
Zur Darstellung der Abstände kann in den meisten IPS ein dreidimensionaler Sicherheitszylinder um das geplante Implantat angezeigt werden, der häufig bereits mit 1,5 bis 2 mm voreingestellt ist.
Weiterhin ist die Ausbildung eines suffizienten prothetischen Austrittsprofils, auch Emergenzprofil genannt, für eine biologisch-ästhetische Versorgung erstrebenswert [Gomez-Meda et al., 2021]. Dafür muss eventuell der verwendete Implantattyp (Implantate auf Weichgewebs- vs. Implantate auf Knochenniveau) und/oder Verbindungstyp (Stoßverbindung vs. konische Verbindung, Angulation der Konusverbindung, Plattform-Switching) an die anatomischen Gegebenheiten angepasst werden. Die Schleimhautdicke sollte letztendlich circa 3 bis 4,5 mm, gemessen von der rauen Implantatoberfläche, entsprechen [Gomez-Meda et al., 2021]. Ein Implantat auf Knochenniveau mit Konusverbindung und Plattform-Switching beispielsweise muss somit tiefer in den Knochen inseriert werden können als eines mit Stoßverbindung und polierter Implantatschulter. Hierdurch wird nochmals verdeutlicht, dass die Anforderungen an die angestrebte Restauration und das verwendete Implantatsystem bereits vor der Planung bekannt sein sollten.
Eine Fehlpositionierung oder Insertion eines ungeeigneten Implantats kann im schlimmsten Fall dazu führen, dass dieses prothetisch nicht zu versorgen ist. Diese Gefahr kann durch die richtige Anwendung des Backward-Plannings minimiert werden.
Übertragung der Implantatposition
Für die Übertragung der virtuell geplanten Implantatposition überschreiten sowohl die dynamische als auch die statisch schablonengeführte Navigation keine klinisch relevanten Abweichungen. So wurden durch Tahmaseb et al. in einer Übersichtsarbeit für die statisch geführte Implantation Abweichungen von durchschnittlich 1,20 mm (1,04–1,44 mm) an der Eintrittsstelle der Implantate, 1,40 mm (1,28–1,58 mm) an den Apizes und Abweichungen von 3,50° (3,00–3,96°) in der Angulation dokumentiert [Tahmaseb et al. 2018]. Im Vergleich wurden für die dynamische Navigation kürzlich von Pellegrino et al. in einer Übersichtsarbeit Abweichungen von durchschnittlich 0,81 mm (0,68–0,94 mm) an der Eintrittsstelle der Implantate, 0,91 mm (0,77–1,05 mm) an den Apizes und Abweichungen von 3,81° (3,08–4,53°) in der Angulation dokumentiert [Pellegrino et al., 2021]. Beide Verfahren scheinen somit vergleichbar zu sein. Die wissenschaftliche Datenlage zur schablonengeführten Navigation ist jedoch noch wesentlich umfangreicher. Generell wird mit Blick auf mögliche Übertragungsfehler zwischen Planung und Implantatinsertion ein Sicherheitsabstand von 1,5 bis 2 mm empfohlen [Tahmaseb et al., 2018; Pellegrino et al., 2021].
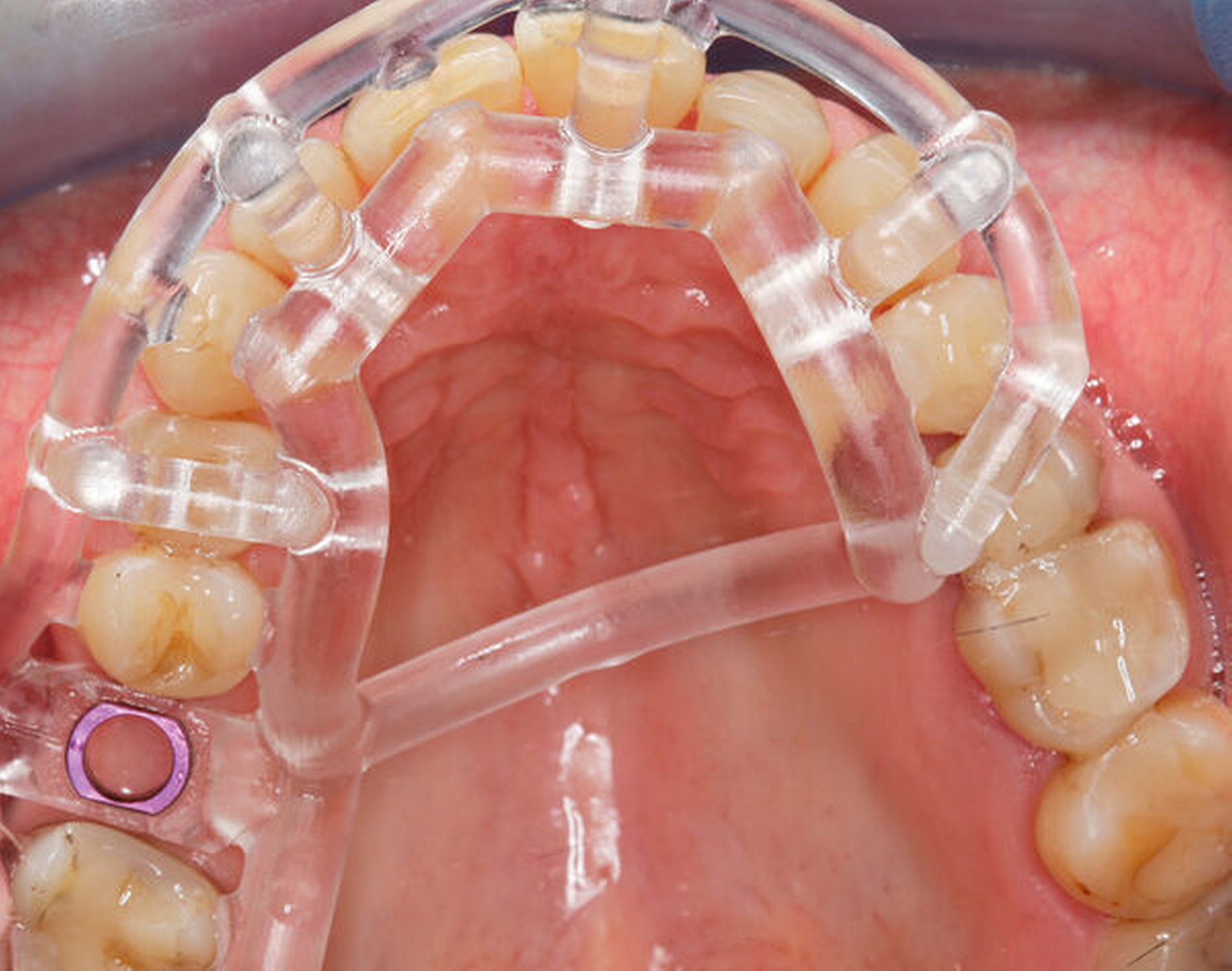
Im vorliegenden Patientenfall wurde die Implantation statisch navigiert mithilfe einer Bohrschablone und einer voll geführten Insertion durchgeführt (Abbildung 3). Dafür wurde der STL-Datensatz der Bohrschablone nach der Konstruktion in der IPS durch einen spezialisierten Mitarbeiter des Servicepartners DEDICAM (CAMLOG Vertriebs GmbH, Wimsheim) für die Bohrschablone zur Verfügung gestellt. Die Herstellung der Schablone erfolgte mithilfe eines 3-D-Druckers (Form 3, Formlabs GmbH, Berlin) im zahntechnischen Labor der Charité – Universitätsmedizin Berlin. Alternativ hierzu kann die Schablone auch vollständig fertig gestellt beim entsprechenden Anbieter bestellt werden.
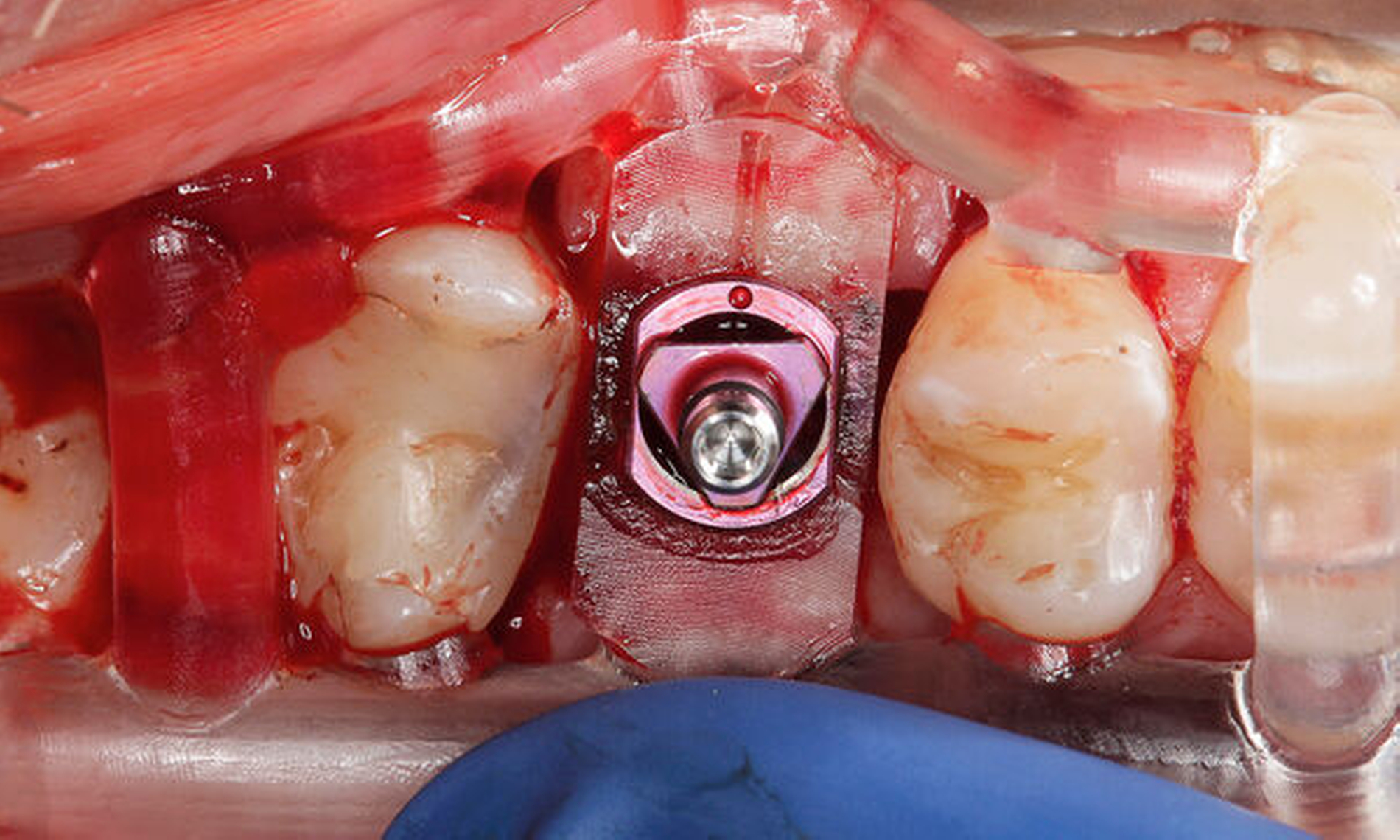
Die genaue Gestaltung der Bohrschablone ist abhängig vom Bohrprotokoll und der Führungsmethode des jeweiligen Implantatherstellers. Beim vorliegenden Patientenfall und Implantatsystem fanden die Aufbereitung des Implantatbetts und die Implantatinsertion durch eine in die Schablone eingeklebte Metallhülse statt (Abbildungen 4 und 5). Sowohl die Bohrer als auch die Einbringpfosten erreichen dabei einen definierten Tiefenstopp (Abbildung 4).
Freilegung und Abformung
Nach Abschluss der Einheilzeit muss nach einer geschlossenen Einheilung des Implantats die Freilegung erfolgen. Bei Weichgewebsdefiziten sind in Absprache mit dem Patienten hierbei gegebenenfalls zusätzliche Schleimhautplastiken indiziert. Dazu gehören beispielsweise der Rolllappen, das Freie Schleimhauttransplantat (FST) oder auch die Papillenrekonstruktionsplastik. Die Notwendigkeit von Schleimhautplastiken hängt dabei häufig nicht unwesentlich von den vorhandenen Hart- und Weichgeweben, der Implantatpositionierung und der Erwartungshaltung des Patienten ab.
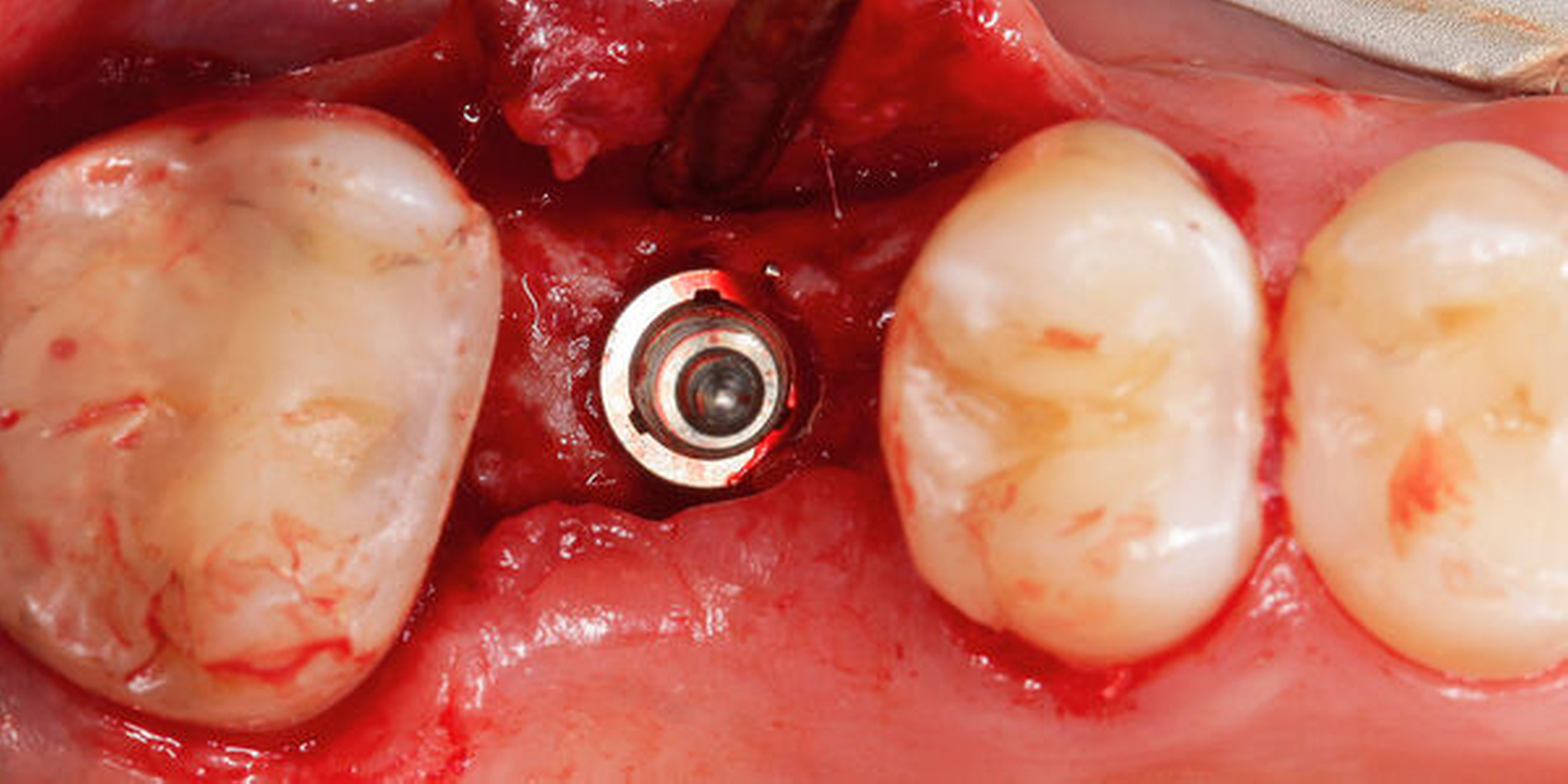
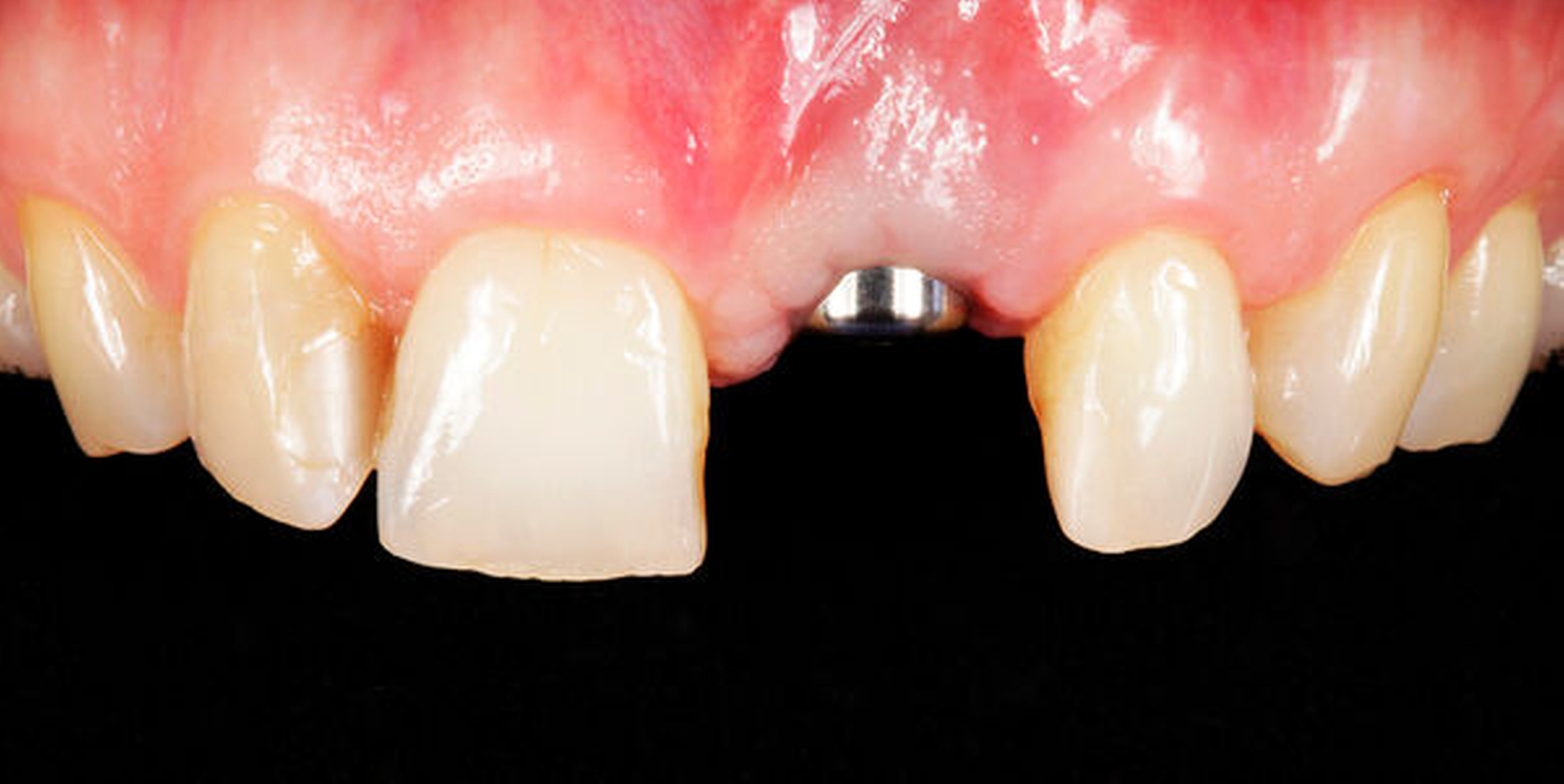
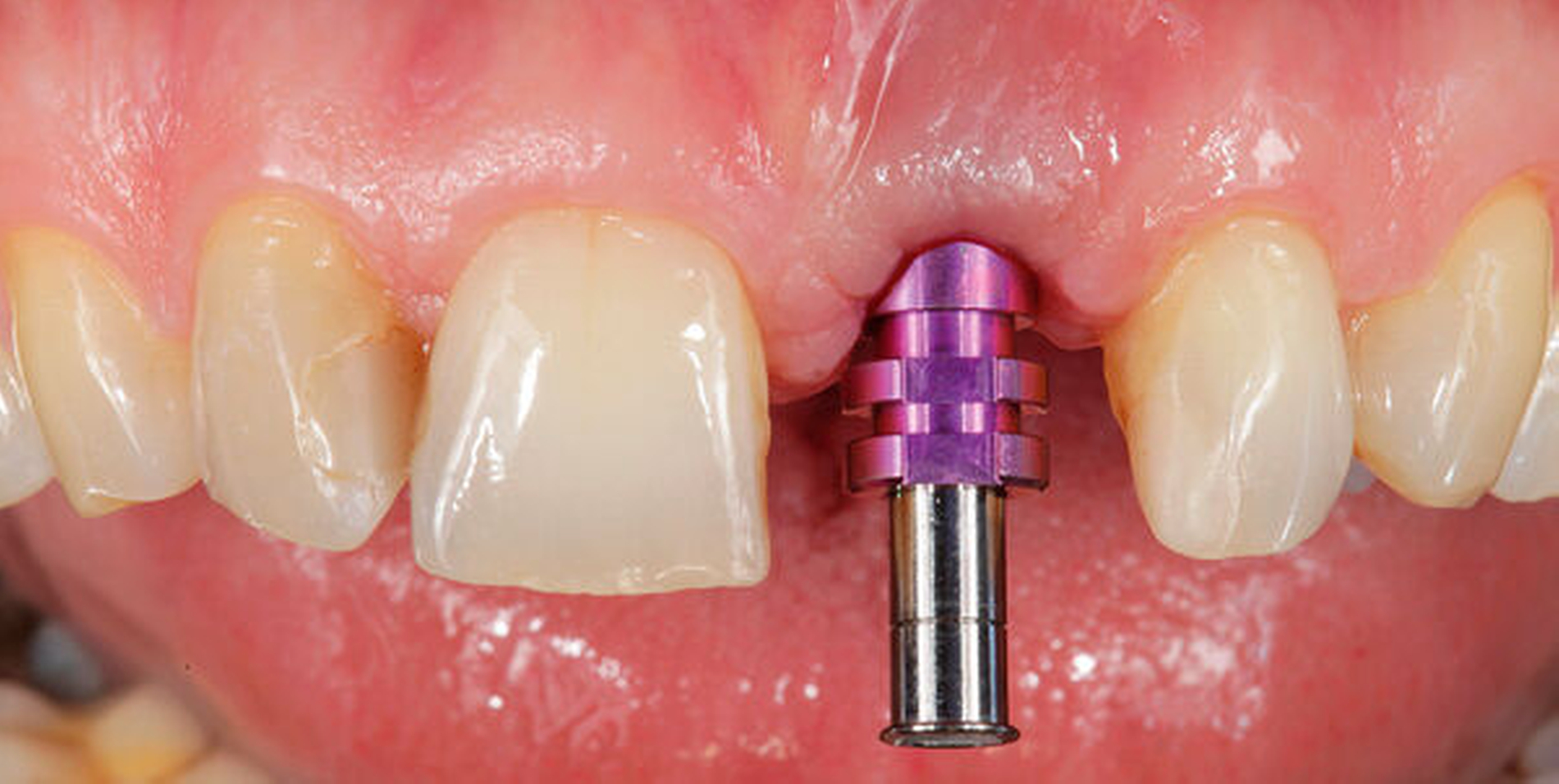
Im vorliegenden Patientenfall erfolgte die Freilegung drei Monate nach der Implantatinsertion mit einer leicht nach palatinal versetzten, krestalen Inzision in Ausdehnung bis zu den Nachbarzähnen. Dadurch wurde unter Verwendung eines konfektionierten Gingivaformers die Schleimhaut zur Verbesserung des vestibulären Defizits leicht nach bukkal verschoben. Die Fixation des Lappens erfolgte mit einer mesialen und einer distalen Einzelknopfnaht (Prolene 6–0, Ethicon Inc., Raritan, USA, Abbildung 6).
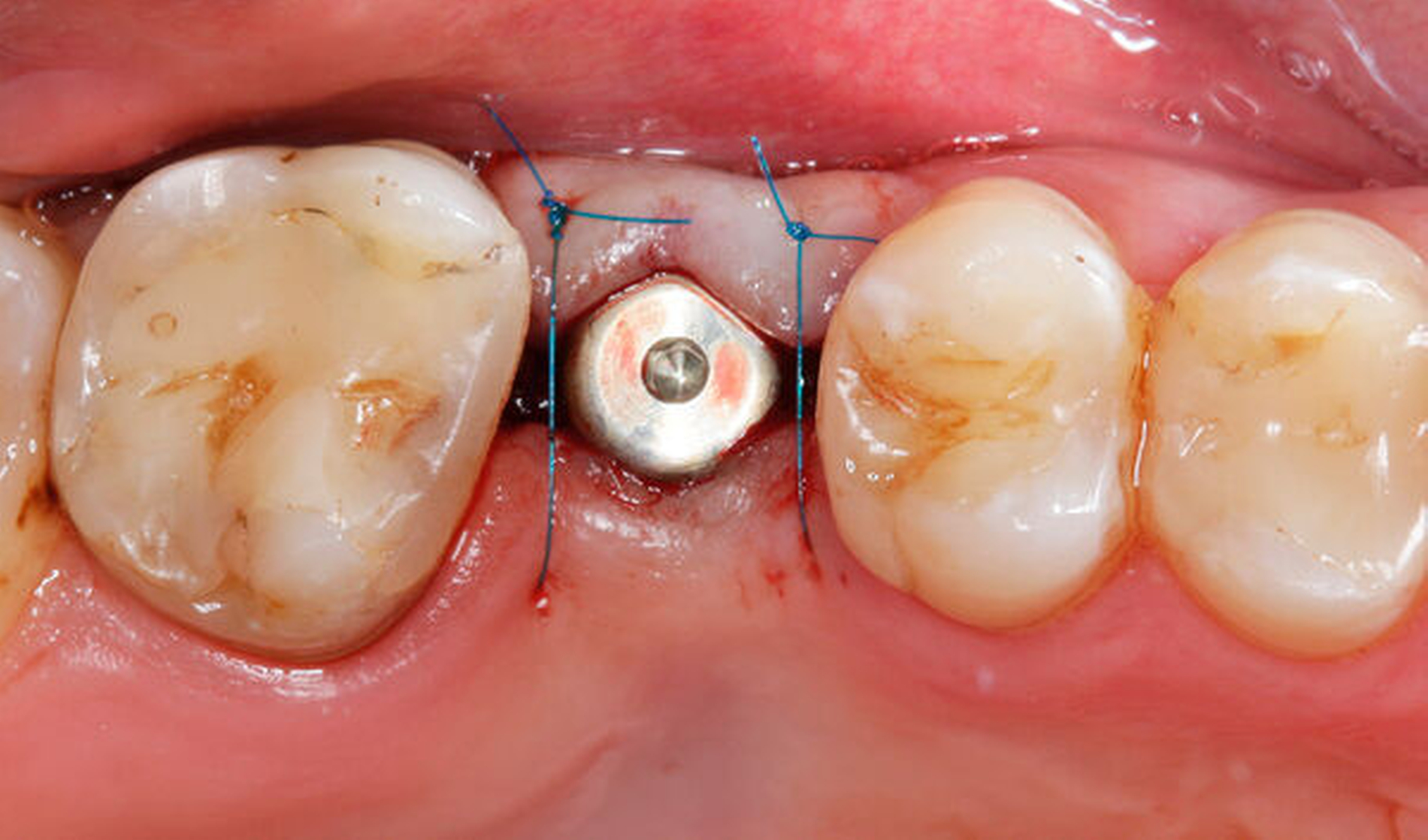
Zwei Wochen nach der Freilegung fand die Abformung für den definitiven Zahnersatz statt. Aus didaktischen Gründen erfolgte diese sowohl konventionell mit einem offenen Abformpfosten und Polyether-Abformmaterial (Impregum, 3M Deutschland GmbH, Neuss) als auch digital mithilfe eines Scankörpers und eines IOS (Trios 3, 3Shape A/S). Digitale Scans scheinen dabei eine vergleichbare 3-D-Genauigkeit wie herkömmliche Implantatabformungen zu besitzen [Papaspyridakos et al., 2020]. Diese Ergebnisse basieren insbesondere auf In-vitro-Studien und müssen noch durch weitere Untersuchungen verifiziert werden. Der intraorale Scan kann vor allem für den Patienten mit Blick auf den Verzicht von Abdruckmasse komfortabler sein.
Als dritte Abformalternative ist die geschlossene Implantatabformung zu nennen. Diese unterscheidet sich mit Blick auf den Abformpfosten und die Verwendung eines konventionellen Abformlöffels.
Herstellung und Eingliederung des Zahnersatzes
Für die Befestigung einer implantatverankerten Einzelkrone können übergeordnet zwei Möglichkeiten unterschieden werden: (1) die transokklusale Verschraubung der Restauration und (2) das Zementieren der Krone auf einem individuellen oder konfektionierten Abutment. Während zementierte implantatretinierte Kronen zu biologischen Komplikationen neigen, werden für verschraubte, implantatgetragene Restaurationen in der Literatur eher technische Komplikationen in Form von Schraubenlockerungen und Retentionsverlusten beschrieben [Sailer et al., 2012]. Die Entscheidung kann von der technischen Machbarkeit und einer Abwägung der Vor- und Nachteile abhängen [Wittneben et al., 2017]. Auch die verwendbaren Materialien (beispielsweise Lithiumdisilikat vs. Zirkoniumdioxid für die Herstellung der Krone und das Material, die Beschichtung und die Individualisierung der Implantatabutments) werden in der Literatur als Entscheidungsfaktoren fortwährend diskutiert [Linkevicius und Apse, 2008; Bressan et al., 2011; Linkevicius, 2017; Lops et al., 2017].
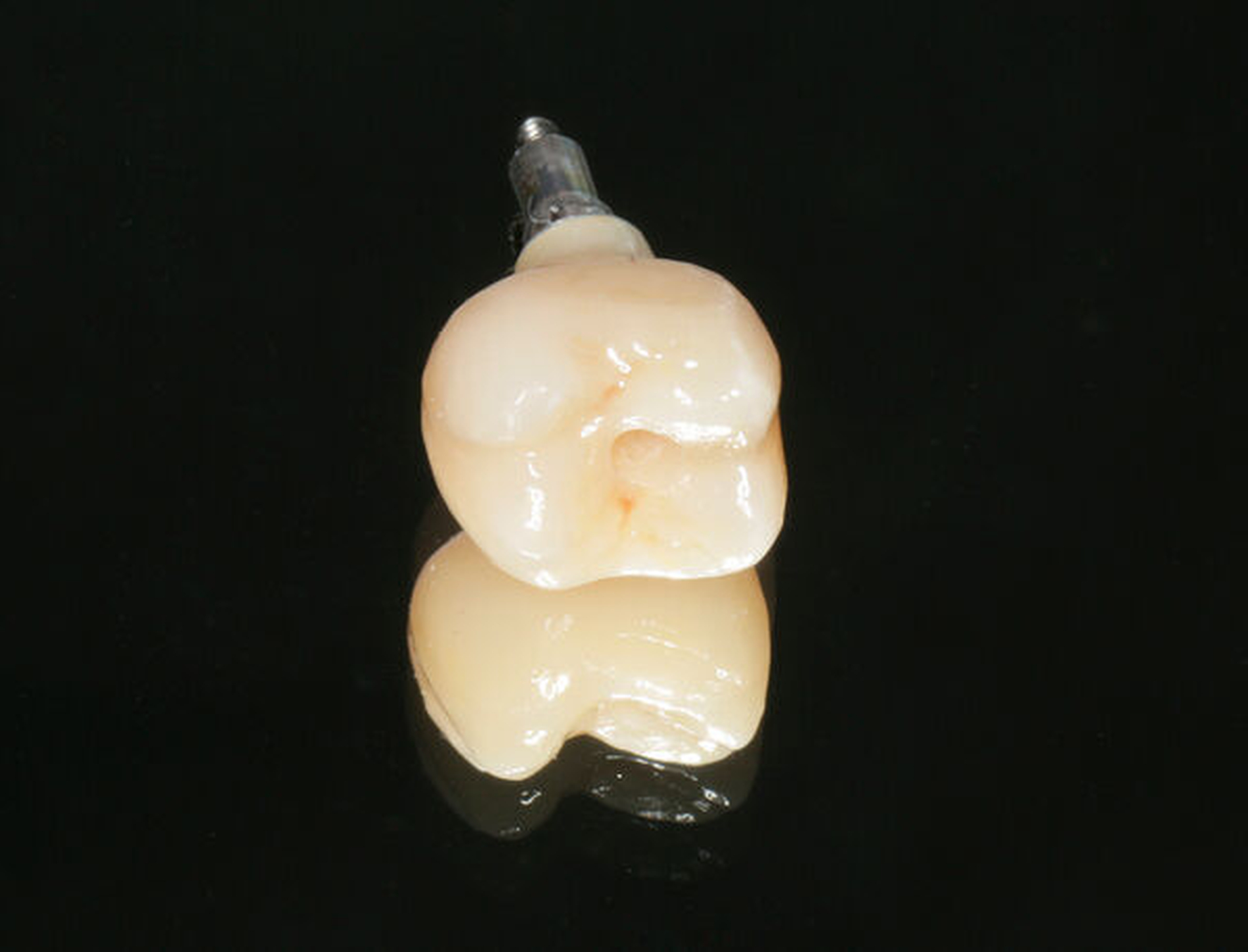
Im vorliegenden Patientenfall wurde sich bereits im Zuge der Implantatplanung (siehe auch den Abschnitt „Implantatpositionierung“) für eine transokklusal verschraubte Krone entschieden. Die Implantatkrone wurde im Hybridverfahren aus Lithiumdisilikat und der zugehörigen Titanklebebasis gefertigt (Abbildung 7). Entsprechend der Vorgabe des Implantatherstellers wurde die Krone mit einem Drehmoment von 20 Ncm eingeschraubt. Zu beachten ist, dass das Drehmoment sich zwischen den Herstellern und Implantattypen, aber auch den verwendeten Materialien des Dentallabors unterscheiden kann. Der transokklusale Schraubenkanal wurde abschließend mit Teflonband und Komposit verschlossen (Abbildungen 8 und 9). Bei auf Implantatabutments zementierten Kronen kann der Hohlraum zwischen der provisorischen Abdeckung des Schraubenkopfes und der definitiven Krone auch als Abflussreservoir für den Befestigungszement dienen. Hier entfällt der okklusale Verschluss mit Komposit.
Zum Schutz der runden Schraubenköpfe und ihrer je nach Implantatsystem variierenden Profile können auch andere Materialien wie Schaumstoff- oder Wattepellets und provisorische Verschlussmassen wie Cavit (3M Deutschland GmbH) verwendet werden. Teflonband hat sich aufgrund seiner einfachen Kondensation und Entfernung klinisch bewährt. Unabhängig davon ist der möglichst speicheldichte Verschluss der letzten 1 bis 2 mm der Zugangskavität bei einer transokklusal verschraubten Krone wichtiger. Dieser kann mit den modernen Kompositen gut gewährleistet werden.
Um Suprakontakte und Dysbalancen zu vermeiden, sollten die Kontakte sowohl mit Okklusions- als auch mit Shimstock-Folie kontrolliert werden. Gleiches gilt für das Einstellen der Approximalkontakte, um einen spannungsfreien Sitz zu gewährleisten. Bei starkem Einschleifen kann es gegebenenfalls notwendig sein, die Restauration im Labor erneut polieren zu lassen, um raue Oberflächen zu vermeiden.
Weiterbehandlung und Nachsorge
Nach Eingliederung der prothetischen Versorgung sollte die Unterweisung des Patienten hinsichtlich der implantatspezifischen Hygiene erfolgen. Dazu gehört auch die Aufklärung über Hilfsmittel für die häusliche Hygiene wie zu verwendende Zahnbürsten, Zahnseide (beispielsweise Superfloss) und Interdentalbürstchen. Vor allem der Bereich des Implantatdurchtritts stellt dabei eine kritische Stelle dar. Denn der im Vergleich zur natürlichen Zahnwurzel reduzierte Implantatdurchmesser kann eine suffiziente Plaquekontrolle für den Patienten erschweren. Deswegen sollte unabhängig vom individuellen Risikoprofil auch bei der Einzelzahnrestauration eine erste Kontrolle innerhalb des ersten Monats nach Eingliederung der Suprakonstruktion erfolgen. Dabei kann die Hygienefähigkeit sowohl der Restauration als auch des Patienten kontrolliert und gegebenenfalls angepasst werden. Des Weiteren sollte nach eventuellen Lockerungen oder Okklusionsstörungen gesehen werden. Suprakontakte und eine daraus resultierende Überbelastung sind dringend zu vermeiden.
Das Recallintervall sollte entsprechend des individuellen Risikoprofils ausgewählt werden. Dieses Vorgehen ist bereits aus der parodontalen Nachsorge bekannt. Je nach klinischem Befund erfolgen die Nachkontrollen eng- oder weitmaschiger. Im klinischen Alltag hat sich zunächst ein dreimonatiger Recall nach der Versorgung bewährt. Lässt sich stets eine entzündungsfreie, gut gereinigte Situation um das Implantat feststellen, kann das Intervall vergrößert werden. Dieses sollte zwölf Monate jedoch nicht überschreiten.
Schlussfolgerungen
Bei Beachtung der diskutierten Arbeitsschritte und der möglichen Fehlerquellen kann die implantologische Versorgung der Einzelzahnlücke eine langfristig erfolgreiche Therapie darstellen, die für jeden implantologisch interessierten Zahnarzt umsetzbar ist. Dabei sollten die individuellen therapeutischen Grenzen stets bekannt sein. Die implantatprothetische Rehabilitation im Frontzahnbereich wird dabei häufig als „Königsdisziplin“ beschrieben. Auch diese ist jedoch unter Berücksichtigung aller Parameter hochästhetisch möglich (Abbildungen 10 bis 12).
Die rasante Entwicklung innerhalb der Zahnmedizin erfordert eine regelmäßige Fort- und Weiterbildung – auch im Bereich der dentalen Implantologie. Dabei sollte nie vergessen werden, dass dazu neben neuen digitalen Konzepten auch das Verhindern, das Erkennen und die Therapie möglicher Komplikationen gehören.
Literaturliste
Abduo, J. and M. Elseyoufi (2018). „Accuracy of Intraoral Scanners: A Systematic Review of Influencing Factors.“ Eur J Prosthodont Restor Dent 26(3): 101-121.
Beretta, M., P. P. Poli and C. Maiorana (2014). „Accuracy of computer-aided template-guided oral implant placement: a prospective clinical study.“ J Periodontal Implant Sci 44(4): 184-193.
Bornstein, M. M., W. C. Scarfe, V. M. Vaughn and R. Jacobs (2014). „Cone beam computed tomography in implant dentistry: a systematic review focusing on guidelines, indications, and radiation dose risks.“ Int J Oral Maxillofac Implants 29 Suppl: 55-77.
Branemark, P. I. (1983). „Osseointegration and its experimental background.“ J Prosthet Dent 50(3): 399-410.
Branemark, P. I., R. Adell, T. Albrektsson, U. Lekholm, S. Lundkvist and B. Rockler (1983). „Osseointegrated titanium fixtures in the treatment of edentulousness.“ Biomaterials 4(1): 25-28.
Bressan, E., G. Paniz, D. Lops, B. Corazza, E. Romeo and G. Favero (2011). „Influence of abutment material on the gingival color of implant-supported all-ceramic restorations: a prospective multicenter study.“ Clin Oral Implants Res 22(6): 631-637.
Cholmakow-Bodechtel, C., E. Füßl-Grünig, S. Geyer, K. Hertrampf, T. Hoffmann, B. Holtfreter, A. R. Jordan, T. Kocher, W. Micheelis, I. Nitschke, S. Noffz, L. Scharf, U. Schiffner, S. Schützhold, H. Stark and S. Zimmer (2016). Fünfte Deutsche Mundgesundsheitsstudie (DMS V). Köln, Institut der Deutschen Zahnärzte (IDZ), Deutscher Zahnärzte Verlag DÄV.
Gomez-Meda, R., J. Esquivel and M. B. Blatz (2021). „The esthetic biological contour concept for implant restoration emergence profile design.“ J Esthet Restor Dent 33(1): 173-184.
Guerrero, M. E., R. Jacobs, M. Loubele, F. Schutyser, P. Suetens and D. van Steenberghe (2006). „State-of-the-art on cone beam CT imaging for preoperative planning of implant placement.“ Clin Oral Investig 10(1): 1-7.
Harris, D., K. Horner, K. Grondahl, R. Jacobs, E. Helmrot, G. I. Benic, M. M. Bornstein, A. Dawood and M. Quirynen (2012). „E.A.O. guidelines for the use of diagnostic imaging in implant dentistry 2011. A consensus workshop organized by the European Association for Osseointegration at the Medical University of Warsaw.“ Clin Oral Implants Res 23(11): 1243-1253.
Jacobs, R. and M. Quirynen (2014). „Dental cone beam computed tomography: justification for use in planning oral implant placement.“ Periodontol 2000 66(1): 203-213.
Jacobs, R., B. Salmon, M. Codari, B. Hassan and M. M. Bornstein (2018). „Cone beam computed tomography in implant dentistry: recommendations for clinical use.“ BMC Oral Health 18(1): 88.
Linkevicius, T. (2017). „The Novel Design of Zirconium Oxide-Based Screw-Retained Restorations, Maximizing Exposure of Zirconia to Soft Peri-implant Tissues: Clinical Report After 3 Years of Follow-up.“ Int J Periodontics Restorative Dent 37(1): 41-47.
Linkevicius, T. and P. Apse (2008). „Influence of abutment material on stability of peri-implant tissues: a systematic review.“ Int J Oral Maxillofac Implants 23(3): 449-456.
Lops, D., E. Stellini, L. Sbricoli, N. Cea, E. Romeo and E. Bressan (2017). „Influence of abutment material on peri-implant soft tissues in anterior areas with thin gingival biotype: a multicentric prospective study.“ Clin Oral Implants Res 28(10): 1263-1268.
Marrone, A., J. Lasserre, P. Bercy and M. C. Brecx (2013). „Prevalence and risk factors for peri-implant disease in Belgian adults.“ Clin Oral Implants Res 24(8): 934-940.
Moraschini, V., L. A. Poubel, V. F. Ferreira and S. Barboza Edos (2015). „Evaluation of survival and success rates of dental implants reported in longitudinal studies with a follow-up period of at least 10 years: a systematic review.“ Int J Oral Maxillofac Surg 44(3): 377-388.
Nasseh, I. and W. Al-Rawi (2018). „Cone Beam Computed Tomography.“ Dent Clin North Am 62(3): 361-391.
Papaspyridakos, P., K. Vazouras, Y. W. Chen, E. Kotina, Z. Natto, K. Kang and K. Chochlidakis (2020). „Digital vs Conventional Implant Impressions: A Systematic Review and Meta-Analysis.“ J Prosthodont 29(8): 660-678.
Pellegrino, G., A. Ferri, M. Del Fabbro, C. Prati, M. G. Gandolfi and C. Marchetti (2021). „Dynamic Navigation in Implant Dentistry: A Systematic Review and Meta-analysis.“ Int J Oral Maxillofac Implants 36(5): e121-e140.
Pjetursson, B. E., U. Bragger, N. P. Lang and M. Zwahlen (2007). „Comparison of survival and complication rates of tooth-supported fixed dental prostheses (FDPs) and implant-supported FDPs and single crowns (SCs).“ Clin Oral Implants Res 18 Suppl 3: 97-113.
Pjetursson, B. E., D. Thoma, R. Jung, M. Zwahlen and A. Zembic (2012). „A systematic review of the survival and complication rates of implant-supported fixed dental prostheses (FDPs) after a mean observation period of at least 5 years.“ Clin Oral Implants Res 23 Suppl 6: 22-38.
Sailer, I., S. Muhlemann, M. Zwahlen, C. H. Hammerle and D. Schneider (2012). „Cemented and screw-retained implant reconstructions: a systematic review of the survival and complication rates.“ Clin Oral Implants Res 23 Suppl 6: 163-201.
Sailer, I., M. Strasding, N. A. Valente, M. Zwahlen, S. Liu and B. E. Pjetursson (2018). „A systematic review of the survival and complication rates of zirconia-ceramic and metal-ceramic multiple-unit fixed dental prostheses.“ Clin Oral Implants Res 29 Suppl 16: 184-198.
Tahmaseb, A., D. Wismeijer, W. Coucke and W. Derksen (2014). „Computer technology applications in surgical implant dentistry: a systematic review.“ Int J Oral Maxillofac Implants 29 Suppl: 25-42.
Tahmaseb, A., V. Wu, D. Wismeijer, W. Coucke and C. Evans (2018). „The accuracy of static computer-aided implant surgery: A systematic review and meta-analysis.“ Clin Oral Implants Res 29 Suppl 16: 416-435.
Wittneben, J. G., T. Joda, H. P. Weber and U. Bragger (2017). „Screw retained vs. cement retained implant-supported fixed dental prosthesis.“ Periodontol 2000 73(1): 141-151.