Ist die Parodontitis ein Risikofaktor für Krebs?
Intraorale Plattenepithelkarzinome (OSCC) repräsentieren 90 Prozent der malignen Tumore der Mundhöhle. Zurzeit stellt sich deren Ätiologie multifaktoriell dar. Vor allem Tabak- und Alkoholabusus spielen eine bedeutende Rolle. Allerdings werden vermehrt auch chronisch entzündliche Erkrankungen aufgrund mangelhafter Mundhygiene, wie sie bei den meisten Tumorpatienten festgestellt wurden, als karzinogene Prädisposition diskutiert.
Die Therapie von Plattenepithelkarzinomen beinhaltet hauptsächlich chirurgische Eingriffe. Trotz immer anspruchsvollerer chirurgischer Techniken hat sich die Patientenüberlebensrate innerhalb der vergangenen zwei Dekaden nicht sonderlich erhöht. Deshalb ist es ausgesprochen wichtig, ein besseres Verständnis der molekularen Mechanismen bei der Entstehung oraler Tumore zu erzielen.
Welche Mechanismen verursachen orale Tumore?
Dabei scheint der Faktor „chronische Entzündung“ sehr Erfolg versprechend hinsichtlich der Identifizierung onkogener Moleküle zu sein. Eine der in der Bevölkerung am weitesten verbreiteten chronisch entzündlichen Erkrankungen ist die chronische Parodontitis. Hierbei sind die Zellen der Mundhöhle einer erheblichen dauerhaften inflammatorischen Last ausgesetzt. Im Rahmen der Entstehung einer chronischen Parodontitis kommt es zu einer durch Bakterien hervorgerufenen Infektion. Dadurch wird das angeborene Abwehrsystem aktiviert, um gegen die Bakterienbesiedlung vorzugehen. Hierbei spielen sogenannte antimikrobielle Peptide eine große Rolle.
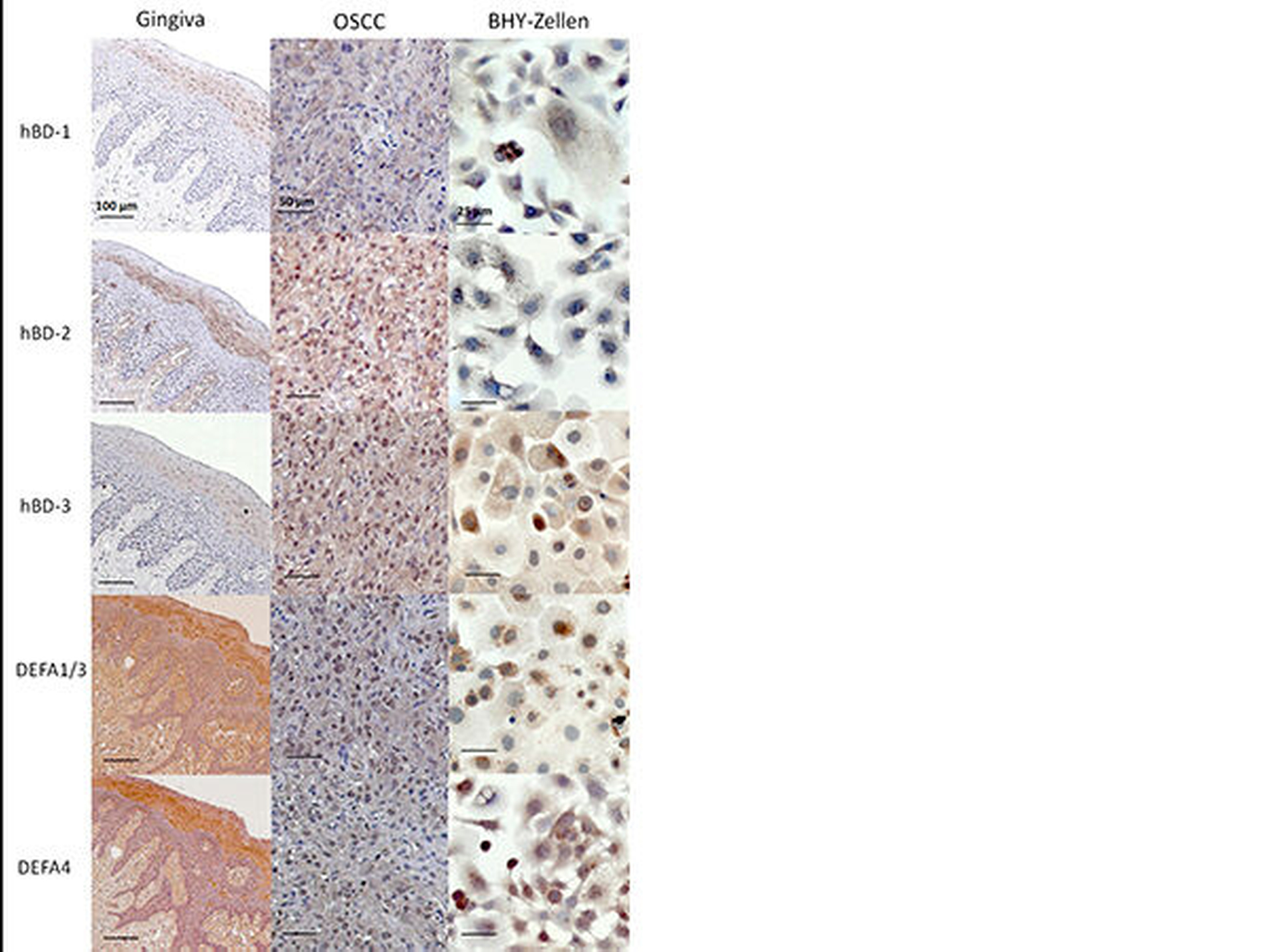
Zu dieser Gruppe gehören die humanen Defensine. Diese Moleküle werden hauptsächlich durch das Epithel der Mundhöhle sekretiert und wirken bakteriozid. Humane Defensine kommen in Epithelien unterschiedlicher Gewebe (Mundhöhle, Urogenitalsystem, Lunge, Darm, Haut) und im Speichel vor. Außerdem sind sie in oralen Läsionen (Reizfibrom, Leukoplakien, orale Plattenepithelkarzinome) gefunden worden.
Diese Beobachtungen haben die Frage aufgeworfen, ob Defensine noch andere physiologische Funktionen neben ihrer antimikrobiellen Wirkung haben könnten. In der Tat hat man Effekte auf Zellwachstumsebene finden können. So kommt es zu einer erhöhten Zellproliferation gingivaler Epithel- sowie oraler Plattenepithelkarzinomzellen, wenn sie mit humanen Defensinen stimuliert werden.
Wird die Molekülstruktur der Defensine analysiert, findet man eine große Ähnlichkeit mit dem epidermalen Wachstumsfaktor (EGF). Dieses Protein steuert das Wachstum von Zellen über die Bindung an seinen Rezeptor (EGFR). Dieser Rezeptor ist nun in der Tumorgenese von eminenter Bedeutung. Wird der EGF-Rezeptor dauerhaft stimuliert, kommt es zu einer ungeordneten Zellproliferation, die zur Entstehung von Tumoren führen kann. Können humane Defensine den EGF-Rezeptor aktivieren und darüber die Zellvermehrung beeinflussen? Um diese Frage zu klären, wurde die Aktivierung des EGF-Rezeptors bei oralen Plattenepithelkarzinomzellen nach Stimulation mit humanen Defensinen (DEFA1/3; DEFA4; hBD-1/-2/-3) analysiert. Alle Defensine waren in der Lage, den Rezeptor zu aktivieren und damit die Zellproliferationsrate zu steigern.
Die ambivalente Rolle der Defensine
Es kommt also zu einem Teufelskreis: Bakterien infizieren den Wirt. Dieser reagiert darauf mit der Sekretion antimikrobieller Peptide. Außerdem kommt es zu einer Inflammation, die ebenfalls zu einer vermehrten Produktion von Defensinen führt. Diese Moleküle wirken nun gegen die Bakterien, aber eben auch als Strukturanaloge des epidermalen Wachstumsfaktors (EGF), womit sie über die Bindung an dessen Rezeptor (EGFR) die Zellen zur vermehrten Proliferation anregen. Da sich die Tumorzellen selbst ebenfalls an der Wirtsabwehr beteiligen, synthetisieren sie selbst dauerhaft ihren eigenen Proliferationsstimulus.
Bei chronischer Entzündung lässt sich nun leicht erklären, welche Mechanismen zur Tumorgenese greifen, nämlich die permanente Aktivierung des EGF-Rezeptors durch die dauerhafte Sekretion von Defensinen. Somit könnte die Gruppe der Defensine einen molekularen Link auf der Achse „Infektion – Inflammation – Turmorgenese“ darstellen.
Bei logischer Betrachtung müsste es jetzt unweigerlich zu einer Krebserkrankung infolge einer Parodontitis kommen. Das ist offensichtlich nicht der Fall. Ein Grund dafür könnte eines der Defensine sein, das noch über eine weitere wichtige Funktion verfügt: Das humane β-Defensin-1 (hBD-1) wirkt zusätzlich als Tumorsuppressor.
Dadurch entfaltet es antiproliferative Effekte auf Zellen. Es ist also ein Antagonist bezüglich proliferativer Prozesse. Solange hBD-1 präsent ist, können sich die Zellen trotz Aktivierung über den EGF-Rezeptor nicht ungeordnet vermehren. Es ist also von eminenter Bedeutung, dass ein Gleichgewicht zwischen hBD-1 und den anderen Defensinen besteht, um eine Tumorinitiation zu verhindern.
Dr. rer. nat. Tatjana HoppeProf. Dr. Søren JepsenPD Dr. rer. nat. Dipl.-Biol. Jochen WinterPoliklinik für Parodontologie, Zahnerhaltung und Präventive ZahnheilkundeUniversität BonnWelschnonnenstr. 17, 53111 Bonnjochen.winter@ukbonn.de
Hoppe T, Kraus D, Novak N, Probstmeier R, Frentzen M, Wenghoefer M, Jepsen S, Winter J: Oral pathogens change proliferation properties of oral tumor cells by affecting gene expression of human defensins. Tumor Biology 2016 Aug 1. 37(10): 13789–13798.
Danksagung: Die vorliegende Arbeit wurde im Rahmen der Klinischen Forschergruppe 208 „Ursachen und Folgen von Parodontopathien – genetische, zellbiologische und biomechanische Aspekte“ mit Förderung durch die Deutsche Forschungsgemeinschaft (DFG) und die Medizinische Fakultät der Universität Bonn durchgeführt.