RCT-Studien sind ein Standard ohne Gold
Die Vorstellung ist faszinierend und die Welt der Forschung wäre gleichsam aufgeräumt und geordnet, wenn es zutreffen würde, was uns die Verfechter der Evidenzpyramide nun seit einigen Dekaden bereits versprechen: Es gibt den einen und besten Weg, um die unbestechliche Wahrheit zu jeder beliebigen Forschungsfrage herauszufinden. Eine Art Universalwerkzeug, mit dem die Wirkung oder Nichtwirkung einer medizinischen Intervention zweifelsfrei nachgewiesen werden kann. Der Glaube daran nimmt zeitweise recht fundamentalistische Züge an: So empfahlen Sackett et al. Mitte der Neunzigerjahre „Wenn Sie auf eine nichtrandomisierte Studie stoßen, sollten Sie besser gar nicht weiterlesen, sondern gleich zum nächsten Artikel weiterblättern“ [Sackett et al., 1996].
Diese Aussage beruhte noch auf der Annahme, eine RCT könnte systematische Fehler nicht nur begrenzen, sondern total beseitigen. Seither haben jedoch Wissenschaftler in allen medizinischen und zahnmedizinischen Disziplinen erkannt, dass dies nicht zutrifft. Nach der „neuen Lehre“ der evidenzbasierten Medizin können „RCTs systematische Fehler minimieren, aber nicht eliminieren“ [Sami/Sedwick, 2011]. Zudem können sie, wie Kaptchuk betont, „ihre eigenen Abweichungen von der Wahrheit einbringen“ [Kaptchuk, 2001]. Die Diskussionen der letzten 20 Jahre haben gezeigt, dass das RCT-Design zahlreiche Schwächen aufweist und nicht unerheblichen Limitierungen unterliegt – von ethischen Grenzen über praktisch undurchführbare Verblindungen bis hin zu spezifischen Verzerrungsrisiken. Würdigt man diese Tatsachen, wird aus dem Universalwerkzeug RCT ein ganz normales Instrument der Wissenschaft, das in einigen Bereichen seine Stärken ausspielen kann, in anderen aber schlicht unbrauchbar für die Forschung ist.
RCTs in der KFO
Um es gleich vorauszuschicken: Mir erscheinen RCTs nicht immer sinnvoll, jedenfalls nicht für zentrale klinische Fragen in der Kieferorthopädie. Meikle [Meikle, 2005] etwa resümierte, den Aussagegehalt von RCTs zur Behandlung von Klasse-II-Anomalien betreffend: „Wenn man fragt, ob RCTs ihr angestrebtes Ziel erreicht haben oder ob sie Erkenntnisse geliefert haben, die nicht bereits aus retrospektiven Studien oder Tierversuchen vorlagen, müsste die Antwort Nein lauten.“ Diese Aussage wiegt umso schwerer, wenn man bedenkt, dass zu keinem Thema der Kieferorthopädie mehr RCTs verfügbar sind als zu Klasse-II-Anomalien.
Zur Beantwortung der Frage, warum RCTs häufig an wesentlichen klinischen Fragestellungen der Kieferorthopädie scheitern, müssen wir uns ihren eigentlichen Zweck vor Augen führen: nämlich zu prüfen, ob eine Behandlung funktioniert, und zwar im Vergleich zu einem Kontrollzustand. Dieser kann in keiner, in einer alternativen oder in einer Placebo-Behandlung bestehen. Und da die Kieferorthopädie von Apparaturen bestimmt wird, liegt genau hier das Problem! Denn „kieferorthopädische Behandlungen gestalten sich nicht als sequenzielle Pilleneinnahme, die man randomisiert durchführen und verblindet auswerten könnte“ [Johnston, 2002]. Im Gegenteil: Selbst „unsichtbare“ Apparaturen sind für den Patienten sichtbar, jedenfalls aber wahrnehmbar. Also scheiden, wenigstens für die meisten Fragestellungen, Placebo-Behandlungen schon einmal aus.
Natürlich besteht immer die Alternative einer RCT mit einer unbehandelten Kontrollgruppe. Selbst wenn wir jedoch ethische Bedenken einmal ausklammern, wollen mir nur wenige klassische Fragestellungen der klinischen Kieferorthopädie einfallen, die ein solches Studienkonzept rechtfertigen würden. Dies umso mehr, wenn wir realistisch bleiben und nicht die jahrzehntelangen klinischen Erfahrungen ignorieren, über die wir in der Kieferorthopädie verfügen. Hierzu gehört, dass wir unbehandelte Kontrollgruppen nicht bedingungslos auch in lächerlichen Szenarien fordern, in denen eine klinisch relevante, stichhaltige Wahrheitsfindung auch ohne Kontrollgruppe gut möglich ist. Ein Beispiel dafür wäre die Aussage, dass sich starke Bissanomalien wie etwa eine Frontzahnstufe > 9 mm nicht von selbst korrigieren, dazu braucht es schlicht keine Beweisführung auf Evidenzstufe I.
Systematische Fehler von RCTs
Zusammenfassend sind also Vergleiche zwischen unterschiedlichen Behandlungsformen die einzige Forschungsmethode auf RCT-Niveau, die uns in der Kieferorthopädie bleibt. Solche RCTs sind zweifellos machbar, aber sind sie auch immer sinnvoll?
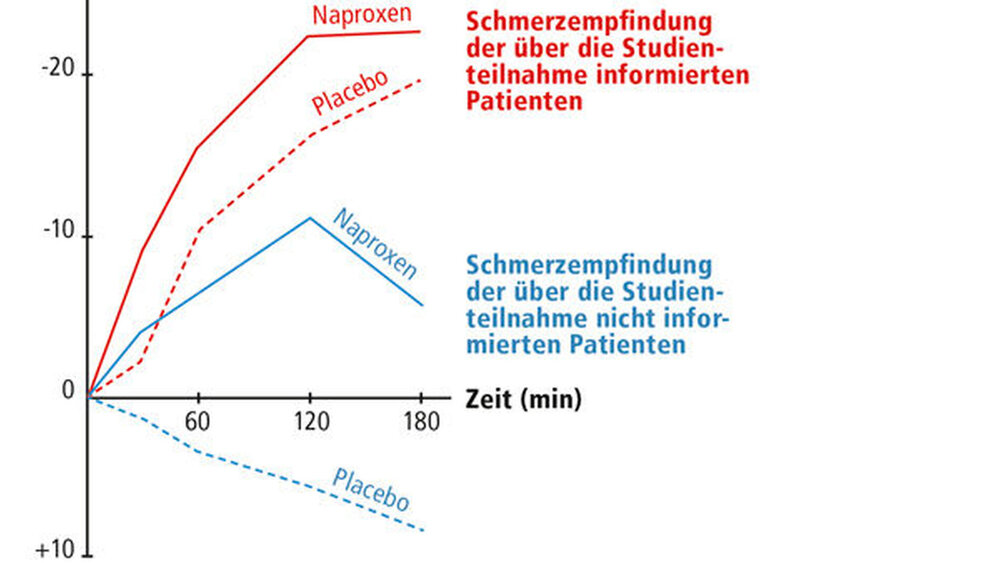
Der Erfolg kieferorthopädischer Behandlungen hängt immer in gewissem Maße von der Kooperation der Patienten ab, weshalb Verzerrungseffekte wie die „aktive Forschungsbeteiligung“ hier sehr stark zum Tragen kommen. Schon die Tatsache, dass von jedem RCT-Teilnehmer eine Einwilligungserklärung nach erfolgter Aufklärung obligatorisch ist (also die Forderung nach informed consent oder informierter Einwilligung), kann das Ansprechen auf die Therapie in einem klinisch möglicherweise höchst relevanten Maß beeinflussen. Bergmann et al. [Bergmann et al., 1994] starteten 1994, kurz vor Inkrafttreten dieser Aufklärungspflicht in Frankreich, eine RCT zum Einfluss der informierten Einwilligung auf die Wirkung von Analgetika. 49 konsekutiv hospitalisierte Patienten mit leichten bis mittelstarken Tumorschmerzen wurden nach dem Zufallsprinzip über ihre Teilnahme an der RCT entweder informiert oder nicht informiert. Im zweiten Schritt erfolgte, wieder per Los, die Zuteilung aller Patienten zu den Behandlungsgruppen Analgetikum (Naproxen) oder Placebo. Die Resultate (Abbildung 1) zur Schmerzlinderung erbrachten in der nicht informierten Normalfallgruppe erwartungsgemäß eine Wirkung des Analgetikums, nicht aber des Placebo. Mit dem Umstand der Aufklärung veränderte sich dieses Bild massiv: Das Placebo wie auch das Analgetikum reduzierten die Tumorschmerzen unter den informierten Patienten signifikant stärker und nachhaltiger als unter den normalen klinischen Bedingungen.
Auch kieferorthopädische Studien unterliegen der Aufklärungspflicht und lassen sich zudem, wie bereits erwähnt, meist weder einfach noch doppelt verblinden. Die daraus resultierenden Einstellungs- und Verhaltensanpassungen bei Patienten und Behandlern beeinflussen auch die Resultate in der Kieferorthopädie in klinisch signifikanter Weise. Ein sehr gutes Beispiel für diesen Zusammenhang ist die RCT von Sandler et al. [Sandler et al., 2008] unter Beteiligung von 51 randomisierten Patienten, die zur stärkeren Verankerung einer festsitzenden Apparatur entweder einen kooperationsabhängigen Headgear trugen oder mit einem kooperationsunabhängigen Gaumenimplantat zur Verankerung versorgt wurden. Die prätherapeutischen PAR-Werte (Schweregrad der Fehlstellungen) waren in beiden Gruppen vergleichbar, die PAR-Rückgänge im Behandlungsverlauf ebenfalls. Headgear und Implantat waren somit gleich wirksam. Auch bestand kein Gruppenunterschied bei der Behandlungsdauer, das heißt, beide Varianten waren auch gleich effizient. Aber ist dies tatsächlich die Wahrheit? Nun, es ist eine Wahrheit, allerdings nicht die klinische, sondern das Abbild einer von der Studie selbst beeinflussten Realität. Sandler et al. geben nämlich zu bedenken, dass „die Headgear-Patienten die Behandler mit der Geschwindigkeit und Effizienz der Methode überraschten […] die Kooperation übertraf das normal zu erwartende Maß […] vermutlich waren wir Zeuge des Hawthorne-Effekts!“ [Sandler et al., 2008].
Der Hawthorne-Effekt ist ein Phänomen, bei dem unter Beobachtung stehende Menschen im Wissen um diese Tatsache ihr Verhalten verbessern oder ändern [McCarney et al., 2007]. Wir müssen uns bewusst sein, dass kieferorthopädische RCTs extrem anfällig für Hawthorne-Effekte sind, da bei all diesen Behandlungen der Erfolg in einem gewissen Maß von der Kooperation des Patienten abhängt. Verändert das Bewusstsein um eine Studienteilnahme die Kooperation, lassen sich demnach alle kooperationsabhängigen Therapieformen durch ein RCT-Konzept nicht zuverlässig prüfen – jedenfalls nicht auf klinisch relevante Wahrheiten. Und dies erklärt vielleicht, wie Meikle 2005 festhielt, „warum RCTs in der Kieferorthopädie ihr beabsichtigtes Ziel verfehlt haben“ [Meikle, 2005].
Alternativen zu RCTs
Wir müssen also akzeptieren, dass für viele kieferorthopädische Fragestellungen keine, oder wenigstens keine vernünftige, Möglichkeit zur Durchführung einer RCT besteht, weil dies mit zu großen Schwierigkeiten verbunden wäre [Cunningham et al., 2011]:
hohe Kosten
ethische Probleme
Aufklärungspflicht, elterliche Einwilligung
Probleme durch systematische Fehler
Behandlungspräferenzen von Behandlern/Patienten
Rekrutieren ausreichend vieler Patienten (oft wird das Angebot teilnahmewilliger Patienten überschätzt)
Die genannten Argumente führen klarerweise zur Frage, wie es nun weitergehen soll vor dem Hintergrund, dass „der verbreitete Glaube, nur RCTs könnten vertrauenswürdige Resultate liefern und Beobachtungsstudien wären irreführend, der Patientenversorgung wie auch der klinischen Forschung und der Ausbildung von Gesundheitsdienstleistern einen schlechten Dienst“ erweist [Concato et al., 2000].
Gibt es Alternativen?
Wenn wir vor unserem geistigen Auge die Evidenzleiter hinuntersteigen, wären Kohortenstudien – also nichtrandomisierte prospektive Studien – die nächste Überlegung. Der einzige nennenswerte Unterschied zu RCTs besteht jedoch in der nicht zufälligen Gruppenzuteilung, so dass im Hinblick auf kieferorthopädische Fragestellungen die meisten bereits erörterten Nachteile von RCTs auch für Kohortenstudien gelten. Folglich müssen wir uns noch eine Stufe tiefer auf die Ebene der Fallkontrollstudien und retrospektiven Studien begeben. Ich persönlich bin voll und ganz der Meinung von Johnston [Johnston, 2002], dass uns „in der Kieferorthopädie nur der Blick zurück nach vorne führt“. Diese Aussage zielt nicht auf eine Rückkehr zu früheren Praktiken, sondern auf eine Verbesserung der Qualität von retrospektiven klinischen Studien: „Aus heutiger Sicht ist die drängendste klinische Frage das Erkennen und, im Rahmen des Möglichen, Eliminieren diverser systematischer Fehler im Gepäck der durchschnittlichen retrospektiven Studie“ [Johnston, 2002].
Ein Vergleich zwischen RCTs, Querschnitt-, Kohorten- und Fallkontrollstudien macht deutlich, dass die drei letzteren Beobachtungsstudien in puncto äußere Validität potenziell besser abschneiden als die RCTs. Anders formuliert lassen sich die gewonnenen Daten besser auf die Allgemeinbevölkerung übertragen, was natürlich wünschenswert ist. Andererseits haben sie den Nachteil einer schlechteren inneren Validität, da es sehr viel schwieriger ist, systematische Fehler und konfundierende Faktoren diverser Art zu beseitigen oder einzudämmen [Carlson/Morrison, 2009].
Wie also können wir retrospektive Studien verbessern? Statt Millionen von Euro ausschließlich für RCTs auszugeben, könnten wir alternativ oder ergänzend in eine Art internationales KFO-Register investieren, wo kieferorthopädische Fälle von Dysgnathien mit eindeutig definierten Merkmalen verpflichtend einzutragen wären. Natürlich sind auch solche Registerstudien nicht frei von systematischen Fehlern, sie bieten jedoch als Primärquelle für populationsbasierte Fallkontrollstudien eine Reihe von Vorteilen [Carlson/Morrison, 2009]:
große Stichproben
systematisch gesammelte Daten
eine wesentlich raschere Durchführung von Studien
relativ geringe Kosten
Studien zu seltenen Effekten und Erkrankungen
informierte Einwilligung nicht mehr erforderlich
eine wesentlich einfachere Auswertung von Langzeiteffekten
Resümierend lässt sich also festhalten, dass „individuelle wie kollektive Experimente, Beobachtungen und Berechnungen jeweils maßgeblich zur Evidenzbasis für eine moderne Therapeutik beitragen. Kontroversen zur relativen Bedeutung der einzelnen Studienkonzepte lenken nur unnötig ab. An die Stelle von Evidenzhierarchien sollte die Akzeptanz – ja das bereitwillige Aufgreifen – einer Vielfalt von Ansätzen treten“ [Rawlins, 2008]. Mit einer solchen Entwicklung verbunden wäre dann auch die Hoffnung auf ein Ende der nun schon viel zu lange geführten, ideologisch aufgeladenen Debatten über das Für und Wider evidenzbasierter Glaubensgegenstände. Mit den zweifellos vorhandenen Verdiensten der EbM, aber ohne den Bias des messianischen Eifers, wird die Wissenschaft besser vorankommen.
Prof. Dr. Sabine Ruf
Direktorin der Poliklinik für Kieferorthopädie
Zentrum für Zahn-, Mund- und Kieferheilkunde
Justus-Liebig-Universität Gießen
Schlangenzahl 1435392 Gießen
Leicht gekürzter Nachdruck aus ZAHNMEDIZIN UND GESELLSCHAFT, Heft 2017–1, Hrsg. von der Interessengemeinschaft Zahnärztlicher Verbände in Deutschland e.V. (IGZ) Originalartikel frei zugänglich unter www.i-g-z.de
Literatur:
[Bergmann et al.; 1994]:
Bergmann, J.F., et al.et al. (1994) A randomised clinical trial of the eff ect of informed consent on the analgesic activity of placebo and naproxen in cancer pain. Clinical Trials and Metaanalysis, 29, 41-47.
[Carlson M. D., Morrison R. S.; 2009]:
Concato, J., Shah, N. and Horwitz, R.I. (2000) Randomized, controlled trials, observational studies, and the hierarchy of research designs. The New England Journal of Medicine, 342, 1887-1892.
[Concato et al.; 2000]:
Concato, J., Shah, N. and Horwitz, R.I. (2000) Randomized, controlled trials, observational studies, and the hierarchy of research designs. The New England Journal of Medicine, 342, 1887-1892.
[Cunningham et al.; 2011]:
Cunningham, S., et al.et al. (2011) In search of the sample: recent experiences of a trial team in orthodontics. Contemporary Clinical Trials, 32, 530-534.
[Johnston; 2002]:
Johnston, L.E., Jr. (2002) Moving forward by looking back: ‚retrospective‘ clinical studies. Journal of Orthodontics, 29, 221-226.
[Kaptchuk; 2001]:
Kaptchuk, T.J. (2001) The double-blind, randomized, placebo-controlled trial: gold standard or golden calf? Journal of Clinical Epidemiology, 54, 541-549.
[McCarney et al.; 2007]:
McCarney, R., Warner, J., Iliffe, S., van Haselen, R., Griffin, M. and Fisher, P. (2007) The Hawthorne effect: a randomised, controlled trial. BMC Medical Research Methodology, 7, 30.
[Meikle, 2005]:
Meikle, M.C. (2005) Guest editorial: what do prospective randomized clinical trials tell us about the treatment of class II malocclusions? A personal viewpoint. European Journal of Orthodontics, 27, 105-114.
[Rawlins; 2008]:
Rawlins, M. (2008) De testimonio: on the evidence for decisions about the use of therapeutic interventions. Lancet, 372, 2152-2161.
[Sackett et al.; 1996]:
Sackett, D.W., Richardson, W., Rosenberg, W. and Haynes, R.B. (1996) Evidence Based Medicine. Churchill-Livingstone, London, p. 108.
[Sami, T., Sedwick, P.; 2011]:
Sami, T. and Sedwick, P. (2011) Do RCTS provide better evidence than observational studies? Opticon1826, 11, 1-10.
[Sandler et al.; 2008]:
Sandler, J., et al.et al. (2008) Palatal implants are a good alternative to headgear: a randomized trial. American Journal of Orthodontics and Dentofacial Orthopedics, 133, 51-57.