Arthroskopische Eingriffe zur CMD-Behandlung
CMD ist durch Schmerzen und/oder eine Dysfunktion im Bereich des Kausystems gekennzeichnet; gemäß Definition der Deutschen Gesellschaft für Funktionsdiagnostik und -therapie (DGFDT) typischerweise als Kaumuskelschmerz, Kiefergelenkschmerz und/oder (para-)funktionell bedingter Zahnschmerz. Dysfunktionen können sich als Bewegungseinschränkung, intraartikuläre Störungen oder okklusale Interferenzen äußern [Hugger et al., 2016]. Darüber hinaus können sekundäre Begleitbeschwerden wie Kopf- oder Nackenschmerzen auftreten, die den Leidensdruck der Betroffenen zusätzlich erhöhen.
Die Prävalenz der CMD liegt bei circa 34 Prozent weltweit [Zieliński et al., 2024]. Die Pathogenese ist komplex und bis heute nicht vollständig verstanden. Man geht davon aus, dass die genetische Disposition, auslösende Faktoren sowie unterhaltende Einflüsse zusammenwirken [Schindler, 2017]. In der klinischen Praxis ist es häufig schwer, eindeutige Auslöser zu identifizieren. Ähnliche klinische und radiologische Befunde können mit sehr unterschiedlichen Symptomen und unterschiedlichem subjektivem Leidensdruck auftreten.
Während die Symptome oft nur leicht ausgeprägt sind und/oder spontan abklingen, erfordern andere Verläufe eine weiterführende Therapie. Eine strukturierte und interdisziplinär abgestimmte Diagnostik ist dafür die Grundlage. Die kürzlich entwickelte Diagnoseklassifikation des craniomandibulären Systems (DC-CMS) ermöglicht eine differenzierte Einteilung der CMD in myogene, arthrogene und/oder okklusogene Formen. Außerdem werden relevante Komorbiditäten erfasst. Damit stellt dies eine weiterentwickelte Systematik gegenüber der klassischen DC/TMD-Klassifikation dar [Weber et al., 2025a; Weber et al., 2025b].
Konservative Behandlungen kommen an ihre Grenzen
Die Behandlung der CMD erfolgt meist interdisziplinär und orientiert sich an der jeweiligen Leitkomponente der Beschwerden. Bei den meisten Patienten ist eine Schienentherapie (zum Beispiel mit adjustierter Aufbissschiene) die Basis der Behandlung. Zudem profitieren viele Betroffene von einer Physiotherapie sowie einer Verhaltensmodifikation. Während sich bei (vorwiegend) myogener Leitkomponente häufig eine Besserung durch konservative Maßnahmen zeigt, kann bei arthrogener Symptomatik der Einsatz minimalinvasiver operativer Verfahren hilfreich sein.
Verschiedene arthroskopisch gestützte Interventionen ergänzen die konservativen Therapieansätze. Diese ermöglichen eine direkte Behandlung intraartikulärer Pathologien [Al-Moraissi et al., 2020a]. Als Option bei therapieresistenten myogenen Beschwerden, aber auch als begleitende/vorbereitende Maßnahme vor chirurgischen Eingriffen kann sich die Injektion von Botulinumtoxin als wirksame Behandlung erweisen [Angelo et al., 2023].
Es gibt aktuell keine einheitliche Empfehlung, zu welchem Zeitpunkt eine (minimalinvasive) chirurgische Intervention erfolgen sollte. Die Leitlinie der Deutschen Gesellschaft für Mund-, Kiefer- und Gesichtschirurgie (DGMKG) zu inflammatorischen Kiefergelenkserkrankungen betont, dass eine Spülung des Gelenks (Lavage) zur Schmerzreduktion und zur Verbesserung der Beweglichkeit beitragen kann, wenn konservative Therapien ausgeschöpft sind [Neff et al., 2021]. Auch die DGFDT weist darauf hin, dass eine frühzeitige Anwendung minimalinvasiver Verfahren sinnvoll sein kann, falls konservative Maßnahmen nicht erfolgreich sind [DGFDT, 2022]. Neuere Metaanalysen empfehlen sogar, diese Verfahren bereits früh ins Behandlungskonzept zu integrieren [Al-Moraissi et al., 2020b].
Experten weisen darauf hin, dass minimalinvasive Verfahren neben den frühen Stadien der CMD auch bei fortgeschrittener Arthrose eingesetzt werden können. Dadurch lässt sich in vielen Fällen eine Verbesserung der Mundöffnung sowie eine Schmerzreduktion erreichen. Aufwendige offene chirurgische Operationen können gegebenenfalls herausgezögert oder sogar verhindert werden [Monje Gil et al., 2024].
Arthroskopisch gestützte Interventionen
Die Arthroskopie des Kiefergelenks ist ein minimalinvasives Verfahren zur Inspektion und Behandlung. Die erste Kiefergelenksarthroskopie wurde 1975 in Japan durch Onishi durchgeführt. In den 1980er-Jahren ist diese dann unter anderem durch McCain in den USA weiterentwickelt worden [McCain, 1988]. In vielen Ländern ist die arthroskopische Therapie des Kiefergelenks fest etabliert. In Deutschland scheint diese jedoch einen eher geringen Stellenwert zu haben, wobei systematische Vergleichsdaten bislang nicht vorliegen.
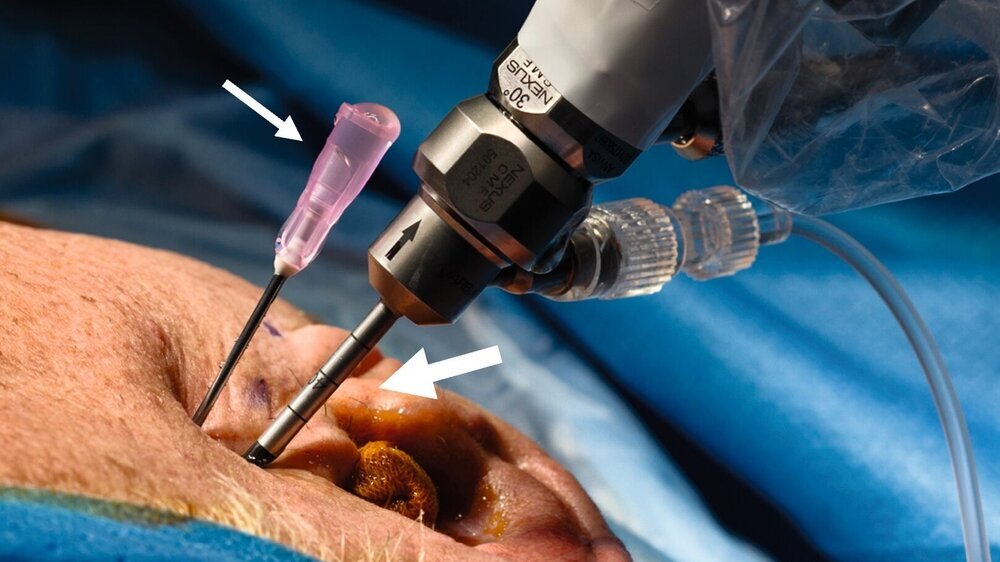
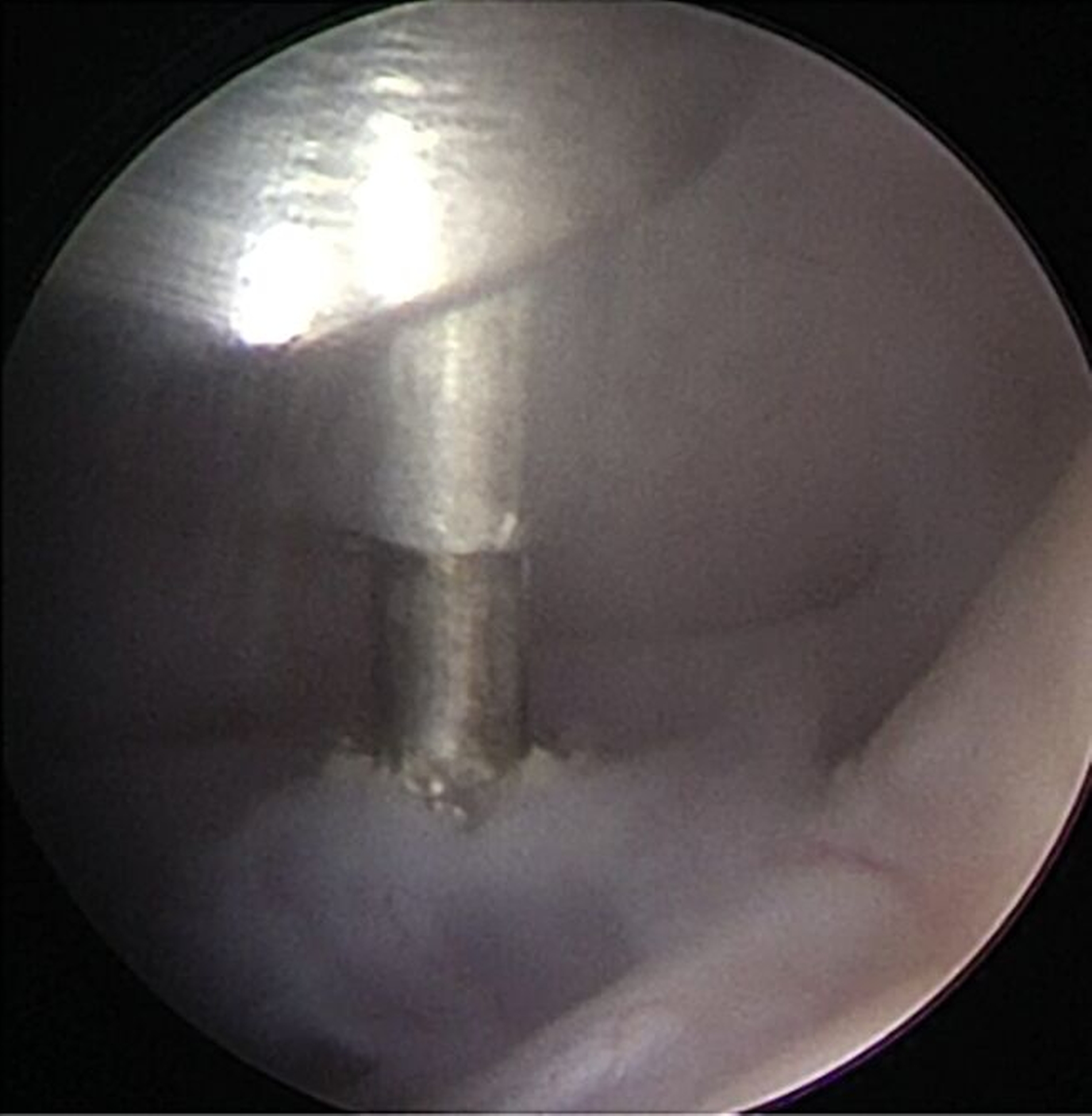
Man unterscheidet drei Formen der Arthroskopie (Level I–III) in Abhängigkeit von der Anzahl der verwendeten Arbeitskanäle. Bei der Level-I-Arthroskopie steht die erweiterte Diagnostik im Vordergrund. Dabei wird das Arthroskop mithilfe eines Trokars im Bereich des höchsten Punkts der Fossa mandibularis in den oberen Gelenkspalt eingebracht. Eine separate Spülkanüle ermöglicht die kontinuierliche Gelenkspülung (Abbildung 1). Die Operation findet in der Regel in ambulanter Vollnarkose statt. Eine Erweiterung auf Level II oder Level III, also die Einführung weiterer Arbeitskanäle, ist während der Operation möglich, sofern dies aufgrund des Befunds indiziert ist.
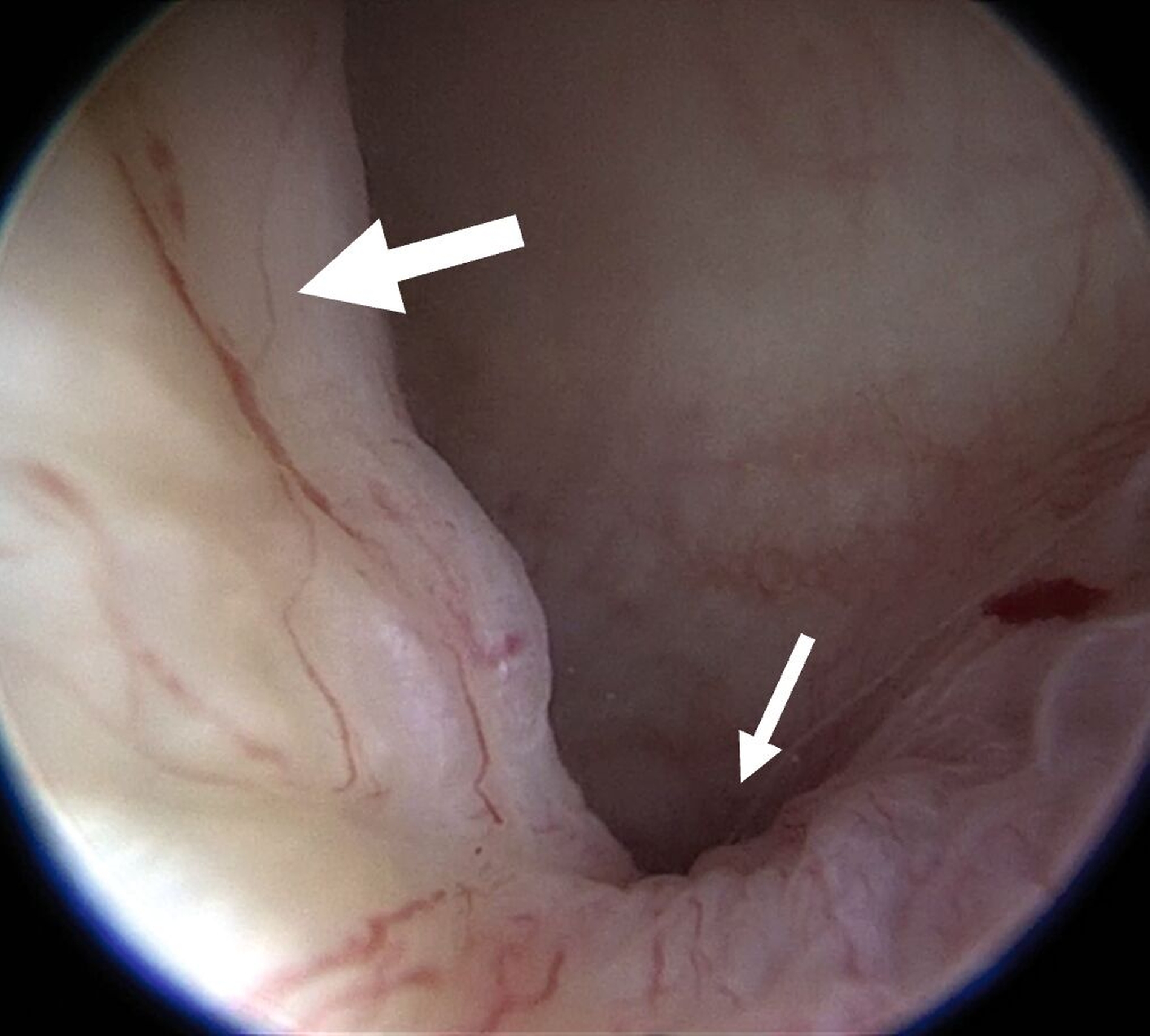
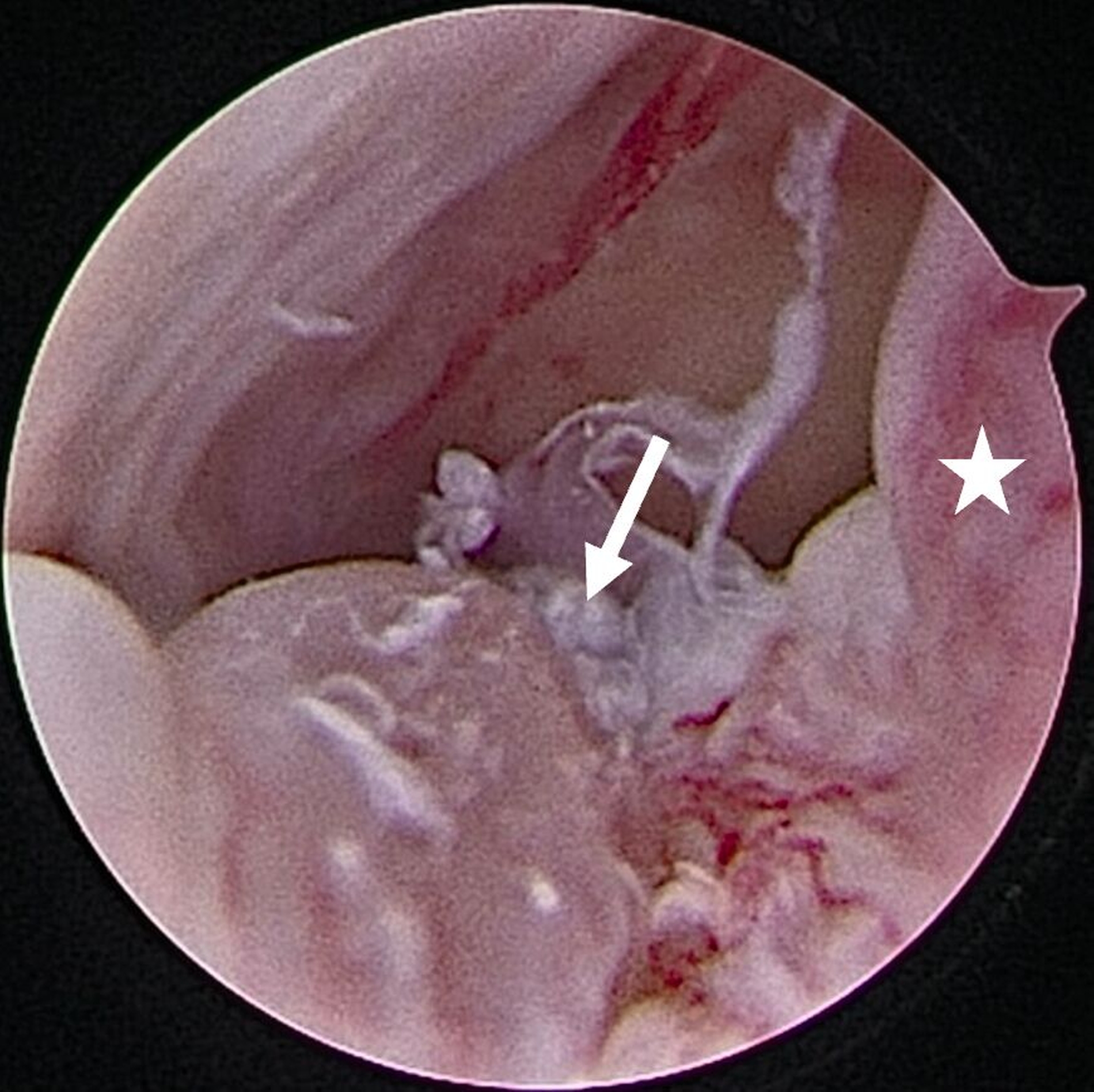
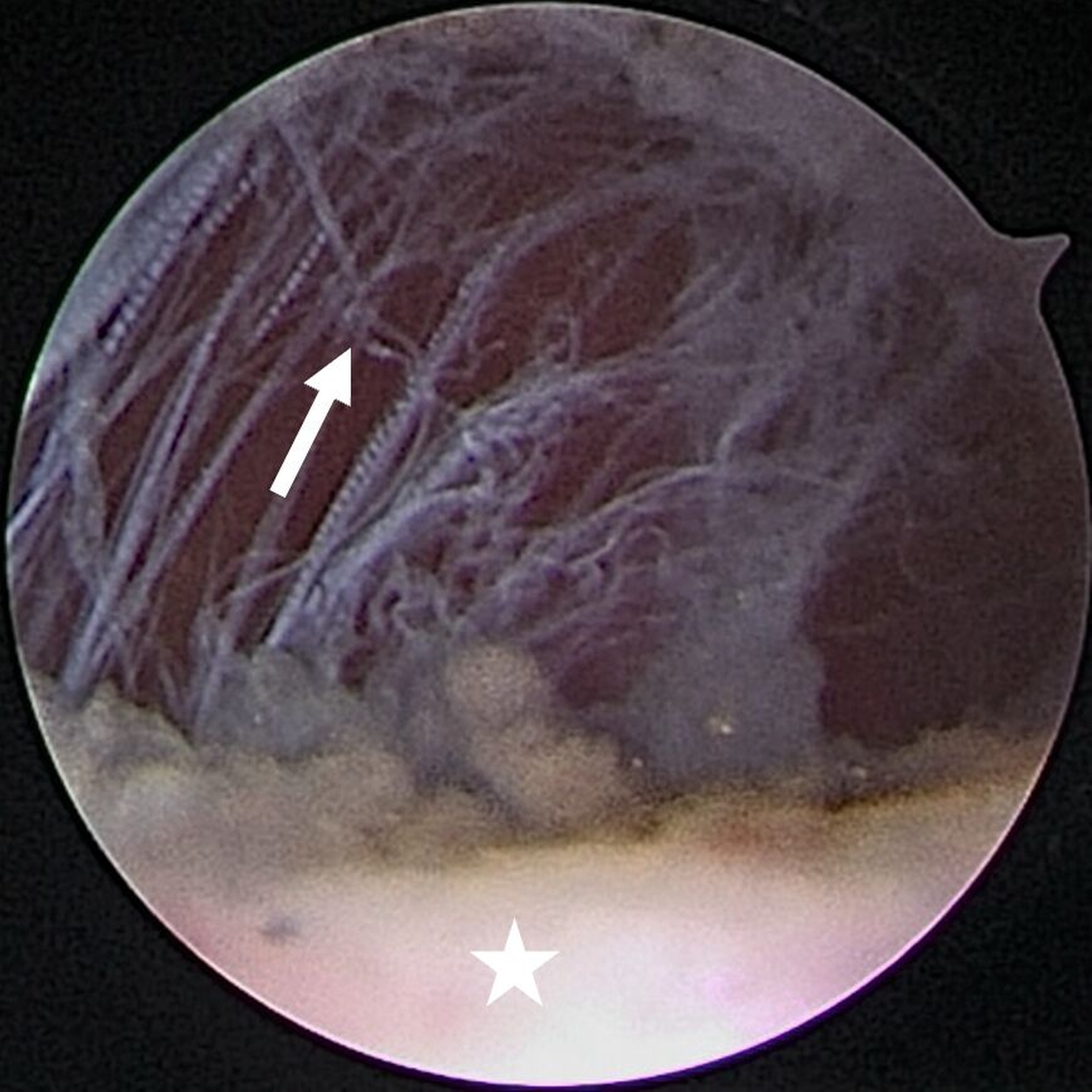
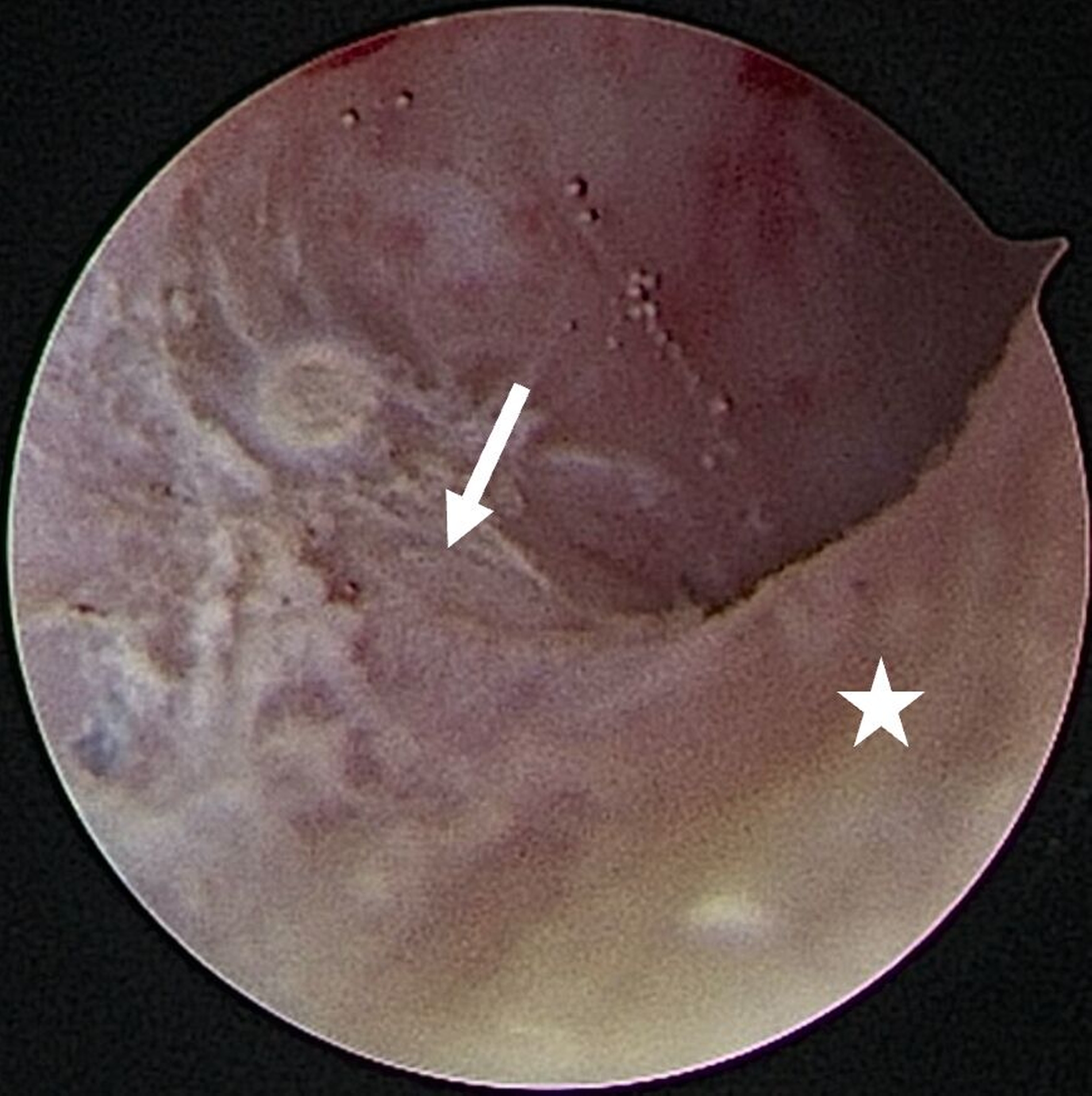
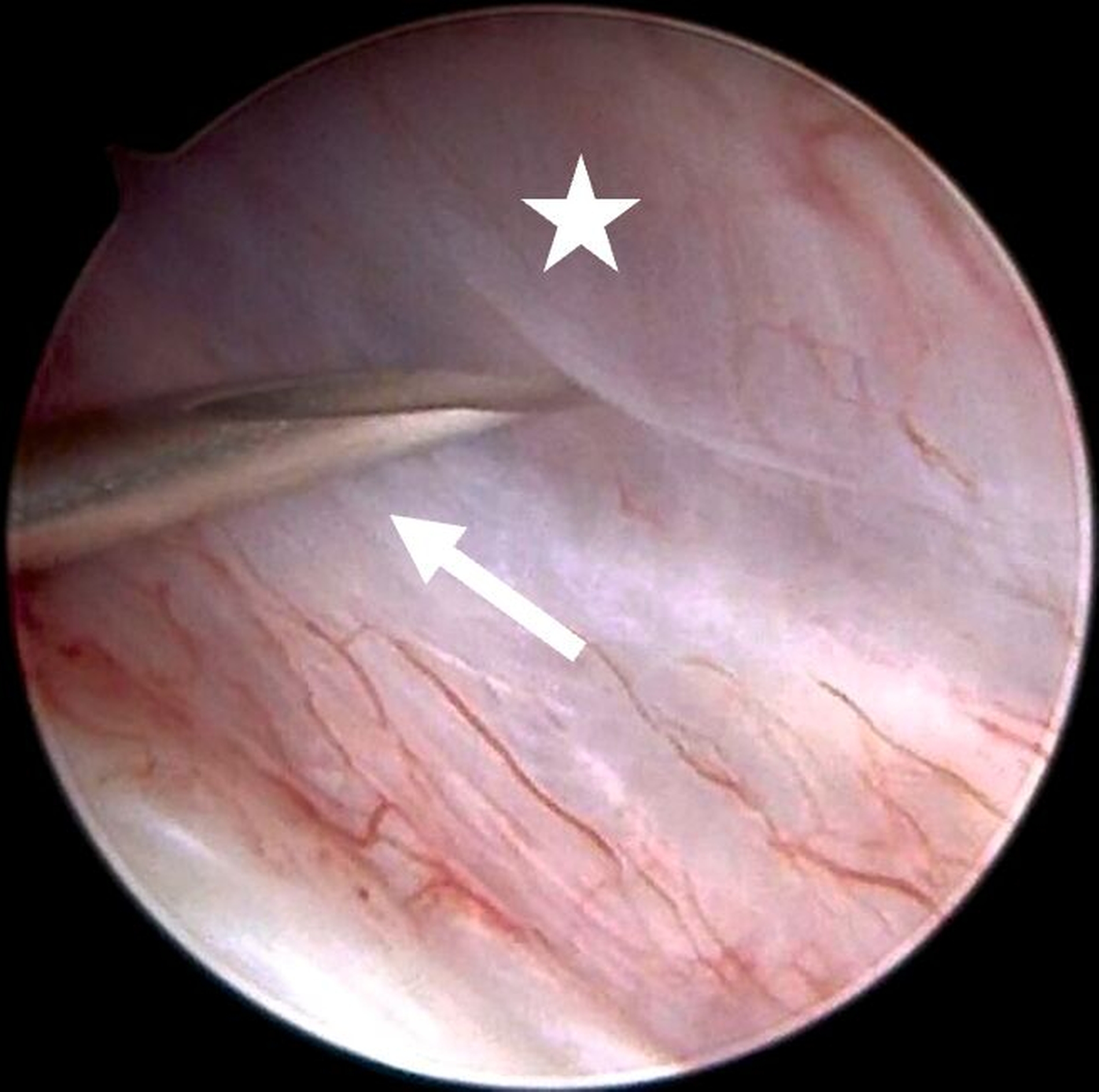
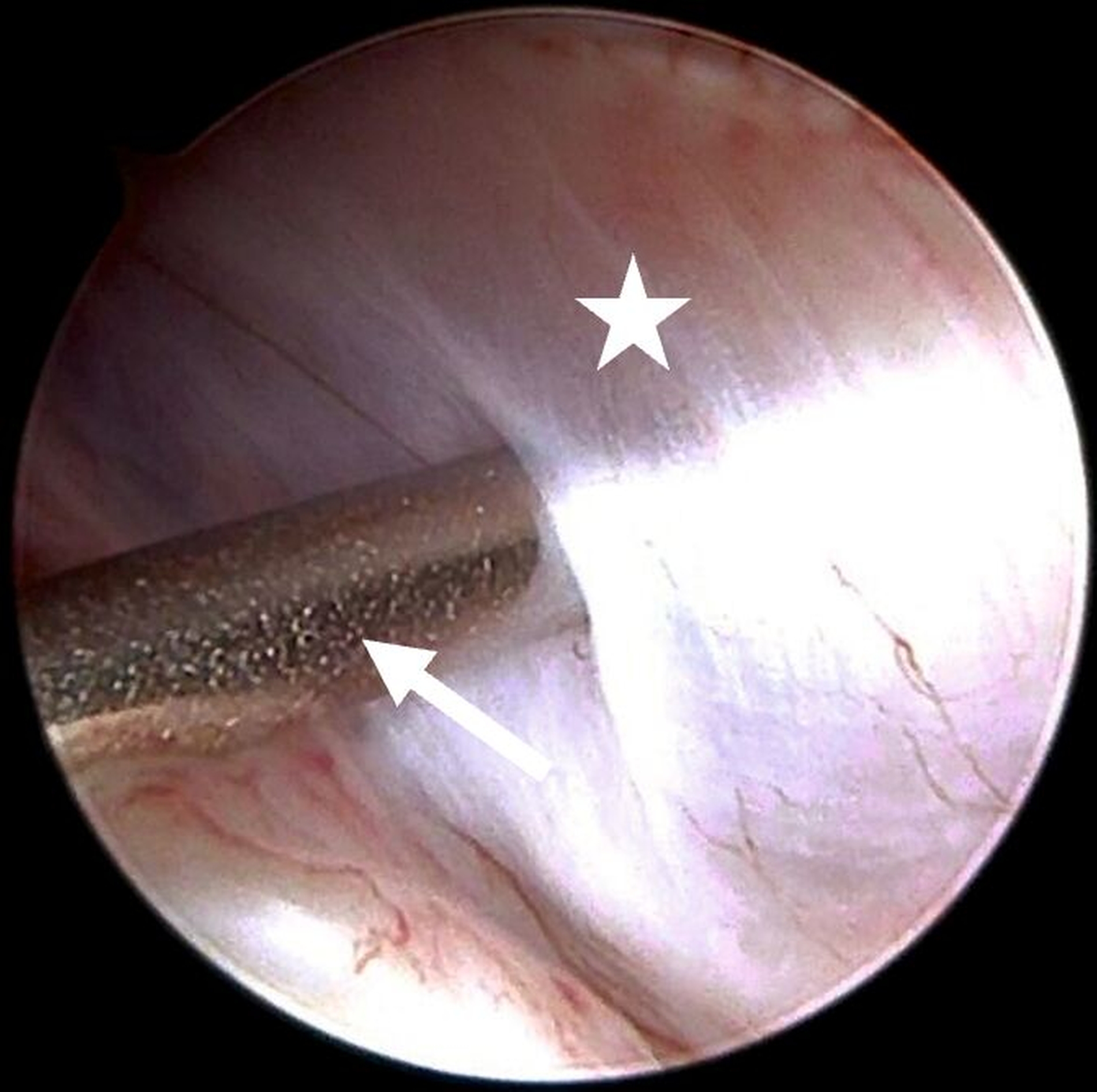
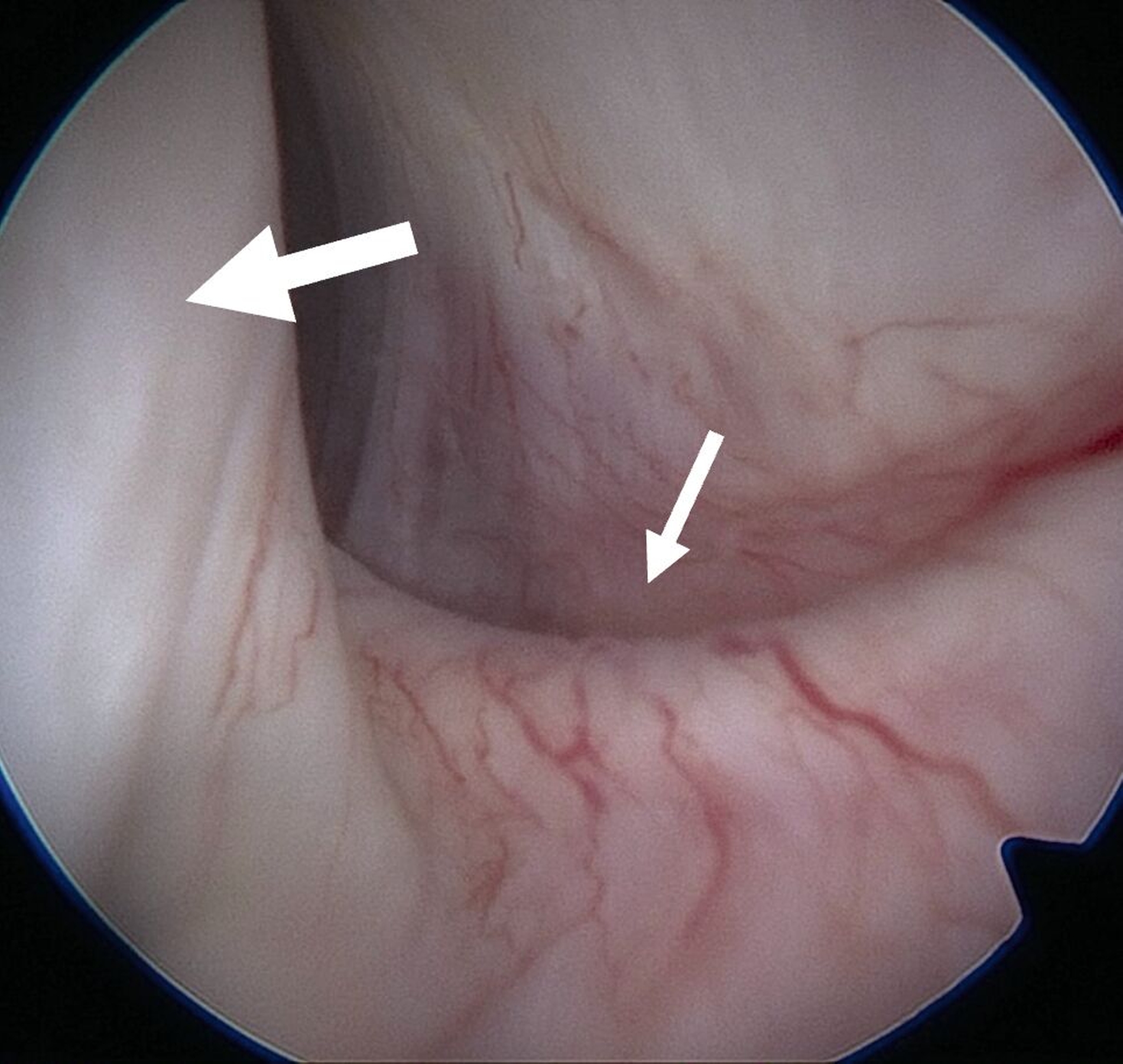
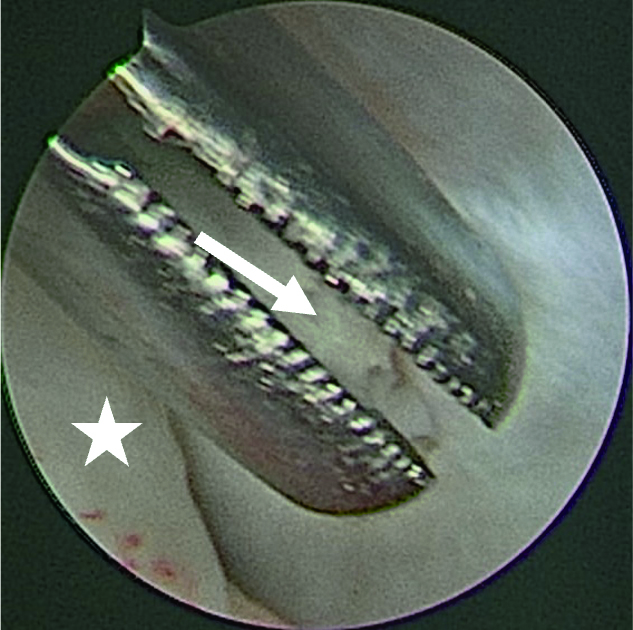
Eine Entzündung im Bereich der Gelenkkapsel (Synovitis) stellt eine häufige Ursache für arthrogen bedingte Beschwerden dar [Mercuri et al., 2025]. Neben der Darstellung des Gelenks und der Behandlung von Pathologien beruht ein positiver Effekt der Arthroskopie auf der Lavage des Gelenks. Dadurch können zum Beispiel proinflammatorische Mediatoren entfernt und intraartikuläre Adhäsionen gelöst werden [Soni, 2019]. Abbildung 2 zeigt die intraoperativen Befunde von zwei Patienten. Es wird jeweils der Übergang zwischen dem hinteren Aufhängungsband und der pars posterior des Discus articularis dargestellt.
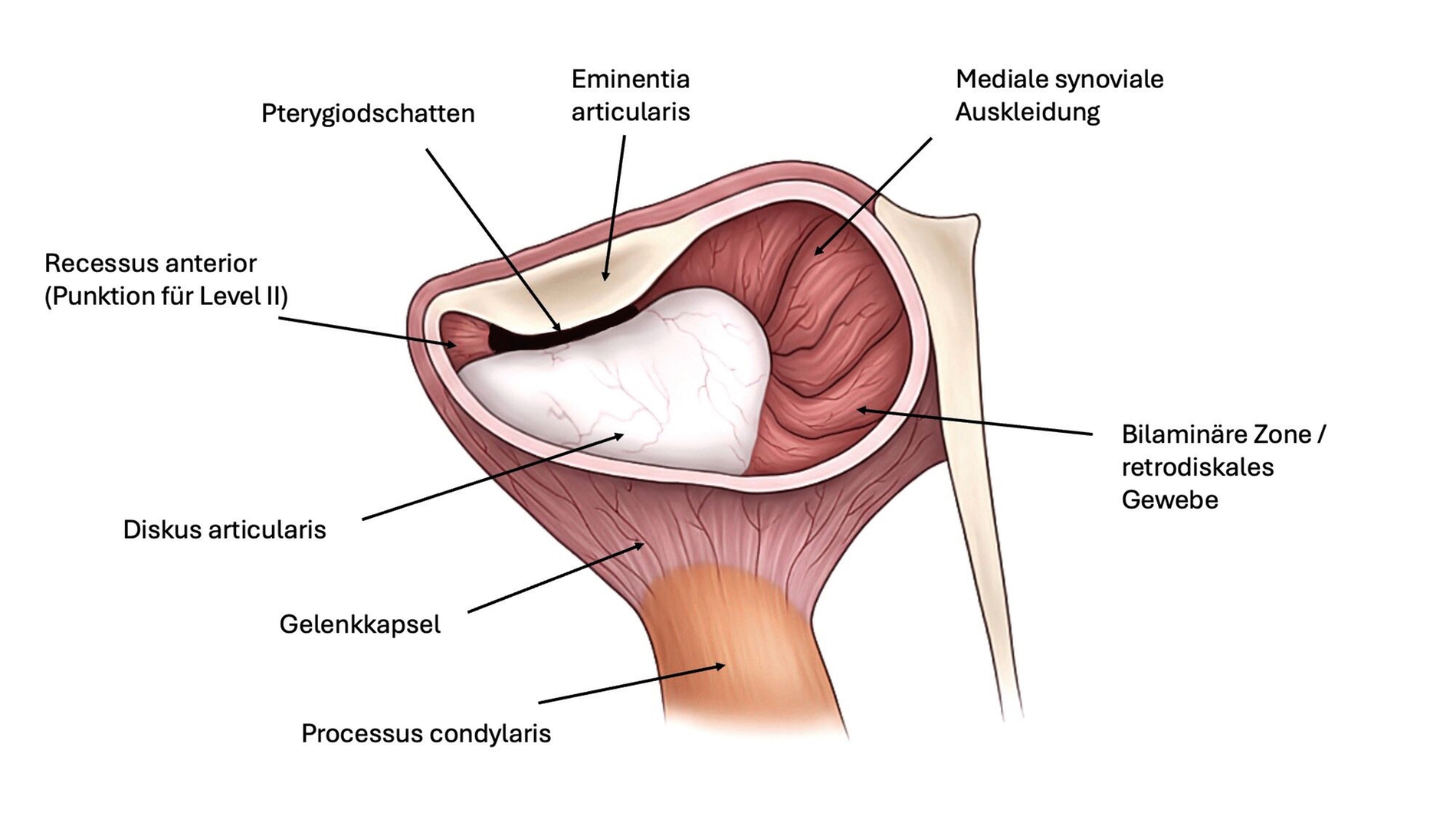
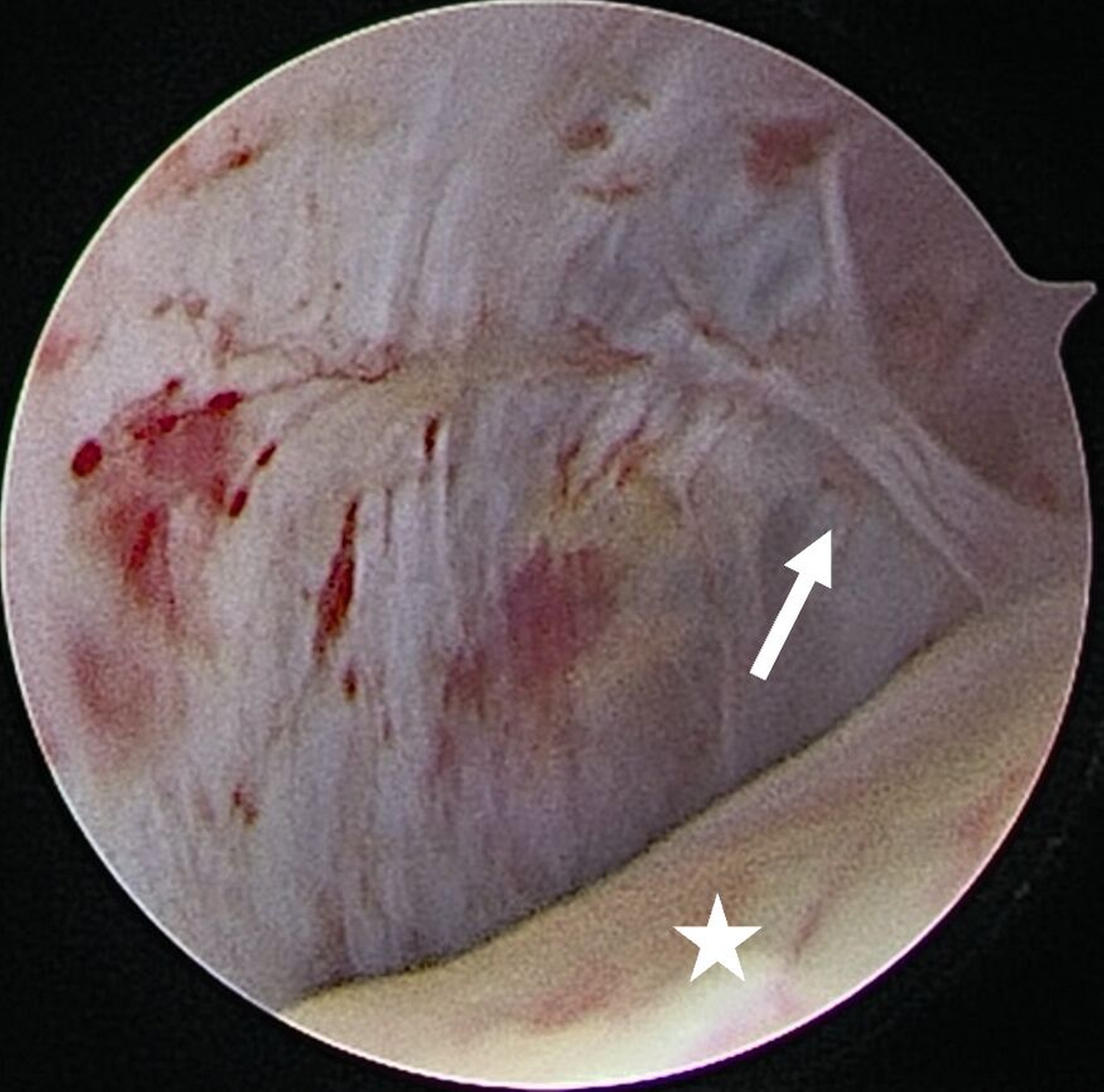
Für die Kiefergelenksarthroskopie ist eine strukturierte Orientierung innerhalb des oberen Gelenkkompartiments essenziell. Hierfür haben sich die sogenannten „seven points of interest“ nach McCain etabliert (Abbildung 3) [Srouji et al., 2018]. Diese sieben anatomischen Referenzpunkte dienen der systematischen Beurteilung des Gelenks während des arthroskopischen Eingriffs. Zunächst werden das mediale synoviale Band und der Pterygoid-Schatten („pterygoid-shadow“) als Orientierungspunkte identifiziert. Es folgen die bilaminäre Zone – eine häufige Schmerzquelle – sowie die hintere Schräge der Gelenkeminenz. Die Beurteilung des Discus articularis gibt Auskunft über Verlagerungen und degenerative Prozesse. Es folgt die Beurteilung der intermediären Zone, die besonders anfällig für eine Perforation ist. Abschließend erfolgt die Begutachtung des vorderen Recessus. Dieser stellt den Eintritt der Punktionsstelle des Level-II-Zugangs dar [Srouji et al., 2018].
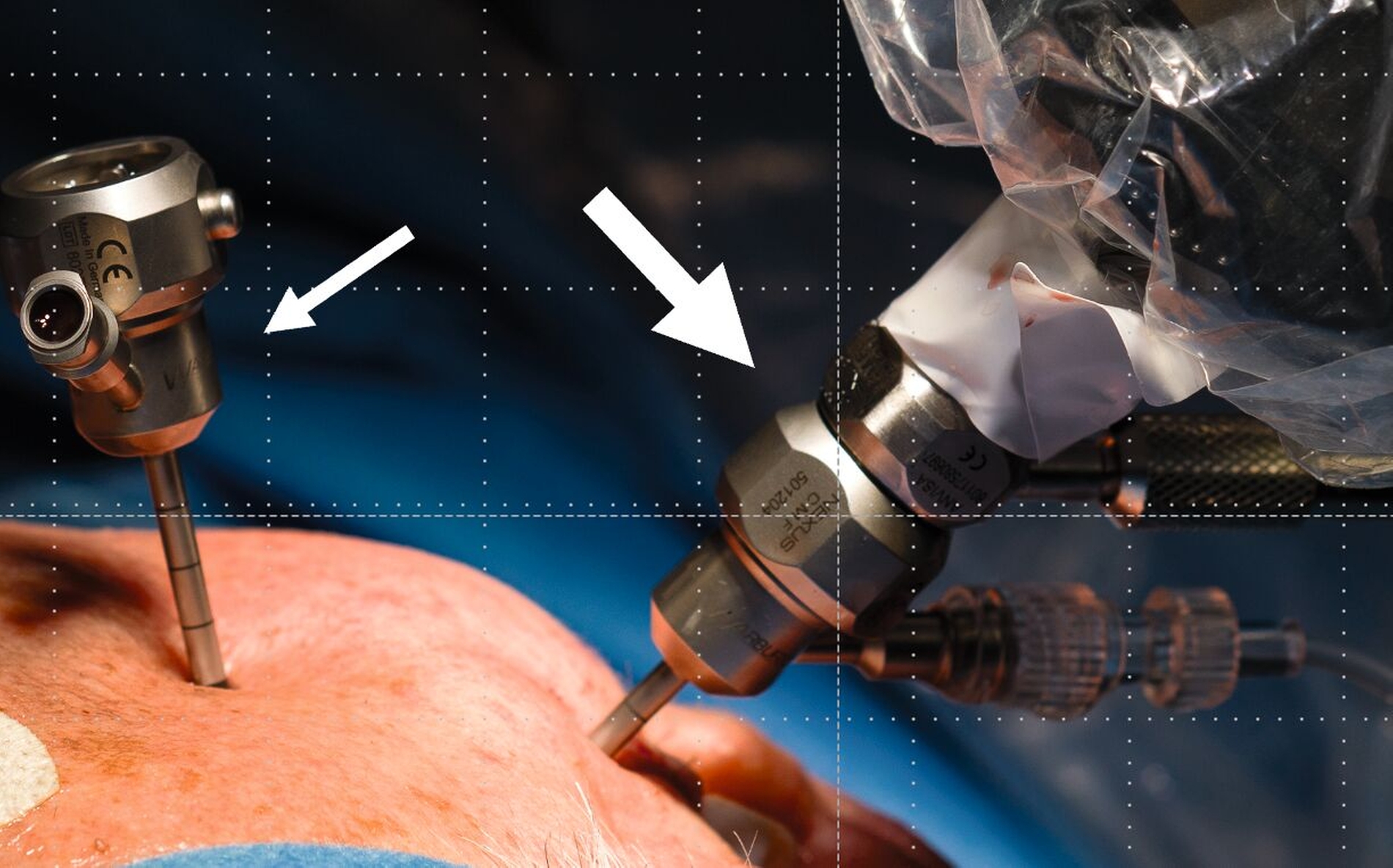
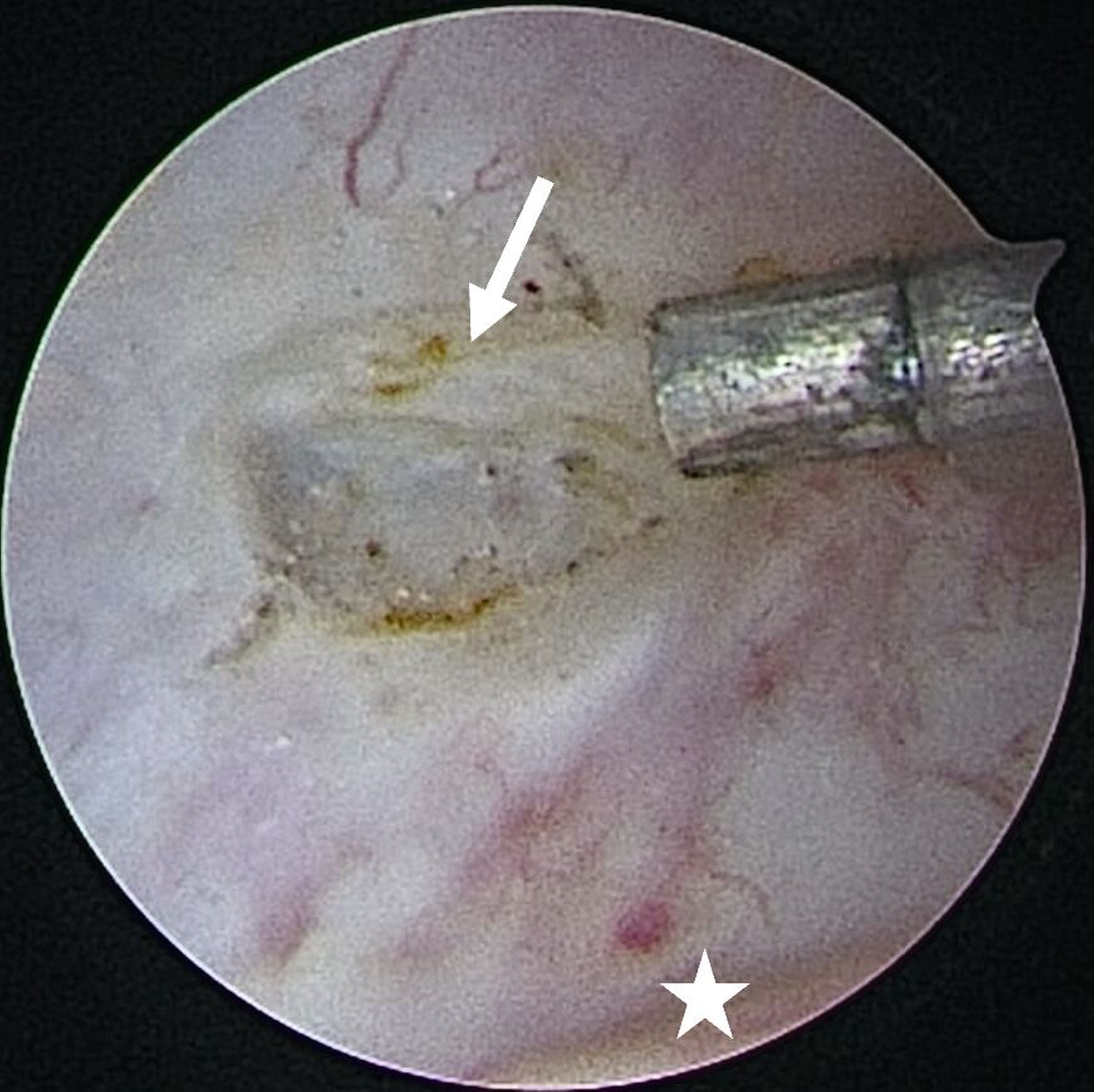
Die Level-II- (Abbildung 4a) beziehungsweisedie Level-III-Arthroskopie beinhalten zusätzlich einen zweiten beziehungsweise einen dritten Zugang über den beispielsweise Verwachsungen entfernt (Abbildung 4b) oder auch Biopsien entnommen werden können. Darüber hinaus ermöglichen diese die Durchführung eines sogenannten „anterior release“ (Abbildung 5). Darunter versteht man das arthroskopische Durchtrennen des vorderen Aufhängungsbandes des Diskus, wodurch dessen Beweglichkeit verbessert werden kann. Auf diese Weise kann der Diskus (unter anschließender konservativer Therapie) wieder in eine physiologischere Position zurückgleiten. Darüber hinaus können auch weiterführende Eingriffe wie Diskopexien durchgeführt werden, also die arthroskopisch gestützte Reposition und Fixation des Diskus in anatomisch korrekter Position [McCain, 1988].
Für intraartikuläre Eingriffe wird häufig die sogenannte Coblation-Technik genutzt (Coblation: Kofferwort aus Controlled Ablation). Diese Technik steht für ein minimalinvasives chirurgisches Verfahren, mit dem durch ein Niedrigtemperaturplasma Gewebe abgetragen werden kann. Im Gegensatz zu thermischen Verfahren wie Laser oder Elektrokaustik arbeitet die Coblation mit Temperaturen zwischen nur 40 bis 70 Grad Celsius. Dadurch kann Gewebe präzise entfernt werden, ohne dass umliegende Strukturen (durch zu hohe Temperaturen) geschädigt werden [Chen et al., 2010].
Als Alternative/Ergänzung zum anterior release kann bei Patientinnen und Patienten mit anteriorer Diskusverlagerung ohne Reposition die Injektion von Botulinumtoxin in den M. pterygoideus lateralis vorgenommen werden. Auch dies kann unter arthroskopischer Kontrolle beziehungsweise im Rahmen eines arthroskopischen Eingriffs (Abbildung 6) mit direkter Sicht erfolgen [Martin-Granizo et al., 2018].
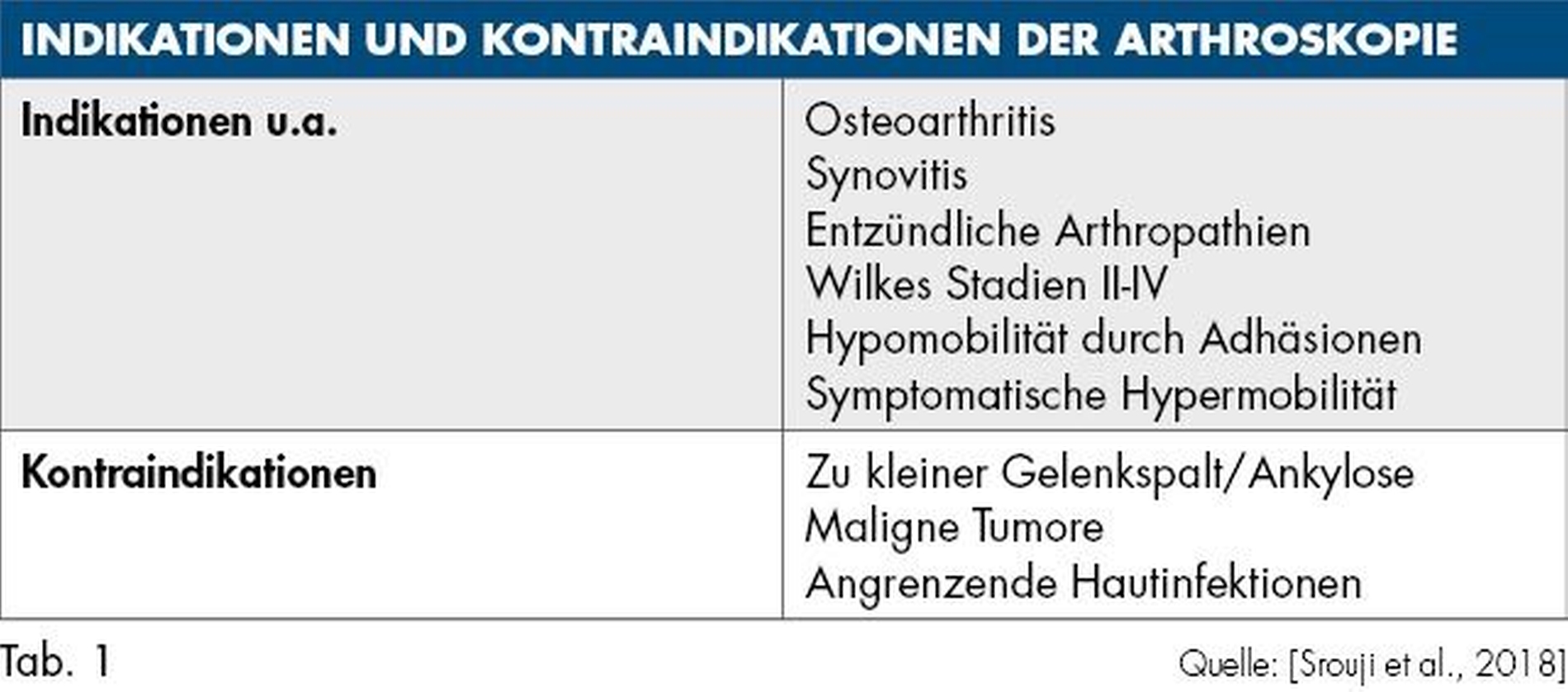
Grundsätzlich kann die Arthroskopie bei einem breiten Indikationsspektrum eingesetzt werden. Es sind nur wenige Kontraindikationen zu beachten (Tabelle 1).
Ein wesentlicher Anteil des therapeutischen Erfolgs der Arthroskopie beruht, je nachdem ob es sich um eine Level I–III handelt, auf der gezielten Beseitigung intraartikulärer Pathologien. Dazu gehören zum Beispiel Verwachsungen, eine eingeschränkte Diskusbeweglichkeit und/oder eine fehlerhafte Diskuslage.
Viele Patienten mit arthrogen bedingten Beschwerden profitieren von einer Kiefergelenksarthroskopie. Bis zu 90 Prozent der Fälle weisen nach der Intervention eine bessere Beweglichkeit des Unterkiefers und/oder weniger Schmerzen auf [Bouloux et al., 2024]. Insbesondere die Kombination mit einer intraartikulären Wirkstoffgabe zeigt sich vorteilhaft [Al-Moraissi et al., 2020b].
Von der Arthroskopie abzugrenzen ist die sogenannte Arthrozentese. Es handelt sich dabei um die Spülung des oberen Gelenkspalts über Punktionskanülen. Eine visuelle Beurteilung des Gelenks ist dadurch nicht möglich. Auch dieses Verfahren zeigt eine hohe Wirksamkeit und gilt als vereinfachte Form der Arthroskopie [Nitzan et al., 2022]. Im direkten Vergleich zeigen verschiedene Studien, dass die Arthroskopie bei arthrogen bedingter CMD der Arthrozentese hinsichtlich funktioneller Verbesserung und Schmerzreduktion überlegen ist [Al-Moraissi, 2015; Al-Moraissi et al., 2020b; Tang et al., 2024]. Insgesamt fehlt es jedoch an abschließender Evidenz, um den Vergleich zwischen Arthroskopie, Arthrozentese und konservativer Therapie zu bewerten.
Injektionswirkstoffe erhöhen die Effektivität
Im Rahmen einer Arthroskopie beziehungsweise Arthrozentese können verschiedene Wirkstoffe ins Gelenk injiziert werden. Dazu zählen Kortikosteroide, Hyaluronsäure sowie plättchenreiches Plasma (PRP) und flüssiges plättchenreiches Fibrin (PRF) [Farshidfar et al., 2025; Zotti et al., 2019]. Eine Metaanalyse aus dem Jahr 2020 zeigt insbesondere für die PRP-Injektion vielversprechende Ergebnisse, mit überlegener Schmerzreduktion und einer Verbesserung der Mundöffnung im Vergleich zu anderen Wirkstoffen [Al-Moraissi et al., 2020b]. Gleichzeitig weisen mehrere Autoren darauf hin, dass die aktuell verfügbare Evidenz maßgeblich auf heterogenen Studien basiert. Belastbare Schlussfolgerungen zur Überlegenheit einzelner Wirkstoffe sind deshalb bisher nur eingeschränkt möglich [Dolwick et al., 2020].
Fallbericht
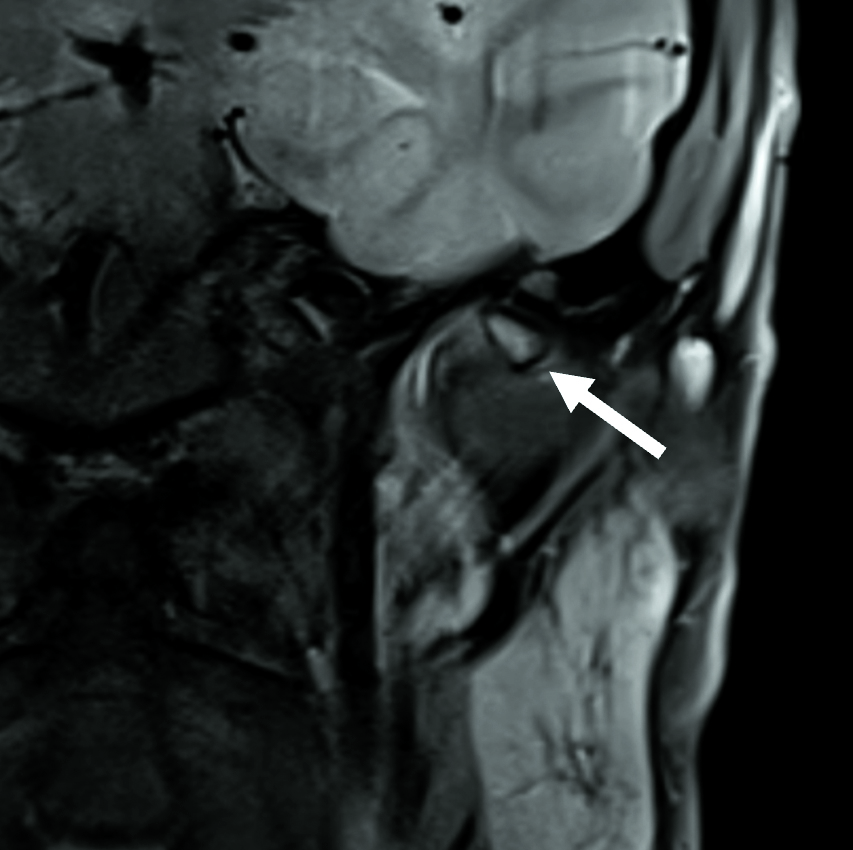
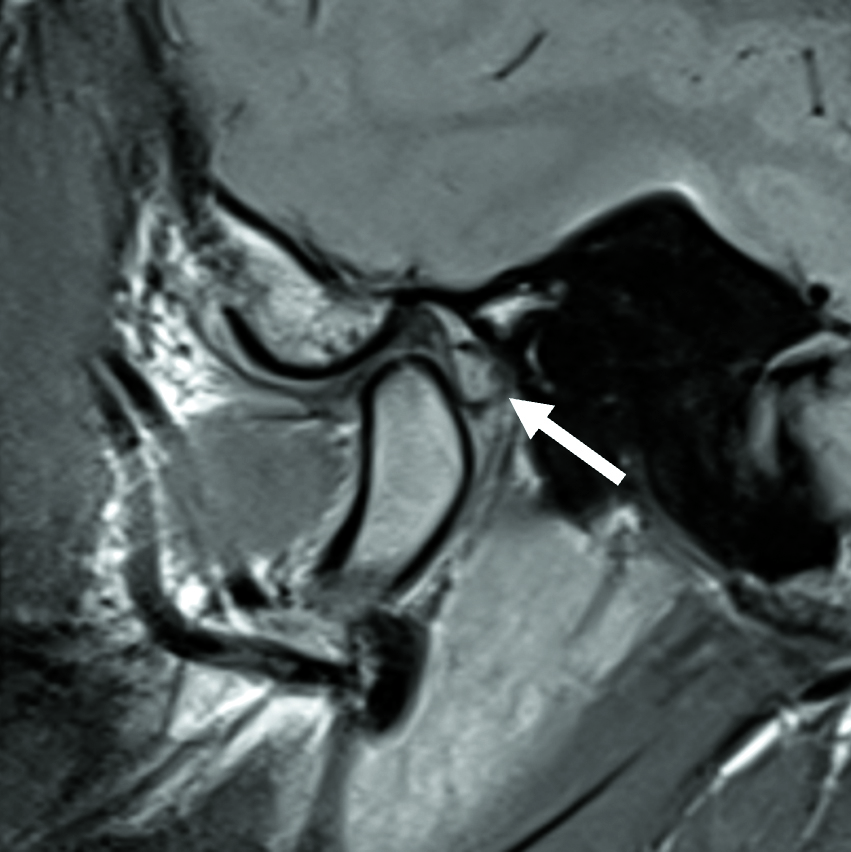
Ein Patient stellte sich in unserer Klinik mit einer seit zwei Wochen bestehenden Okklusionsstörung vor. Klinisch zeigte sich bei habituellem Mundschluss eine Protrusionsstellung des Unterkiefers. Darüber hinaus berichtete der Patient über Schmerzen im linken Kiefergelenk, insbesondere bei Mobilisation nach dorsal. Durch die zeitnah durchgeführte MRT-Untersuchung wurde eine synoviale Chondromatose des linken Kiefergelenks diagnostiziert. Die beschriebene Symptomatik wurde am ehesten von einem circa 8 mm großen freien Gelenkkörper im dorsalen Bereich des Gelenks verursacht, der ein Zurückgleiten des Diskus articularis (beziehungsweise des Kondylus) verhinderte (Abbildung 7).

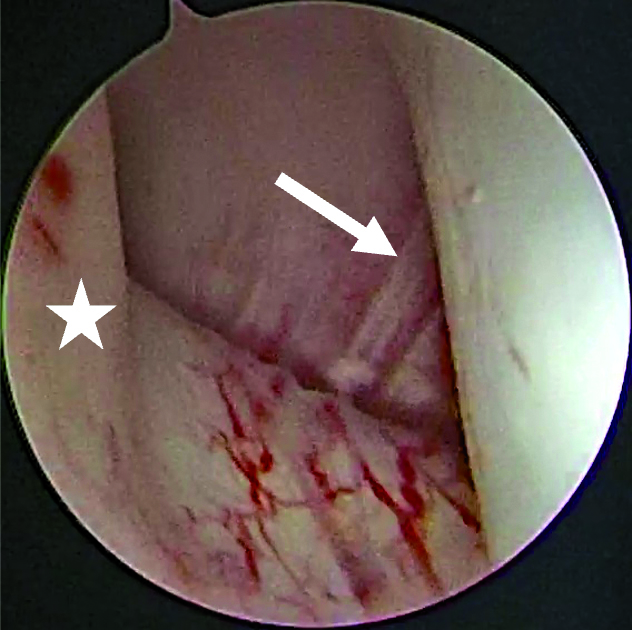
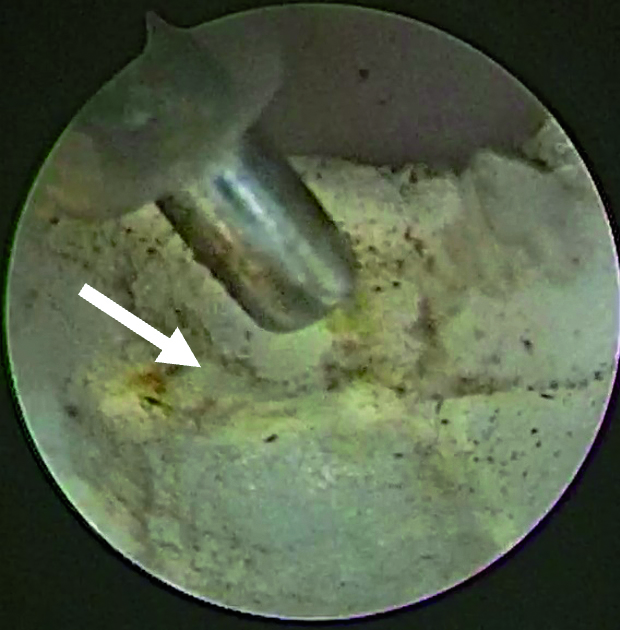
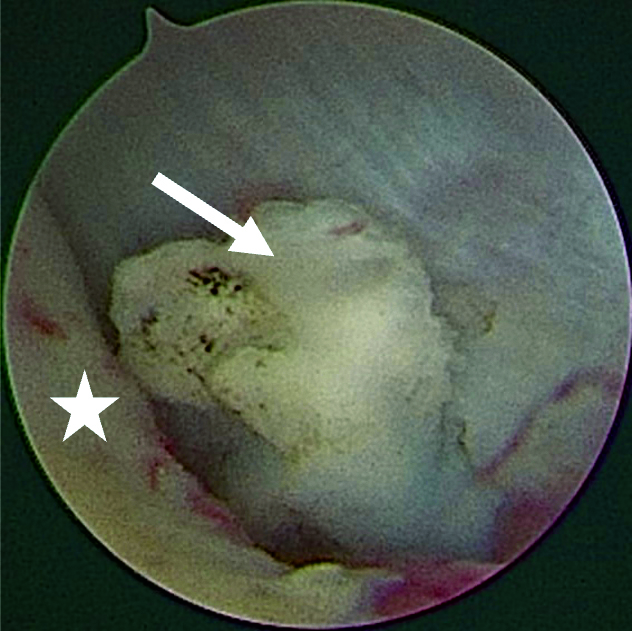
Im Rahmen einer Level-II-Arthroskopie (Abbildung 8) in Vollnarkose konnte der Gelenkkörper nach Zerkleinerung durch Coblation über einen Arbeitskanal vollständig entfernt werden. Die histologische Aufarbeitung ergab hyalinen Knorpel mit (sklerosiertem) Bindegewebe. Der Eingriff verlief komplikationslos; postoperativ zeigte sich unmittelbar eine regelrechte Okklusion. Die Schmerzen waren am ersten postoperativen Tag bereits vollständig regredient.
Das CMD-Behandlungskonzept der MKG Charité
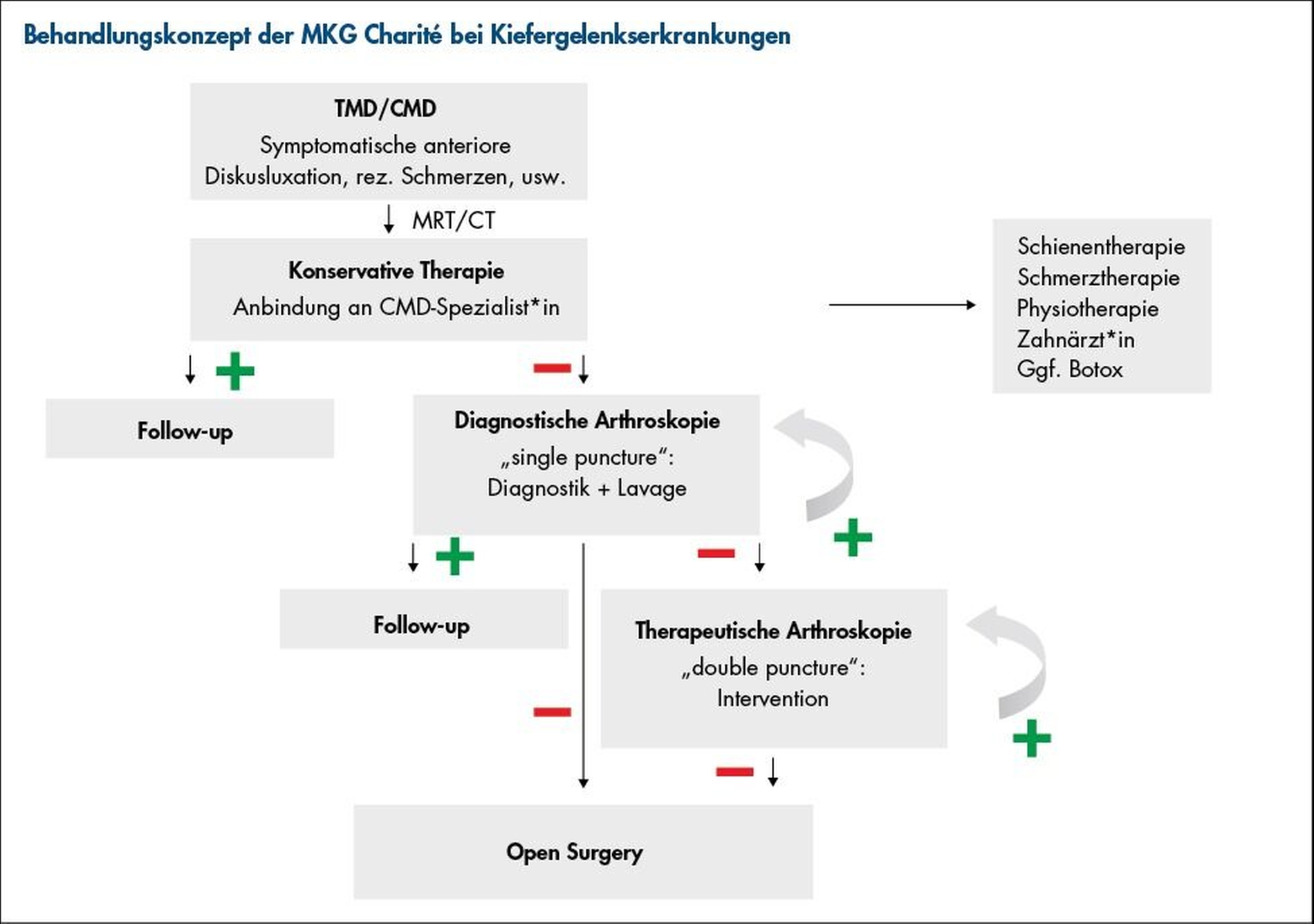
Die Behandlung der CMD erfolgt interdisziplinär in enger Zusammenarbeit mit Kolleginnen und Kollegen der Zahnmedizin sowie der Physio- und Schmerztherapie. Nach ausführlicher Untersuchung folgt eine entsprechende Therapie. Die Aufklärung des Patienten über die bestehende Leitkomponente ist dabei der erste Schritt. Ist eine funktionelle Behandlung notwendig, steht die Schienentherapie mittels adjustierter Aufbissschiene im Zentrum der Therapie. Neben der Funktionsdiagnostik (falls nicht bereits bei Vorstellung vorhanden) erfolgt bei speziellen Fragestellungen zur Beurteilung des Gelenks eine dreidimensionale knöcherne Bildgebung (DVT oder CT) sowie die Darstellung der Weichgewebe im Rahmen einer funktionellen MRT-Bildgebung.
Ist eine klinische Besserung der Symptomatik trotz entsprechend konservativer (Vor-)Behandlung nicht zu erwarten, kann bei arthrogen bedingten Beschwerden nach etwa drei Monaten eine diagnostische Arthroskopie des Kiefergelenks indiziert sein (Abbildung 9). Neben der visuellen Beurteilung intraartikulärer Strukturen ermöglicht das Verfahren eine Lavage, die in vielen Fällen bereits zu einer deutlichen Symptomlinderung führt. Bei persistierenden Beschwerden kann die Arthroskopie im Verlauf wiederholt oder auf weiterführende minimalinvasive Eingriffe (Level II/III) ausgeweitet werden. Dabei fokussieren wir uns aktuell vorwiegend auf Level-II-Techniken, da Level-III-Eingriffe an unserer Klinik aufgrund der aktuell noch begrenzten Datenlage und eines erhöhten Risikoprofils nur bei seltenen Befundkonstellationen zum Einsatz kommen.
Sollte eine arthroskopische Behandlung nicht möglich oder erfolgversprechend erscheinen, ist in ausgewählten Fällen ein offenes chirurgisches Vorgehen indiziert [Baecher et al., 2025]. Bei myogener Genese kann darüber hinaus zusätzlich eine Botulinumtoxin-Injektion in die Kaumuskeln zur Reduktion von Schmerzen und Muskelhyperaktivität beitragen. Neue Therapieoptionen wie die transarterielle Embolisation (TAE) können bei therapieresistenten Beschwerden in Erwägung gezogen werden [Fleckenstein et al., 2025].
Zusammenfassung
Aufgrund des hohen Leidensdrucks der CMD-Patientinnen und -Patienten, die auf konservative Therapien nicht ausreichend ansprechen, gewinnen minimalinvasive Verfahren zunehmend an Bedeutung. Sowohl die Literatur als auch unsere klinischen Erfahrungen zeigen, dass viele Patienten mit arthrogen bedingten Beschwerden von einer Arthroskopie profitieren. Das Risikoprofil ist gering. Entsprechend sollte dieses Verfahren frühzeitig angeboten werden.
Fünf Videosequenzen ergänzen die grafischen Darstellungen und vermitteln ein räumliches Verständnis der arthroskopischen Befunde:
>>Arthroskopische Entfernung einer Chondromatose (Level II)
>>Arthroskopisch kontrollierte Vollblutinjektion
>>Diskusperforation rechtes Kiefergelenk
Literaturliste
Al-Moraissi, EA. Arthroscopy versus arthrocentesis in the management of internal derangement of the temporomandibular joint: a systematic review and meta-analysis. Int J Oral Maxillofac Surg 2015; 44, 104–112.
Al-Moraissi, EA, Farea, R, Qasem, KA, Al-Wadeai, MS, Al-Sabahi, ME & Al-Iryani, GM. Effectiveness of occlusal splint therapy in the management of temporomandibular disorders: network meta-analysis of randomized controlled trials. Int J Oral Maxillofac Surg 2020a; 49, 1042–1056.
Al-Moraissi, EA, Wolford, LM, Ellis, E, 3rd & Neff, A. The hierarchy of different treatments for arthrogenous temporomandibular disorders: A network meta-analysis of randomized clinical trials. J Craniomaxillofac Surg 2020b; 48, 9–23.
Angelo, DF, Sanz, D, Maffia, F & Cardoso, HJ. Outcomes of IncobotulinumtoxinA Injection on Myalgia and Arthralgia in Patients Undergoing Temporomandibular Joint Arthroscopy: A Randomized Controlled Trial. Toxins (Basel) 2023; 15.
Baecher, H, Maheta, B, Lottner, LM, Panayi, AC, Knoedler, S, Guastaldi, F, Mano, JF, Koerdt, S, Rendenbach, C, Heiland, M, Knoedler, L & Doll, C. Current clinical and translational challenges in temporomandibular joint reconstruction. Front Bioeng Biotechnol 2025; 13, 1590021.
Bouloux, GF, Chou, J, DiFabio, V, Ness, G, Perez, D, Mercuri, L, Chung, W & Crago, CA. The Contemporary Management of Temporomandibular Joint Intra-Articular Pain and Dysfunction. J Oral Maxillofac Surg 2024; 82, 623–631.
Chen, MJ, Yang, C, Zhang, SY & Cai, XY. Use of Coblation in arthroscopic surgery of the temporomandibular joint. J Oral Maxillofac Surg 2010; 68, 2085–2091.
DGFDT. 2022. Zur Therapie craniomandibulärer Dysfunktionen [Online]. Available: www.dgfdt.de/documents/266840/266917/Wissenschaftliche+Mitteilung+zurTherapie+der+craniomandibulären+Dysfunktion/ec517239-963b-41bd-ac1d-79ebe628090d [abgerufen am 25.10.2025].
Dolwick, MF & Widmer, CG. Temporomandibular joint arthrocentesis: an evidence-based review. Frontiers of Oral and Maxillofacial Medicine 2020; 2.
Farshidfar, N, Amiri, MA, Estrin, NE, Ahmad, P, Zhang, Y, Sculean, A & Miron, RJ. Use of liquid platelet-rich fibrin (liquid PRF) in temporomandibular joint disorders: A narrative review with clinical recommendations. Periodontol 2000 2025; 00, 1–23.
Fleckenstein, FN, Voss, J, Doll, C, Maleitzke, T, Winkler, T, Siebert, E & Collettini, F. Transcatheter Arterial Embolization as a Treatment for Chronic Pain due to Temporomandibular Joint Osteoarthritis. CardioVascular and Interventional Radiology 2025; 48, 687–693.
Hugger, A, Lange, M, Schindler, M & Türp, JC. Begriffsbestimmungen: Funktionsstörung, Dysfunktion, craniomandibuläre Dysfunktion (CMD), Myoarthropathie des Kausystems (MAP). Deutsche Zahnärztliche Zeitschrift 2016; 71, 165–166.
Martin-Granizo, R, Maniegas, L, Colorado, L, Millon-Cruz, A & de Pedro, M. Direct infiltration of botulinum toxin into the pterygoid lateral muscle for repositioning of the disc during arthroscopy of the temporomandibular joint. Br J Oral Maxillofac Surg 2018; 56, 769–771.
McCain, JP. Arthroscopy of the human temporomandibular joint. J Oral Maxillofac Surg 1988; 46, 648–655.
McCain, JP (ed.) 1996. Principles and Practice of Temporomandibular Joint Arthroscopy. St. Louis: Mosby.
Mercuri, LG, Greene, CS & Manfredini, D. The temporomandibular joint disc: A complex fable about an elusive butterfly. Cranio 2025, 1–8.
Monje Gil, F, Martínez Artal, P, Cuevas Queipo de Llano, A, Muñoz Guerra, M, González Ballester, D, López Arcas, JM, López Cedrún, JL, Gutiérrez Pérez, JL, Martín-Granizo, R, Del Castillo Pardo de Vera, JL, García Medina, B, González-García, R, Moreno Sánchez, M, Rodríguez, EV, Fernández Sanromán, J, López Martos, R, Peral Cagigal, B, Redondo Alamillos, M, Morey Mas, M, Salcedo Gil, C, Ramos Medina, B, Valls Ontañón, A, Masià Gridilla, J & Dean Ferrer, A. Consensus Report and Recommendations on the Management of Late-stage Internal Derangement of the Temporomandibular Joint. J Clin Med 2024; 13.
Neff, A & Schmidt, C. 2021. Inflammatorische Erkrankungen des Kiefergelenks - Juvenile idiopathische Arthritis und Rheumatoide Arthritis des Kiefergelenks [Online]. Available: www.awmf.org/leitlinien/detail/ll/007-061.html [abgerufen am 25.10.2025].
Nitzan, DW & Naaman, HL. Athrocentesis: What, When, and Why? Atlas Oral Maxillofac Surg Clin North Am 2022; 30, 137–145.
Schindler, H, Türp, J. (eds.) 2017. Konzept Okklusionsschiene: Quintessence Publishing.
Soni, A. Arthrocentesis of Temporomandibular Joint- Bridging the Gap Between Non-Surgical and Surgical Treatment. Ann Maxillofac Surg 2019; 9, 158–167.
Srouji, S & McCain, J (eds.) 2018. Modern Temporomandibular Joint Arthroscopy: Operative Single-Cannula Arthroscopy. In: Nahlieli, O. (ed.) Minimally Invasive Oral and Maxillofacial Surgery, Berlin, Heidelberg: Springer.
Tang, YH, van Bakelen, NB, Gareb, B & Spijkervet, FKL. Arthroscopy versus arthrocentesis and versus conservative treatments for temporomandibular joint disorders: a systematic review with meta-analysis and trial sequential analysis. Int J Oral Maxillofac Surg 2024; 53, 503–520.
Weber, D & Neff, A. Die interdisziplinäre Diagnoseklassifikation des craniomandibulären Systems (DC-CMS). Die MKG-Chirurgie 2025a; 18, 195–203.
Weber, D, Neff, A, Peroz, I, Koerdt, S, Doll, C & von Stein-Lausnitz, M. 2025b. Die interdisziplinäre Diagnoseklassifikation des craniomandibulären Systems (DC-CMS) [Online]. Available: www.zm-online.de/artikel/2025/zm-2025-21/die-interdisziplinaere-diagnoseklassifikation-des-craniomandibulaeren-systems-dc-cms [abgerufen am 16.11.2025].
Zieliński, G, Pająk-Zielińska, B & Ginszt, M. A Meta-Analysis of the Global Prevalence of Temporomandibular Disorders. J Clin Med 2024; 13.
Zotti, F, Albanese, M, Rodella, LF & Nocini, PF. Platelet-Rich Plasma in Treatment of Temporomandibular Joint Dysfunctions: Narrative Review. Int J Mol Sci 2019; 20, 277.