Ist eine gesteuerte Knochenregeneration mit Meeresalgen möglich?
Resorbierbare und volumenstabile Membranen auf Kollagenbasis gelten in der Zahnmedizin als etablierter Standard für eine gesteuerte Geweberegeneration, Bindegewebsaugmentationen und Knochenaufbauverfahren. Trotz ihrer bewährten klinischen Anwendung bestehen weiterhin gewisse Herausforderungen:
So lässt sich die potenzielle Prionenbelastung tierischer Materialien theoretisch nicht vollständig ausschließen, die Herstellungsprozesse sind mit entsprechendem Aufwand verbunden – und auch ethische Fragestellungen rücken zunehmend in den Fokus. Zudem können individuelle religiöse oder weltanschauliche Überzeugungen von Patientinnen und Patienten in Einzelfällen Einfluss auf die Materialpräferenz nehmen. Diese Aspekte verdeutlichen ein wachsendes Interesse an nachhaltigen, Tierprodukt-freien Alternativen, die sowohl biologisch leistungsfähig als auch wirtschaftlich darstellbar und gesellschaftlich breit akzeptiert sind.
Vor diesem Hintergrund wurden pflanzen- und marinenbasierte Biomaterialien in den vergangenen Jahren vermehrt als mögliche Alternativen untersucht. Ziel der Studien der Kieler Forschungsgruppe war es, Meeresalgen als Quelle biobasierter Polymere systematisch zu untersuchen, geeignete Arten mit günstigen biologischen Eigenschaften zu identifizieren und in PLA-Komposite für eine potenzielle klinische Anwendung zu integrieren.
Eine echte Alternative zu Kollagenmembranen?
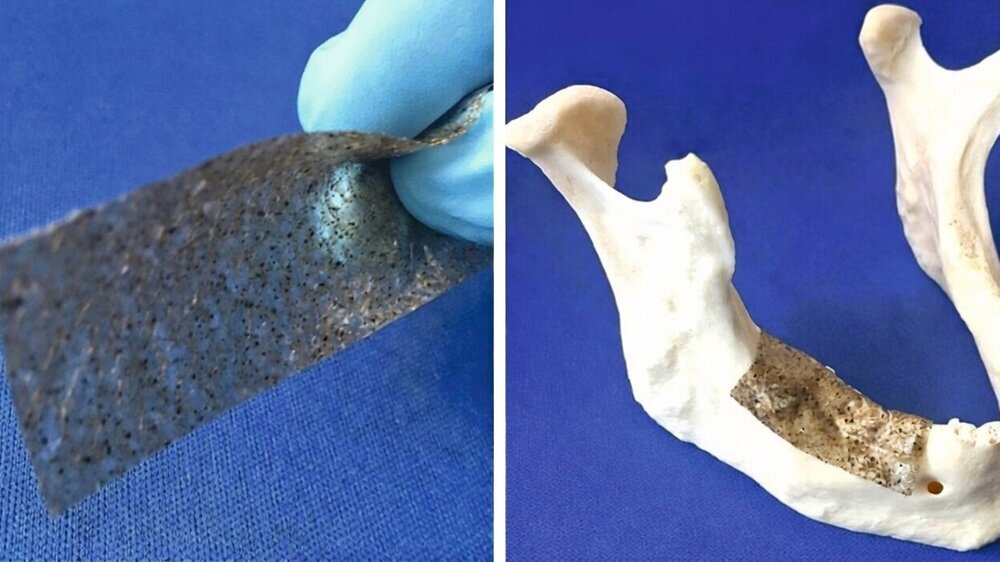
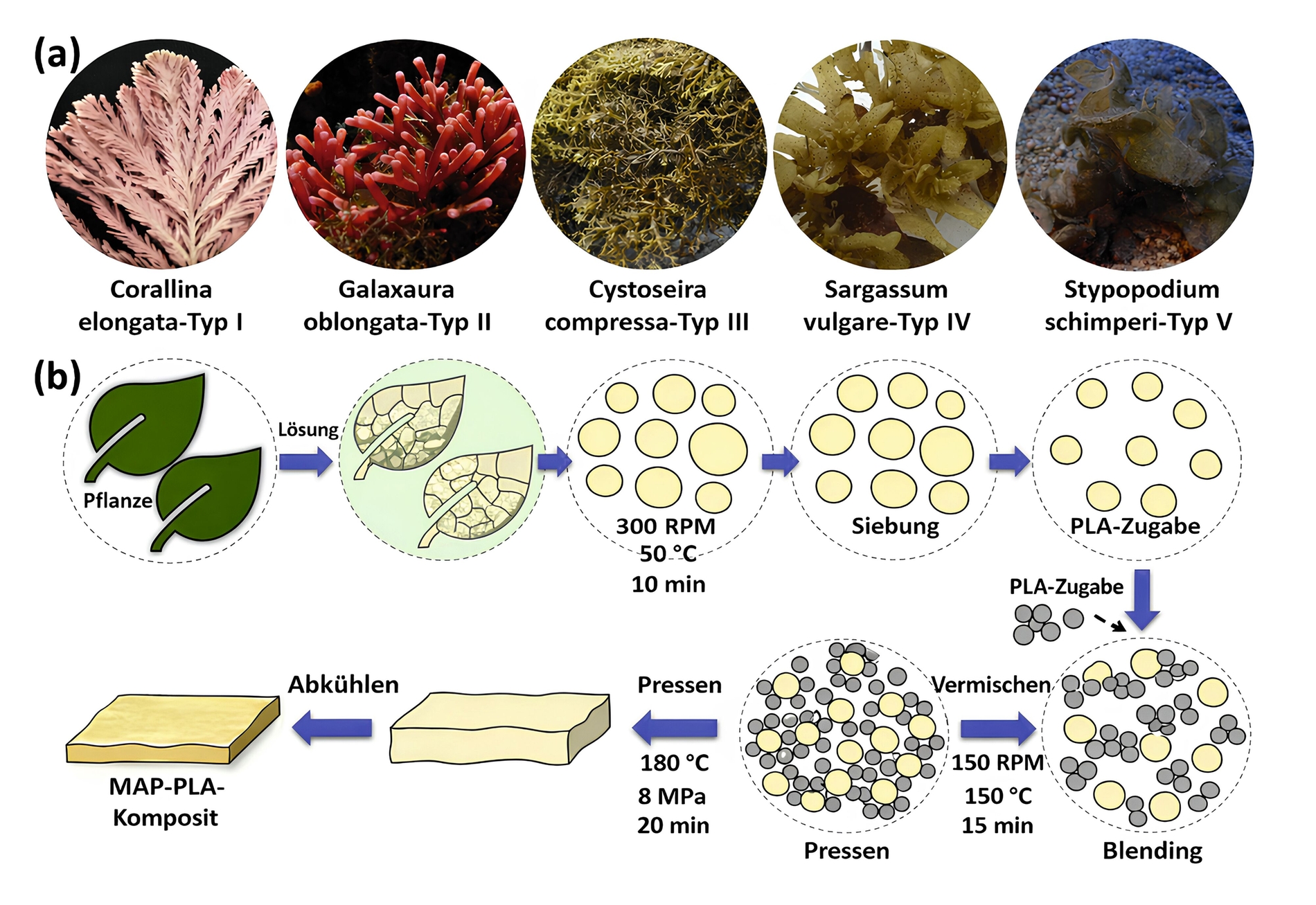
In der ersten Studie [Sayin et al., 2020] wurden fünf marine Algenarten — Corallina elongata, Galaxaura oblongata, Cystoseria compressa, Sargassum vulgare und Stypopodium schimperi — aus dem Mittelmeer bei Antalya und Iskenderun (Türkei) gesammelt, gereinigt, getrocknet und zu Meeresalgen(MAP)-PLA-Membranen verarbeitet. Zytokompatibilitätstests zeigten, dass alle Membranen zellverträglich waren. Besonders hervorzuheben war, dass Sargassum-vulgare-PLA (Typ IV) die Proliferation von Osteoblasten über alle Referenzgruppen hinweg förderte.
Diese Ergebnisse deuten darauf hin, dass Meeresalgen-basierte Membranen eine praktikable, Tierprodukt-freie Alternative zu Kollagenmembranen für eine gesteuerte Geweberegeneration, Bindegewebsaugmentation und Wundheilung darstellen könnten. Abbildung 1 zeigt die gesammelten Arten sowie das Herstellungsschema der MAP-PLA-Membranen.
Bei Osteosarkomzellen potenziell tumorhemmend
Aufbauend auf diesen Erkenntnissen wurde die selektive Wirkung von Sargassum-vulgare-PLA-Patches auf Osteosarkomzellen (SaOS-2) untersucht [Veziroglu et al., 2021]. Während die Proliferation humaner Osteoblasten (HOBs) unverändert hoch blieb, zeigte sich bei den SaOS-2-Zellen eine signifikant reduzierte Zellproliferation. Der zugrunde liegende Mechanismus scheint in der Störung der Filopodien zwischen den Tumorzellen zu liegen, was die Zell-zu-Zell-Kontakte reduziert. Diese Ergebnisse lassen vermuten, dass SVP-PLA-Patches potenziell tumorhemmend wirken können, ohne die normale Knochenbildung zu beeinträchtigen – und möglicherweise eine klinisch relevante Option für ossäre Karzinome in der Zahnmedizin darstellen.
Ein weiterer Vorteil für die klinische Anwendung einer Membran wäre ihre Resistenz gegenüber einer bakteriellen Besiedlung. Die getesteten Algen-PLA-Komposite zeigten durchweg eine hohe Zytokompatibilität, wobei die bakterielle Kolonisation insbesondere bei Sargassum-vulgare-PLA deutlich reduziert war, gefolgt von Galaxaura-oblongata-PLA und Cystoseria-compressa-PLA. SEM-Analysen deuten auf glattere Oberflächen im Vergleich zu kollagenbasierten Membranen hin, was möglicherweise eine Infektionsreduktion sowie die Gewebe- und Knochenregeneration unterstützen kann [Weitkamp et al., 2024].
Schließlich wurde das Potenzial der Oberflächenfunktionalisierung untersucht. In enger Zusammenarbeit mit der Technischen Fakultät Kiel (Chair for Multicomponent Materials) wurden die MAP-PLA-Patches mittels eines besonderen Beschichtungsverfahrens (initiated Chemical Vapor Deposition, iCVD) mit einem speziellen Polymeren (p(HEMA-co-EGDMA)) beschichtet. Dadurch konnten eine erhöhte Hydrophilie sowie eine optimale Zelladhäsion der Osteoblasten erreicht werden, während die Morphologie der Membranen unverändert blieb. Diese funktionalisierten Patches eignen sich besonders für Anwendungen im Knochen- und Gewebeengineering in der Zahnmedizin und in der Orthopädie [Reichstein et al., 2021].
Knochenersatzmaterial aus Rotalgen ist bereits etabliert
Ein weiterer interessanter Aspekt ist, dass bereits ein Knochenersatzmaterial (KEM) auf dem Markt ist, das aus Rotalgen stammt und vor 30 Jahren – ebenfalls in Kiel – unter der Leitung von Prof. Dr. Dr. Rolf Ewers entwickelt wurde. Die Ergebnisse seiner Studie zur Sinusbodenelevation zeigen stabile und zuverlässige Ergebnisse [Ewers, 2005]. Das Material – über Jahre unter dem Namen Algipore etabliert und heute als AlgOss 100 verfügbar – gilt als eines der am längsten wissenschaftlich dokumentierten algenbasierten Knochenaufbaumaterialien.
Die Arbeiten zeigen, dass Membranen aus Meeresalgen-PLA-Kompositen eine nachhaltige, Tierprodukt-freie Alternative darstellen könnten. Die Ex-vivo-Ergebnisse liefern vielversprechende Hinweise für die klinische Anwendung, insbesondere im Hinblick auf die Zellkompatibilität, die antibakterielle Wirkung und selektiv anti-proliferative Eigenschaften. Parallel dazu weisen die entwickelten Membranen eine hohe funktionelle Modifizierbarkeit auf.
Gleichzeitig bestehen noch Herausforderungen, die für die Translation in die klinische Praxis berücksichtigt werden müssen:
unterschiedliche Eigenschaften derselben Algenart unter verschiedenen Umweltbedingungen
eine potenzielle Schwermetallbelastung
Lagerung und Sterilisation, die noch standardisiert werden müssen
Die potenzielle Anwendung der Meeresalgen-Membranen eröffnet erstmals die realistische Perspektive eines vollständig pflanzen- beziehungsweise algenbasierten GBR-Protokolls. Ein solches veganes Regenerationskonzept geht dabei weit über die bloße Substitution tierischer Materialien hinaus; vielmehr repräsentiert es einen paradigmatischen Ansatz zur Etablierung einer neuartigen Biomaterialklasse in der Zahnmedizin. Diese zeichnet sich dadurch aus, dass sie
nachhaltig und ressourcenschonend gewonnen werden kann,
ethisch sowie religiös universell akzeptabel ist,
potenziell unabhängig von tierischen Lieferketten und
gezielt biologisch funktionalisierbar ist.
Literaturliste
Sayin S, Kohlhaas T, Veziroglu S, Okudan EŞ, Naz M, Schröder S, Saygili EI, Acil Y, Faupel F, Wiltfang J, Aktas OC, Gülses A. Marine Algae-PLA composites as de novo alternative to porcine derived collagen membranes. Materials Today Chemistry, 2020;17:100276. ISSN: 2468-5194.
Veziroglu S, Ayna M, Kohlhaas T, Sayin S, Fiutowski J, Mishra YK, Karayürek F, Naujokat H, Saygili EI, Acil Y, Wiltfang J, Faupel F, Aktas OC, Gülses A. Marine Algae Incorporated Polylactide Acid Patch: Novel Candidate for Targeting Osteosarcoma Cells without Impairing the Osteoblastic Proliferation. Polymers (Basel). 2021 Mar 10;13(6):847. doi: 10.3390/polym13060847. PMID: 33801946; PMCID: PMC8001715.
Reichstein W, Sommer L, Veziroglu S, Sayin S, Schröder S, Mishra YK, Saygili Eİ, Karayürek F, Acil Y, Wiltfang J, Gülses A, Faupel F, Aktas OC. Initiated Chemical Vapor Deposition (iCVD) Functionalized Polylactic Acid-Marine Algae Composite Patch for Bone Tissue Engineering. Polymers (Basel). 2021 Jan 7;13(2):186. doi: 10.3390/polym13020186. PMID: 33430187; PMCID: PMC7825612.
Weitkamp JT, El Hajjami S, Acil Y, Spille J, Sayin S, Okudan ES, Saygili EI, Veziroglu S, Flörke C, Behrendt P, Wiltfang J, Aktas OC, Gülses A. Antibacterial properties of marine algae incorporated polylactide acid membranes as an alternative to clinically applied different collagen membranes. J Mater Sci Mater Med. 2024 Jan 29;35(1):9. doi: 10.1007/s10856-024-06778-y. PMID: 38285196; PMCID: PMC10824850.
Ewers R. Maxilla sinus grafting with marine algae derived bone forming material: a clinical report of long-term results. J Oral Maxillofac Surg. 2005 Dec;63(12):1712-23. doi: 10.1016/j.joms.2005.08.020. PMID: 16297691.