Odontogene Sinusitis erkennen und richtig behandeln
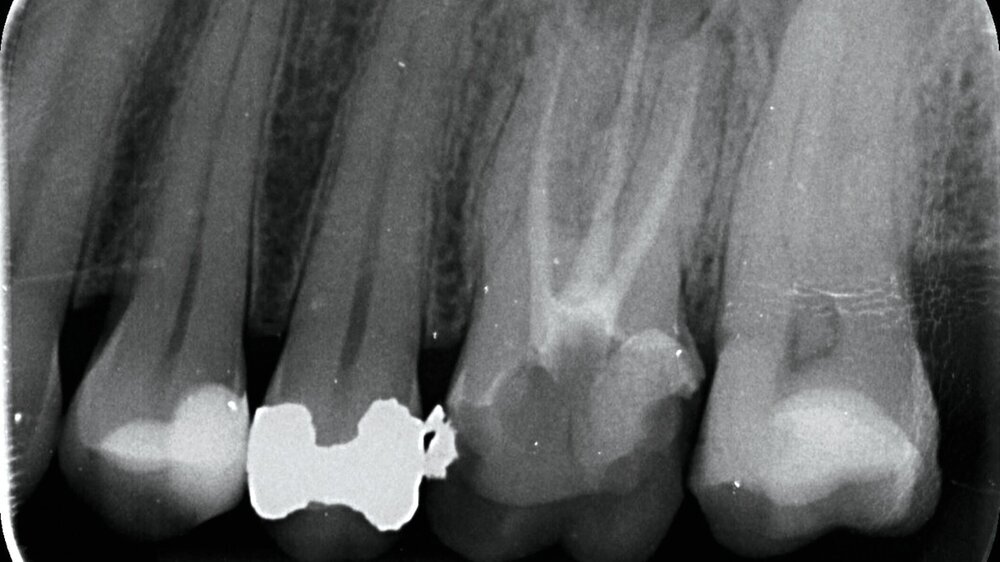
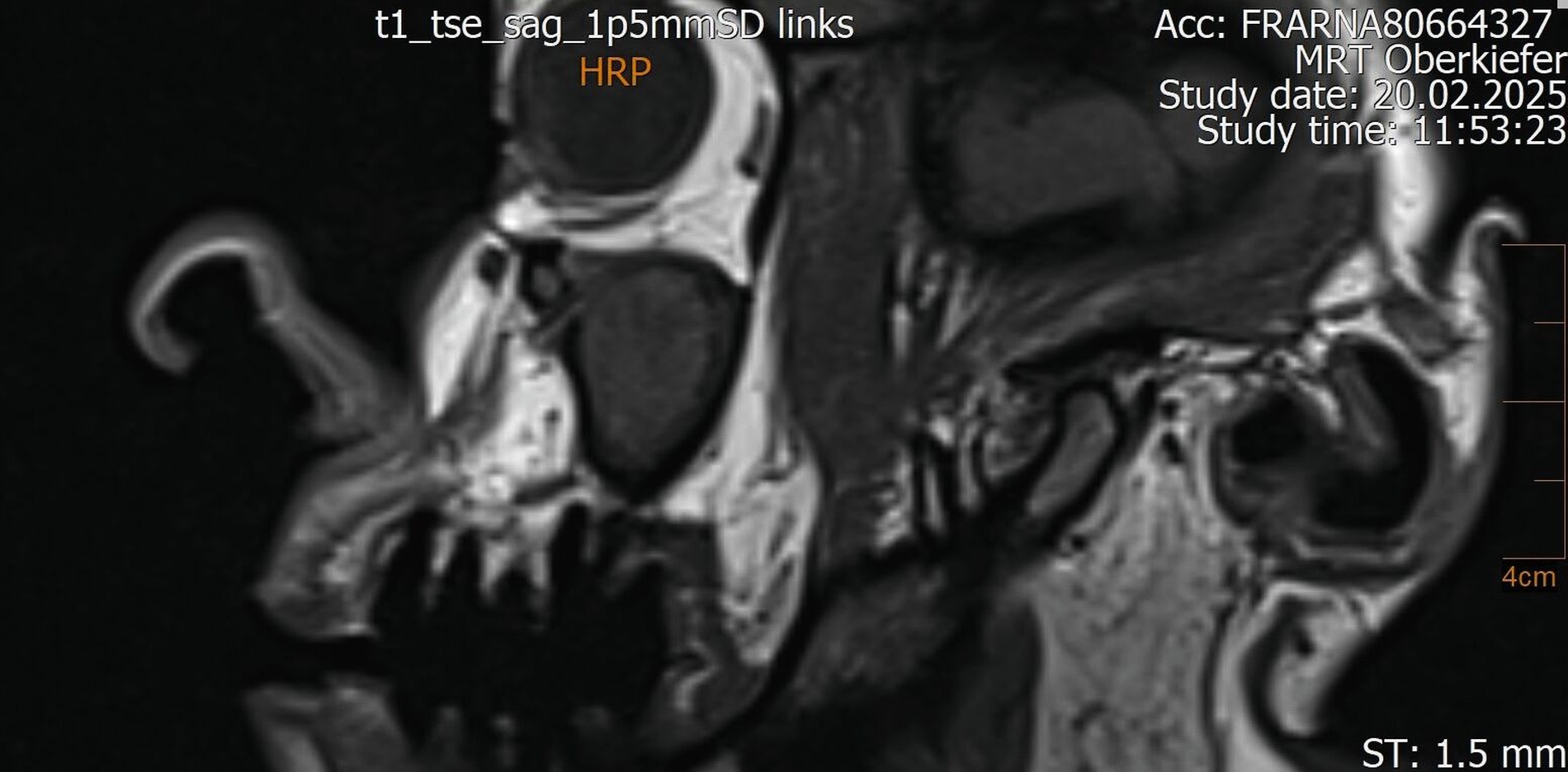
Im Februar 2022 stellte sich die 46-jährige Patientin nach Überweisung durch die Hauszahnärztin mit seit zwei Wochen bestehenden Schmerzen im linken Oberkiefer in einer MKG-chirurgischen Praxis vor. Klinisch und radiologisch zeigten sich eine tiefe Karies an Zahn 26 mit apikaler Ostitis und enger Beziehung zur Kieferhöhle (Abbildung 1) sowie der devitale Zahn 27.
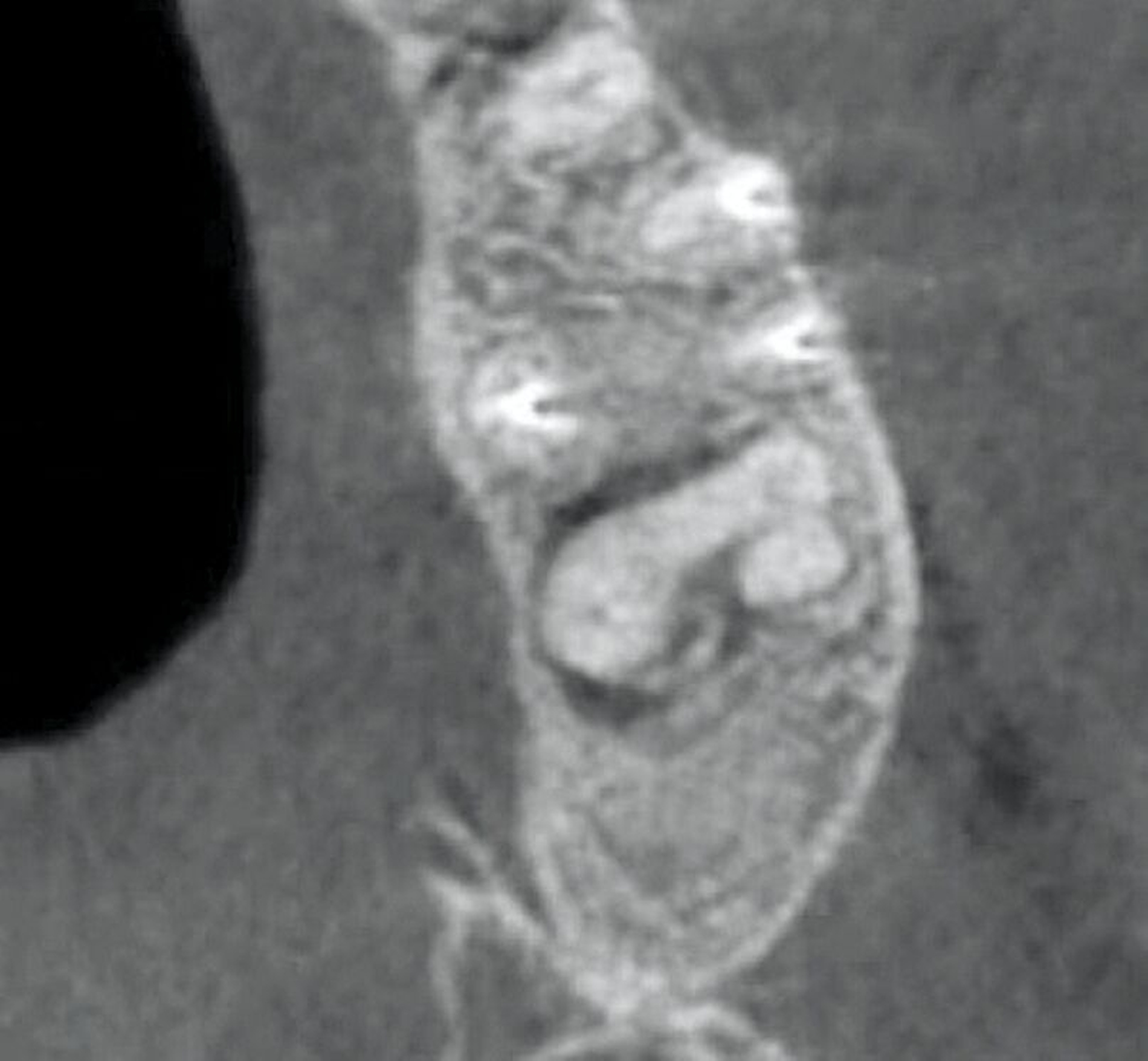
Zwischen März und Oktober 2022 erfolgten dort eine Wurzelkanalbehandlung und später eine Revision an Zahn 26 sowie eine Trepanation von Zahn 27 mit Abfluss von putridem Sekret. Trotz dieser Maßnahmen blieben die Beschwerden bestehen. Ein DVT im Mai 2023 zeigte eine zystische Läsion in regio 27 mit Verdacht auf Kieferhöhlenperforation und bereits vollständiger Verschattung der linken Kieferhöhle (Abbildung 2). Zahn 27 wurde daraufhin extrahiert.
In der Folge wurde leider die weiterhin bestehende Symptomatik als rhinogen fehlinterpretiert, da die odontogenen Foki als behandelt galten. Ab August 2023 entwickelte die Patientin eine einseitige, linksbetonte Pansinusitis mit persistierender Sekretion, Kopfschmerzen und zunehmender Abgeschlagenheit. Wiederholte HNO-ärztliche Behandlungen mit Clindamycin und Kortison führten zu einer nur vorübergehenden Besserung. Die weiterhin bestehende odontogene Ursache blieb unerkannt.
Ein im Februar 2024 durch die HNO veranlasstes DVT bestätigte erneut eine einseitige Pansinusitis (Abbildung 3), ohne den dentalen Bezug zu erfassen. Daraufhin wurde eine chirurgische Sanierung der Nasennebenhöhlen geplant, die jedoch aus Kapazitätsgründen des Krankenhauses nicht durchgeführt wurde. Im Januar 2025 kam es schließlich zu einer akuten Verschlechterung mit starken Schmerzen.
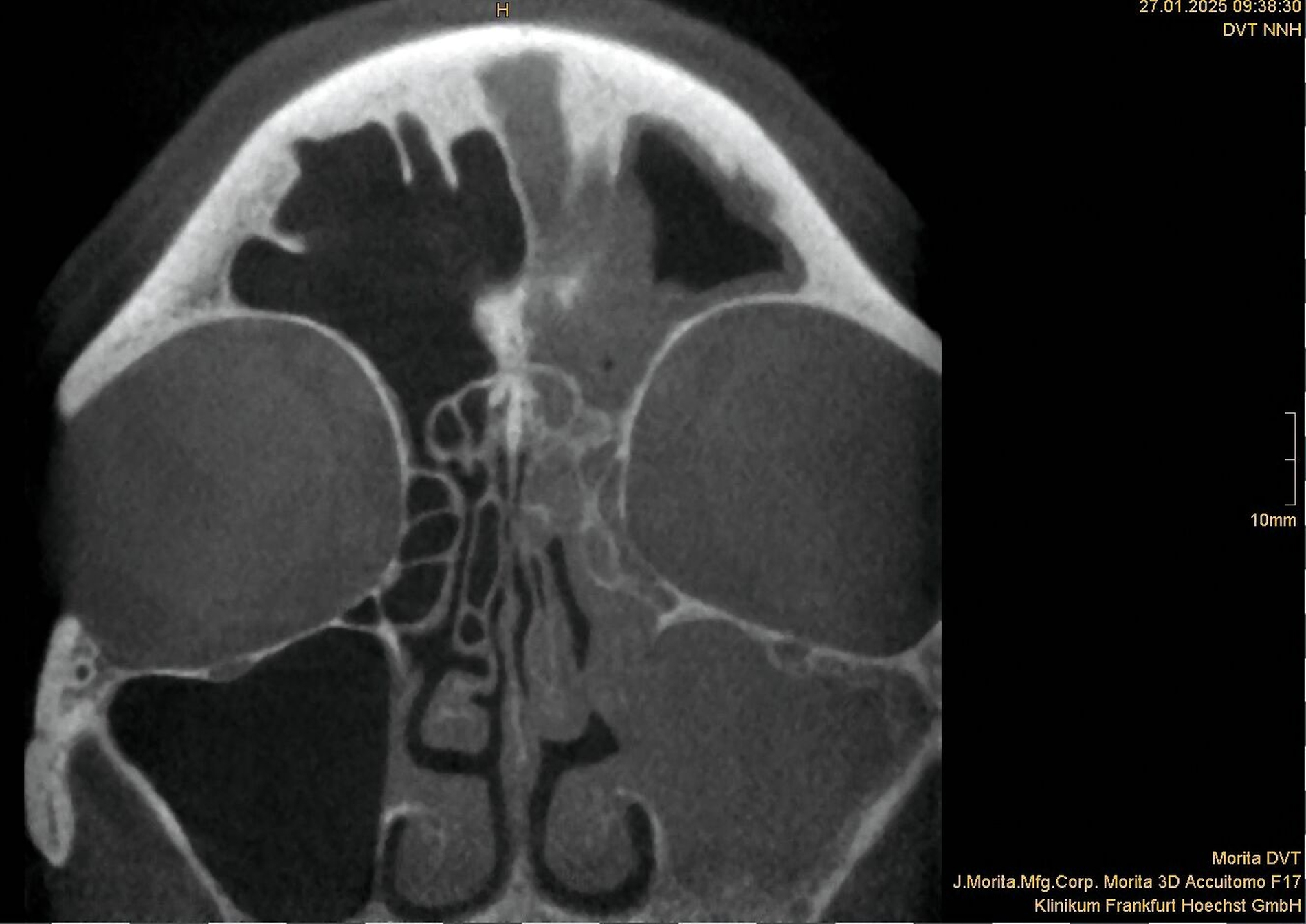
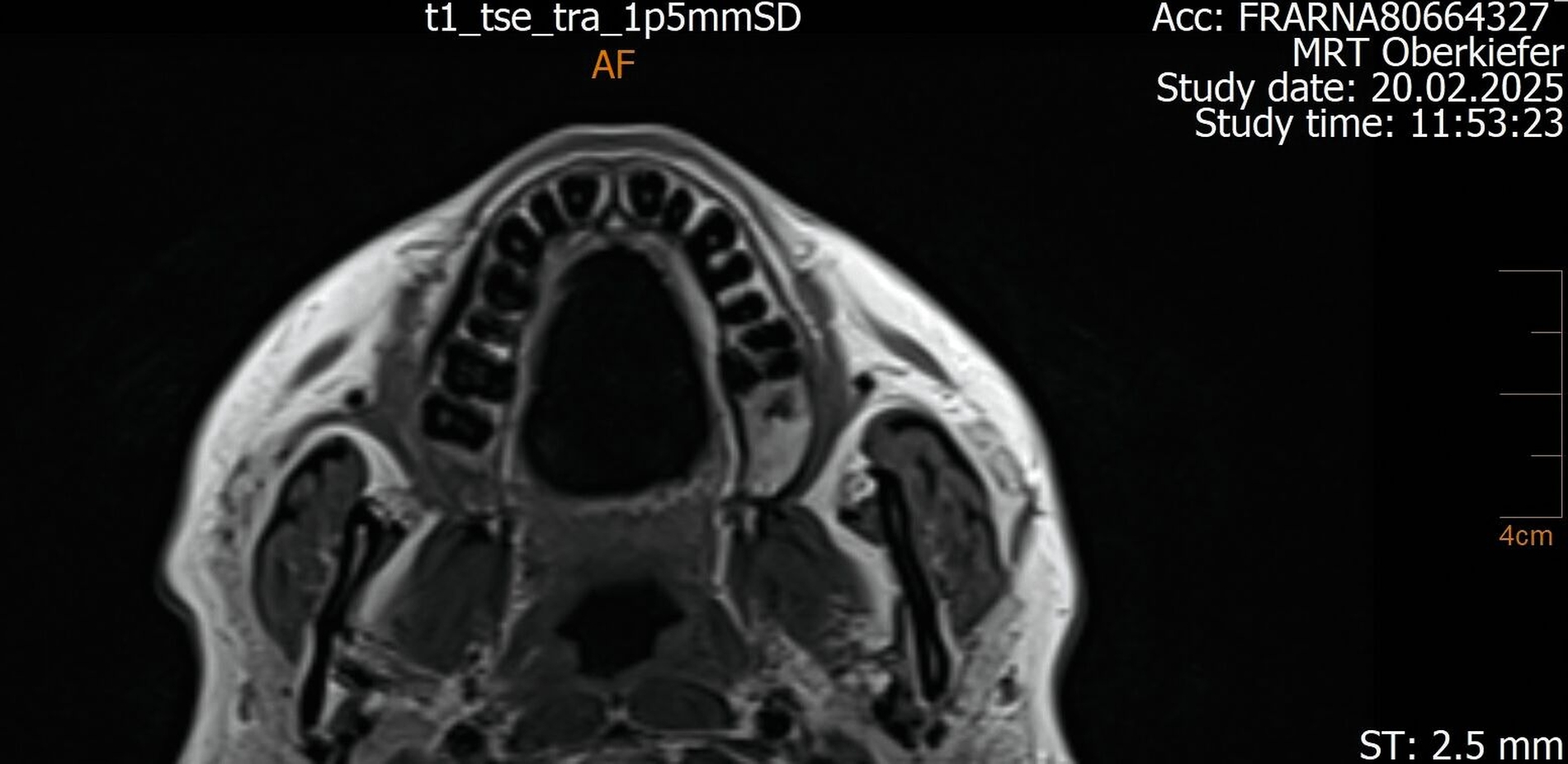
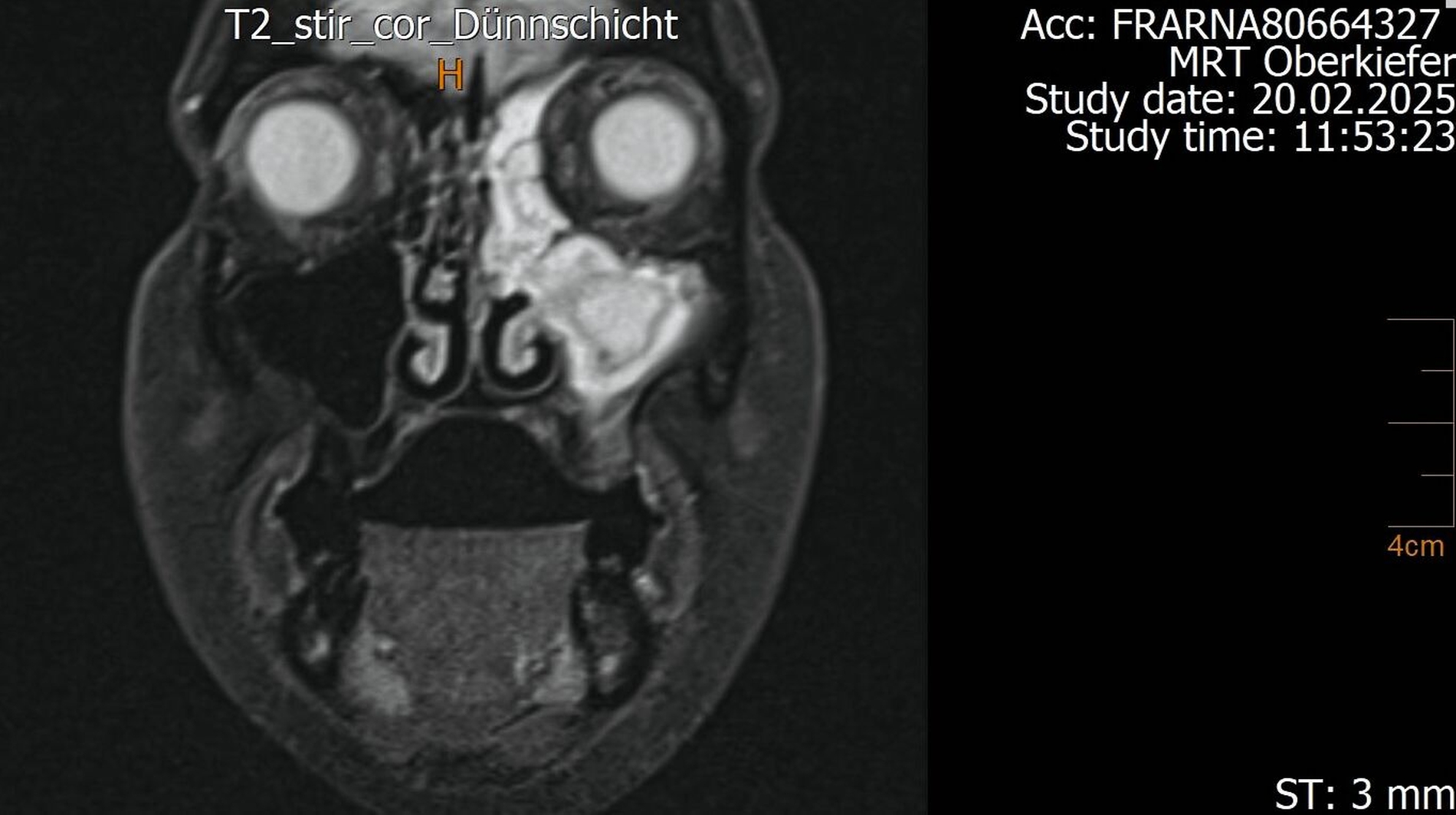
Der Wendepunkt erfolgte schließlich im Februar 2025 im Rahmen einer Kontrolluntersuchung bei der Hauszahnärztin. Diese nahm die langjährige Beschwerdesymptomatik ernst und veranlasste eine MRT-Untersuchung am Deutschen Zentrum für Dentaldiagnostik (DZD). Die MRT-Bildgebung ergab eine chronische Osteomyelitis im Bereich der Extraktionsregion von Zahn 27 sowie eine ausgeprägte apikale Ostitis an Zahn 26 mit vollständiger Verschattung der linken Kieferhöhle und Ausdehnung der Entzündung ins Siebbein und in die Stirnhöhle. Auch konnte durch den befundenden Radiologen eine interradikuläre Fistelung an Zahn 26 erkannt werden, weshalb die Sinusitis als odontogen eingestuft wurde (Abbildungen 4 bis 7).
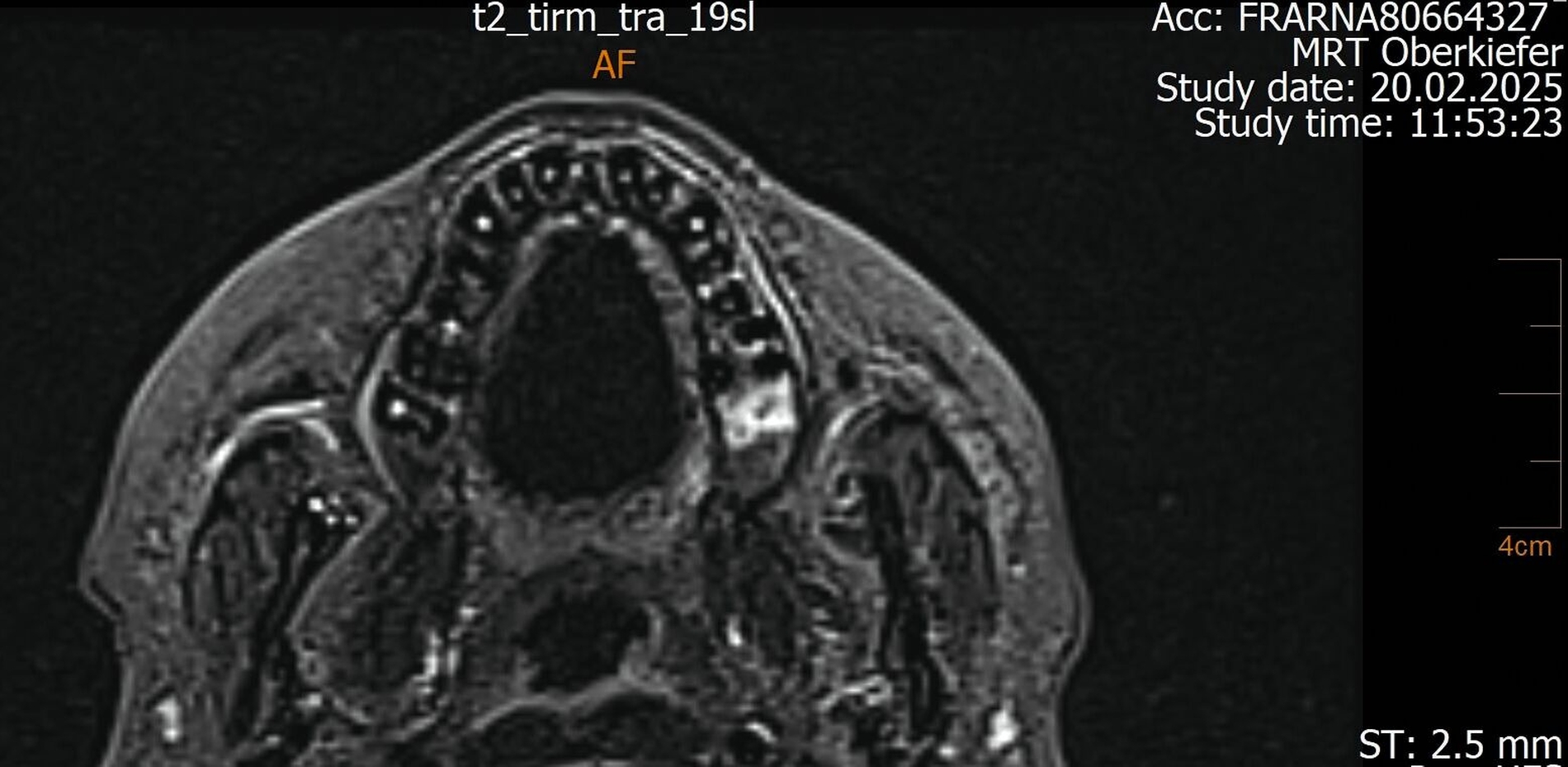
Therapie
Die Patientin stellte sich daraufhin am 27. Februar 2025 initiativ bei uns vor. Nach Sichtung der Unterlagen erfolgten die OP-Aufklärung und die zeitnahe Terminierung der Operation. Am 10. März 2025 folgte dann die chirurgische Sanierung unter stationären Bedingungen. Wir entschieden uns für die Extraktion von Zahn 26, der aufgrund der interradikulären Fistelung nicht erhaltungswürdig war und den Fokus für die chronische Sinusitis und die Beschwerden darstellte.
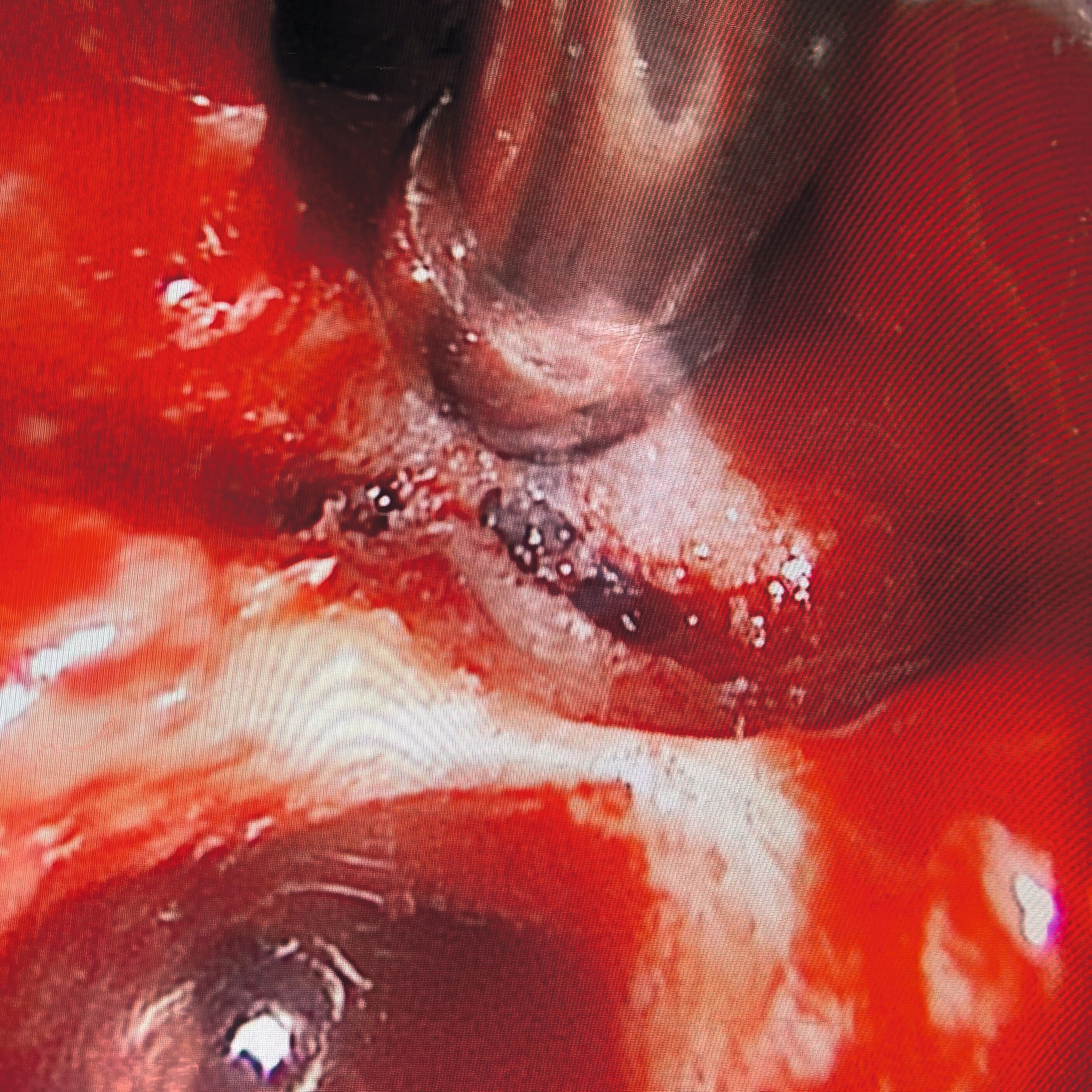
Intraoperativ zeigte sich die interradikuläre Perforation im Sinne eines Fistelgangs zur linken Kieferhöhle (Abb. 8), die bereits präoperativ in der alio loco durchgeführten MRT-Bildgebung erkennbar gewesen war (Abb. 7). Zudem entfernten wir das Empyem und die pathologisch veränderte Schleimhaut sowie das Narbengewebe unter Schonung der noch intakten Schneider’schen Membran.
Zur Kieferhöhle wählten wir einen fazialen Zugang mit temporärer Knochenfensterentnahme, da eine direkte Sanierung des odontogenen Fisteltrakts, das Abtragen der narbigen Schleimhautanteile und die simultane Zahnentfernung sowie der Verschluss der daraus resultierenden Mund-Antrum-Verbindung so in einer Sitzung sicher erreichbar waren. Der Knochendeckel wurde mittels Microosteosyntheseplatte repositioniert. Ein transnasaler Ballonkatheter wurde wenige Tage zur Tamponade und Blutstillung belassen, um einen Hämatosinus zu vermeiden.
Heilungsverlauf
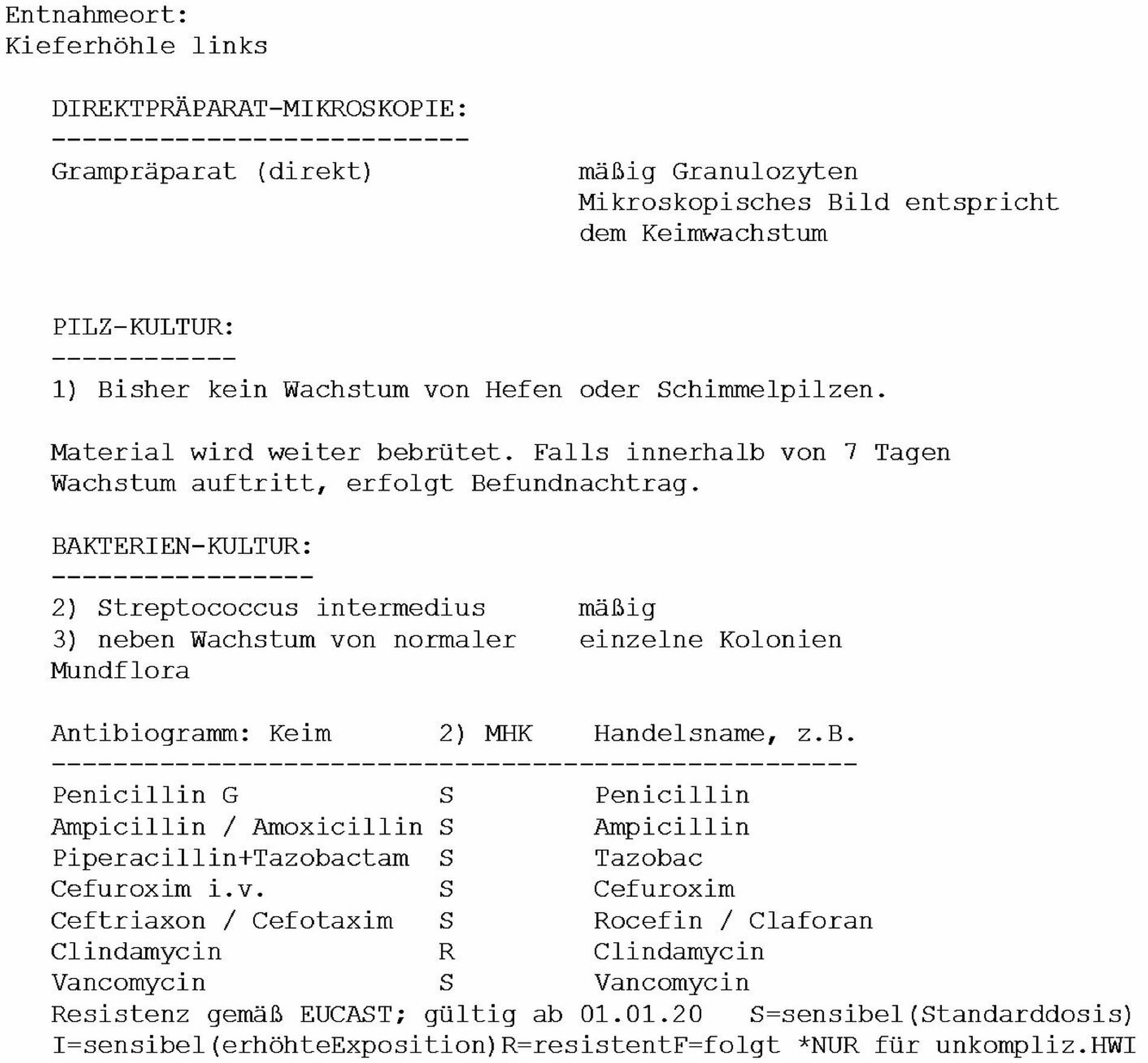
Etwa eine Woche postoperativ entwickelte sich eine eitrige Sekretion im Bereich der Naht auf dem Alveolarkamm regio 26. Die mikrobiologische Untersuchung (siehe Antibiogramm, Abbildung 9) zeigte beim dominierenden Streptococcus intermedius eine Resistenz gegenüber Clindamycin. Da die Patientin eine Penicillinallergie angab, wurde nach eingehender Abwägung eine zehntägige Therapie mit Cefuroxim (Cefurax 500 mg) eingeleitet, die zu einer klinischen Ausheilung und Beschwerdefreiheit führte.
Diskussion
Odontogene versus rhinogene Sinusitis
Dieser Fall demonstriert die Herausforderungen und Schwierigkeiten bei der Differenzierung zwischen odontogener und rhinogener Sinusitis. Trotz dentalem Fokus dominierte die Einschätzung einer primär rhinogenen Ursache für die Sinusitis – nach vermeintlicher Sanierung des odontogenen Fokus. Die recht kleine Fistelung war in den konventionellen Röntgenaufnahmen nicht eindeutig erkennbar, der odontogene Fokus wurde durch die MRT-Aufnahme hervorgehoben.
Die Problematik der Differenzierung zwischen odontogenen und rhinogenen Sinusitiden wird in der Literatur häufig beschrieben: Bis zu 40 Prozent der einseitigen Sinusitiden sind odontogen bedingt, werden aber in bis zu 30 Prozent der Fälle initial falsch klassifiziert [Little et al., 2018]. Die charakteristischen Unterschiede zeigen sich klinisch und radiologisch: Odontogene Sinusitiden präsentieren sich typischerweise unilateral, zeigen eine enge räumliche Beziehung zu dentogenen Infektionsherden und sprechen schlecht auf alleinige antibiotische Monotherapien an, weshalb eine chirurgische Intervention nötig ist [Workman et al., 2018]. Im Unterschied dazu sind rhinogene Formen oft bilateral und mit vollständiger nasaler Obstruktion assoziiert [Raj et al., 2022].
Die diagnostische Abklärung odontogener Sinusitiden erfolgt primär klinisch und mittels digitaler Volumentomografie (DVT). Letztere bietet durch ihre hohe Auflösung im dentalen Bereich klare Vorteile zur Beurteilung endodontischer, parodontaler und ossärer Strukturen sowie zur Identifikation möglicher oroantraler Verbindungen.
In speziellen Fällen kann ergänzend eine MRT sinnvoll sein – etwa bei unklarer Symptomatik, bei Verdacht auf Weichteilbeteiligung, bei einem chronisch-rezidivierenden Verlauf oder bei unzureichender Abgrenzbarkeit im DVT. Im vorgestellten Fall ermöglichte die MRT den Nachweis des interradikulären Fistelgangs zur Kieferhöhle und damit die korrekte Zuordnung des Entzündungsfokus.
Die MRT in der dentalen Diagnostik
Die Überlegenheit der MRT bei Weichteil- und Entzündungsdarstellung ist in der Zahnmedizin mittlerweile gut belegt. Aktuelle Studien zeigen, dass sich die MRT unter anderem gut zur Beurteilung von Schleimhautverdickungen eignet, was für die Diagnostik von Sinusitiden entscheidend sein kann [Parker et al., 2024]. Im Bereich der odontogenen Infektionen erreicht die MRT eine bemerkenswerte diagnostische Genauigkeit mit einer Sensitivität von 0,95 und einer Spezifität von 0,84 [Heikkinen et al., 2023]. Besonders wertvoll ist die Möglichkeit, Knochenmarködeme strahlungsfrei darzustellen, was die Früherkennung von Osteomyelitiden revolutioniert hat [Lee et al., 2016].
Neue Forschungsarbeiten demonstrieren den besonderen Nutzen der dentalen MRT bei der Differenzierung zwischen Granulomen und periapikalen Zysten. Diese Unterscheidung ist klinisch relevant, da sie einen direkten Einfluss auf die Therapieplanung und Prognoseabschätzung endodontischer Behandlungen hat [Juerchott et al., 2018]. Auch für die Beurteilung parodontaler Gewebe und des Heilungsverlaufs nach Parodontitistherapien hat sich die MRT als wertvolles Instrument erwiesen [Schara et al., 2009]. Zur Verbesserung der Implantatplanung gibt es bereits Ansätze mittels MRT als Alternative zum CT, dabei schnitt dieses ähnlich wie das CT ab, untersucht wurde die Genauigkeit der Vermessung des Kieferknochens [Aguiar et al., 2008].
Um die besonders strahlungssensible Gruppe der Kinder besser zu schützen, gibt es bereits Studien, die zeigen, dass eine kieferorthopädische Behandlungsplanung mithilfe der dentalen MRT möglich ist. Hochauflösende isotrope MRT-Datensätze können in laterale Fernröntgenbilder umgewandelt werden und ermöglichen dabei zuverlässige Messungen, die mit den herkömmlichen Messwerten aus klassischen Röntgenaufnahmen eine hohe Übereinstimmung zeigen [Heil et al., 2017].
Die Weiterentwicklung der MRT-Technologie eröffnet ständig neue Anwendungsgebiete. So ermöglichen moderne Hochfeldgeräte mittlerweile die Darstellung feinster anatomischer Strukturen im dentalen Bereich, funktionelle MRT-Untersuchungen geben zunehmend Aufschluss über Durchblutungsverhältnisse und Stoffwechselprozesse im Kieferknochen, im parodontalen Gewebe und in der Pulpa, was für unterschiedlichste Disziplinen der Zahnmedizin wertvoll ist.
Damit könnten die nicht-invasiven Verfahren zukünftig die Diagnostik von Pulpitiden und parodontalen Erkrankungen grundlegend verändern. Besonders wichtig ist der strahlungsfreie Charakter der MRT, der wiederholte Untersuchungen ohne Strahlenbelastung ermöglicht. Dies ist nicht nur aus Gründen der Strahlungshygiene bedeutsam, sondern erlaubt auch ein konsequenteres Monitoring von chronischen Erkrankungen und Therapieverläufen.
Fazit: Die Kombination aus hervorragender Weichteildarstellung, fehlender Strahlenbelastung und zunehmender Verfügbarkeit macht die dentale MRT zu einem heute bereits unverzichtbaren Werkzeug in der modernen zahnärztlichen Diagnostik.
Odontogene Infektionen und Resistenzbildung
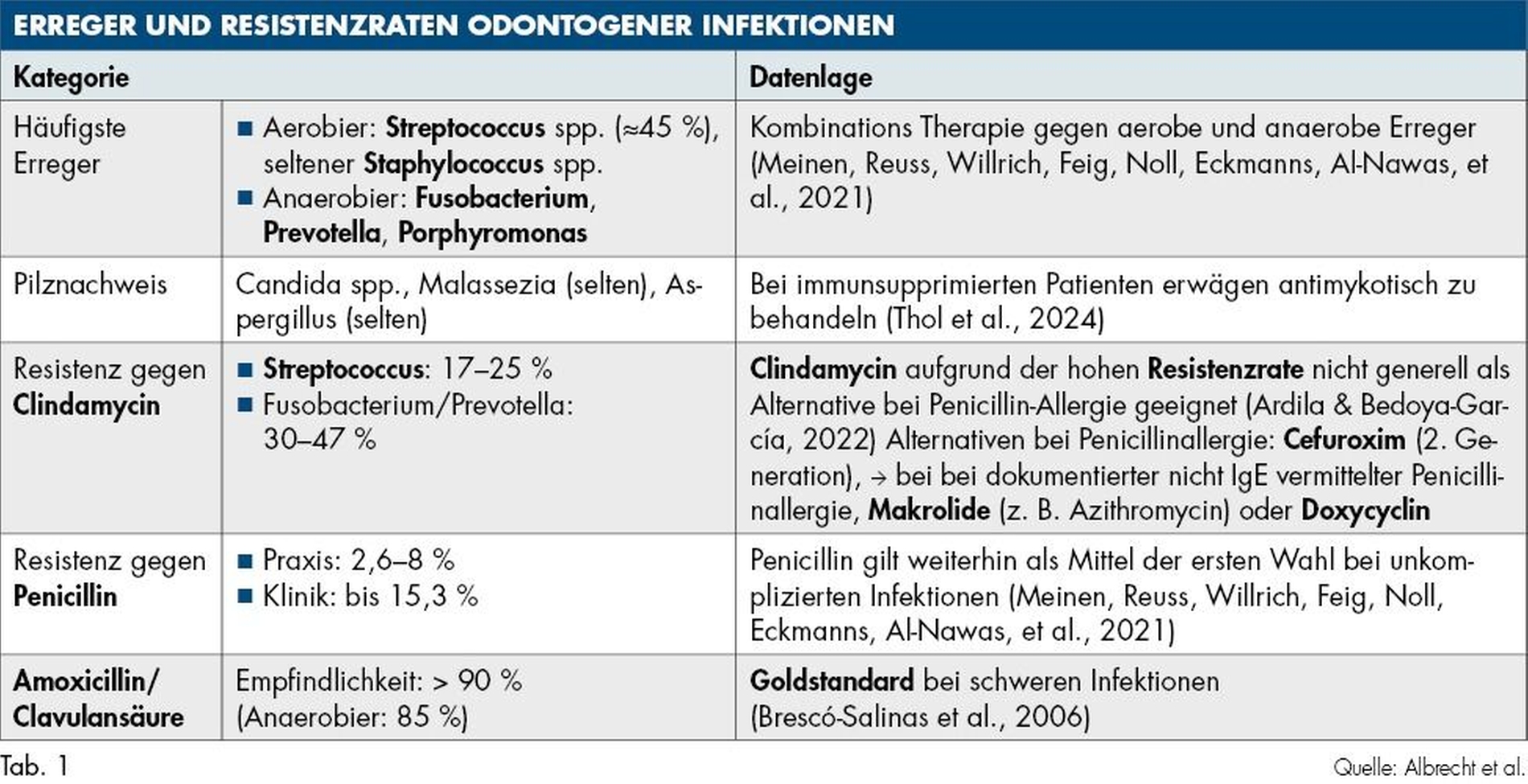
Odontogene Infektionen gehören zu den häufigsten Ursachen für Kopf-Hals-Infektionen und werden regelmäßig mit Antibiotika behandelt. Sie weisen typischerweise ein polymikrobielles Erregerprofil auf, bei dem sowohl aerobe als auch anaerobe Bakterien nachweisbar sind. Zu den häufig isolierten Anaerobiern zählen Fusobacterium, Prevotella, Parvimonas und Porphyromonas, während unter den aeroben Erregern vor allem Streptococcus- und Staphylococcus-Spezies dominieren [Meinen et al., 2021]. Interessanterweise werden in einem signifikanten Anteil der Fälle auch Pilze wie Malassezia, Aspergillus und Candida nachgewiesen, die wohl als Begleitbefund einzuordnen sind [Thol et al., 2024].
Aktuelle Studien zeigen hohe Resistenzraten gegenüber den häufig verwendeten Antibiotika: Clindamycin: 17–47 Prozent Resistenz bei Streptococcus, Fusobacterium, Prevotella; Metronidazol: 25,5 Prozent Resistenz bei Anaerobiern; Penicillin: 2,6–15,3 Prozent Resistenz bei Streptococcus, Staphylococcus [Ardila & Bedoya-García, 2022; Bigus et al., 2023; Heim et al., 2020; López-González et al., 2019; Meinen et al., 2021; Țenț et al., 2019; Thol et al., 2024; Vavro et al., 2024].
Die Resistenz gegen Penicillin und Aminopenicilline fällt mit 2 bis 15 Prozent zwar geringer aus, zeigt jedoch in Krankenhaussettings deutlich höhere Werte als in zahnärztlichen Praxen [Ardila & Bedoya-García, 2022; Brescó-Salinas et al., 2006; Meinen et al., 2021; Vavro et al., 2024). Gramnegative Bakterien und Anaerobier wie Prevotella und Bacteroides spp. zeigen zunehmend Resistenzen gegen multiple Antibiotika, darunter Penicillin, Erythromycin und Clindamycin [Ardila & Bedoya-García, 2022]. Amoxicillin/Clavulansäure erweist sich nach wie vor als eines der wirksamsten Antibiotika, da die meisten Isolate eine Empfindlichkeit aufweisen [Brescó Salinas et al., 2006; Brescó-Salinas et al., 2006; López-González et al., 2019].
Laut der S3-Leitlinie „Odontogene Infektionen“ sollte die kalkulierte Antibiose bei schweren Verläufen stets eine Kombination aus β-Lactam-Antibiotikum (zum Beispiel Amoxicillin/Clavulansäure) und Metronidazol berücksichtigen, um Anaerobier-Resistenzen zu umgehen. Bei Penicillinallergie wird Cefuroxim (2. Generation) als Alternative empfohlen, sofern keine Typ-I-Allergie vorliegt (AWMF, 2023). Es weist eine geringe Kreuzreaktivität von < 3 Prozent bei Penicillinallergikern auf, sofern keine Anaphylaxie auf Penicilline vorliegt. Damit gilt es als sichere Alternative bei Patienten mit Penicillinallergie mit nicht-IgE-vermittelten Reaktionen [Campagna et al., 2012].
Kritische Prüfung dokumentierter Penicillinallergien
Die Problematik unkritisch dokumentierter Penicillinallergien stellt im Zusammenhang mit der dargestellten fortschreitenden Resistenzbildung ein zunehmendes Problem in der medizinischen Versorgung dar. Aktuelle Studien zeigen, dass etwa 90 Prozent der Patienten, die als penicillinallergisch gelten, dieses Label zu Unrecht tragen [Al-Nawas et al., 2021; Luintel et al., 2025].
Diese Fehleinschätzung hat weitreichende Konsequenzen für die Therapieplanung und Patientenversorgung. Die Unterscheidung zwischen echten IgE-vermittelten allergischen Reaktionen und anderen Unverträglichkeitsreaktionen erweist sich in der Praxis bei der Anamneseerhebung oft als komplex. Viele dokumentierte „Allergien“ basieren auf unspezifischen Symptomen wie gastrointestinalen Beschwerden oder Hautausschlägen, die nicht zwangsläufig auf eine echte Allergie hindeuten [Banks et al., 2019]. Hier helfen strukturierte Ansätze wie der PEN-FAST-Score (Tabelle 2), das tatsächliche Allergierisiko besser einzuschätzen.
Eine Studie aus dem Jahr 2020 hat ein klinisches Entscheidungsmodell zur Penicillinallergie entwickelt und validiert, um Patienten mit einem niedrigen Risiko für Penicillinallergien zu identifizieren, die möglicherweise keine spezielle Hauttestung benötigen. Die Untersuchung wurde mit 622 Patienten aus Melbourne (Australien) durchgeführt, die eine Penicillinallergie angaben, und sich einem Allergietest unterzogen. Vier Merkmale, die mit einem positiven Testergebnis in Verbindung standen, wurden identifiziert: Penicillinallergie weniger als fünf Jahre her, Anaphylaxie/Angioödeme, schwere Hautreaktionen (SCAR) und ärztliche Behandlung während der Allergieepisode. Das Modell PEN-FAST zeigt, dass Patienten mit einem Score unter drei Punkten ein geringes Risiko für eine echte Penicillinallergie haben und keine formelle Testung benötigen. Der negative prädiktive Wert dieses Scores lag bei 96,3 Prozent.
Ein strukturiertes Vorgehen zur Überprüfung eines Verdachts auf Penicillinallergien sollte insbesondere immer dann durchgeführt werden, wenn eine chirurgische Intervention geplant ist oder wenn sich eine Behandlung – bei Verwendung eines alternativen Antibiotikums aufgrund des Verdachts auf Penicillinallergie – als therapierefraktär zeigt. Bei dringendem Verdacht können ein Hauttest, ein oraler Provokationstest oder eine spezifische IgE-Diagnostik erfolgen.
Die unnötige Vermeidung von Penicillinen führt häufig zur Verordnung von Breitspektrumantibiotika wie Clindamycin oder Fluorchinolonen. Dies zeigt sich in der überproportional häufigen Verordnung von Clindamycin durch deutsche Zahnärzte, die im Jahr 2012 bei 37,8 Prozent lag und bis 2021 auf 23,4 Prozent zurückging. Damit ist Clindamycin noch immer das am zweithäufigsten verordnete Antibiotikum [Albrecht et al., 2024].
Fazit für die Praxis
Eine einseitige Sinusitis ist häufig odontogenen Ursprungs – daher immer den dentoalveolären Bereich sorgfältig mit beurteilen und gegebenenfalls den dentalen Fokus sanieren.
Zur Diagnostik ist in der Regel ein DVT ausreichend; eine MRT ist nur bei therapierefraktären Verläufen oder bei Verdacht auf eine Weichteil- beziehungsweise Knochenbeteiligung sinnvoll.
Angegebene Penicillinallergien sollten kritisch hinterfragt werden, hier ist der FAST-PEN-Score ein sinnvolles, ergänzendes Tool.
Bei therapierefraktärem Verlauf kann ein Antibiogramm erstellt werden, um die Resistenzlage des dominierenden Keims zu bestimmen.
Wenn keine IgE-vermittelte Reaktion auf Penicillin vorliegt, können Cephalosporine der zweiten Generation meist sicher eingesetzt werden.
Clindamycin sollte aufgrund der hohen Resistenzraten nur zurückhaltend oder gezielt nach Antibiogramm verwendet werden.
Die kritische Überprüfung dokumentierter Penicillinallergien sollte fester Bestandteil der klinischen Praxis sein. Durch den Einsatz validierter Scores, durch eine gezielte Anamnese und Diagnostik (beispielsweise mittels Antibiogramm) können unnötige Therapieeinschränkungen vermieden und die Antibiotikaselektion kann optimiert werden. Bei dokumentierter, nicht IgE-vermittelter Penicillinreaktion kann Cefuroxim als Alternative verwendet werden, bei einer echten Sofortreaktion sollte ein Allergologe aufgesucht werden. Dies ist insbesondere in der zahnärztlichen Versorgung von Bedeutung, wo Penicilline nach wie vor zu den wirksamsten und sichersten Therapeutika bei odontogenen Infektionen zählen.
Literaturliste
Aguiar, M. F., Marques, A. P., Carvalho, A. C. P., & Cavalcanti, M. G. P. (2008). Accuracy of magnetic resonance imaging compared with computed tomography for implant planning. Clinical Oral Implants Research, 19(4), 362-365. doi.orghttps://doi.org/10.1111/j.1600-0501.2007.01490.x.
Al-Nawas, B., Eickholz, P., & Hülsmann, M. (2021). Antibiotika in der Zahnmedizin. Quintessenz Verlag. books.google.de/books.
Albrecht, H., Schiegnitz, E., & Halling, F. (2024). Facts and trends in dental antibiotic and analgesic prescriptions in Germany, 2012–2021. Clinical Oral Investigations, 28(1), 100.
Ardila, C., & Bedoya-García, J.-A. (2022). Antimicrobial resistance in patients with odontogenic infections: A systematic scoping review of prospective and experimental studies. Journal of Clinical and Experimental Dentistry, 14. doi.org/10.4317/jced.59830.
AWMF-S3-Leitlinie (2023). Odontogene Infektionen. Registernummer: 007-006.
Banks, T., Tucker, M., & Macy, E. (2019). Evaluating Penicillin Allergies Without Skin Testing. Current Allergy and Asthma Reports, 19, 1-7. doi.org/10.1007/s11882-019-0854-6.
Bigus, S., Russmüller, G., Starzengruber, P., Reitter, H., & Sacher, C. (2023). Antibiotic resistance of the bacterial spectrum of deep space head and neck infections in oral and maxillofacial surgery — a retrospective study. Clinical Oral Investigations, 27, 4687-4693. doi.org/10.1007/s00784-023-05095-y.
Brescó Salinas, M., Costa Riu, N., Berini Aytés, L., & Gay Escoda, C. (2006). Antibiotic susceptibility of the bacteria causing odontogenic infections.
Brescó-Salinas, M., Costa-Riu, N., Berini-Aytés, L., & Gay-Escoda, C. (2006). Antibiotic susceptibility of the bacteria causing odontogenic infections. Medicina oral, patologia oral y cirugia bucal, 11 1.
Campagna, J. D., Bond, M. C., Schabelman, E., & Hayes, B. D. (2012). The Use of Cephalosporins in Penicillin-allergic Patients: A Literature Review. The Journal of Emergency Medicine, 42(5), 612-620. doi.orghttps://doi.org/10.1016/j.jemermed.2011.05.035.
Heikkinen, J., Jokihaka, V., Nurminen, J., Jussila, V., Velhonoja, J., Irjala, H., Soukka, T., Happonen, T., Järnstedt, J., Nyman, M., Mattila, K., & Hirvonen, J. (2023). MRI of odontogenic maxillofacial infections: diagnostic accuracy and reliability. Oral Radiol, 39(2), 364-371. doi.org/10.1007/s11282-022-00646-7.
Heil, A., Lazo Gonzalez, E., Hilgenfeld, T., Kickingereder, P., Bendszus, M., Heiland, S., Ozga, A.-K., Sommer, A., Lux, C. J., & Zingler, S. (2017). Lateral cephalometric analysis for treatment planning in orthodontics based on MRI compared with radiographs: A feasibility study in children and adolescents. PLOS ONE, 12(3), e0174524. doi.org/10.1371/journal.pone.0174524.
Heim, N., Jürgensen, B., Kramer, F., & Wiedemeyer, V. (2020). Mapping the microbiological diversity of odontogenic abscess: are we using the right drugs? Clinical Oral Investigations, 25, 187-193. doi.org/10.1007/s00784-020-03350-0.
Juerchott, A., Pfefferle, T., Flechtenmacher, C., Mente, J., Bendszus, M., Heiland, S., & Hilgenfeld, T. (2018). Differentiation of periapical granulomas and cysts by using dental MRI: a pilot study. International Journal of Oral Science, 10(2), 17. doi.org/10.1038/s41368-018-0017-y.
Lee, Y. J., Sadigh, S., Mankad, K., Kapse, N., & Rajeswaran, G. (2016). The imaging of osteomyelitis. Quant Imaging Med Surg, 6(2), 184-198. doi.org/10.21037/qims.2016.04.01.
Little, R. E., Long, C. M., Loehrl, T. A., & Poetker, D. M. (2018). Odontogenic sinusitis: A review of the current literature. Laryngoscope Investig Otolaryngol, 3(2), 110-114. doi.org/10.1002/lio2.147.
López-González, E., Vitales-Noyola, M., González-Amaro, A., Méndez-González, V., Hidalgo-Hurtado, A., Rodríguez-Flores, R., & Pozos-Guillen, A. (2019). Aerobic and anaerobic microorganisms and antibiotic sensitivity of odontogenic maxillofacial infections. Odontology, 107, 409-417. doi.org/10.1007/s10266-019-00414-w.
Luintel, A., Healy, J., Blank, M., Luintel, A., Dryden, S., Das, A., Darzi, A., & Cooke, G. (2025). The Global Prevalence of Reported Penicillin Allergy: A Systematic Review and Meta-Analysis. The Journal of infection, 106429. doi.org/10.1016/j.jinf.2025.106429.
Meinen, A., Reuss, A., Willrich, N., Feig, M., Noll, I., Eckmanns, T., Al-Nawas, B., & Markwart, R. (2021). Antimicrobial Resistance and the Spectrum of Pathogens in Dental and Oral-Maxillofacial Infections in Hospitals and Dental Practices in Germany [Original Research]. Frontiers in Microbiology, Volume 12 - 2021. doi.org/10.3389/fmicb.2021.676108.
Meinen, A., Reuss, A., Willrich, N., Feig, M., Noll, I., Eckmanns, T., Al‐Nawas, B., & Markwart, R. (2021). Antimicrobial Resistance and the Spectrum of Pathogens in Dental and Oral-Maxillofacial Infections in Hospitals and Dental Practices in Germany. Frontiers in Microbiology, 12. doi.org/10.3389/fmicb.2021.676108.
Parker, M., Beyea, S., Rioux, J., King, B., Abdolell, M., Reeve, S., Lieuwen, B., Bowen, C., & Volders, D. (2024). 0.5T MRI as a competitor to CT for sinus imaging. Scientific Reports, 14(1), 31774. doi.org/10.1038/s41598-024-81958-y.
Raj, G., Raj, M., & Loh, J. S. P. (2022). Pathophysiology and clinical presentation of odontogenic maxillary sinusitis. Dentistry Review, 2(2), 100044. doi.orghttps://doi.org/10.1016/j.dentre.2022.100044.
Schara, R., Sersa, I., & Skaleric, U. (2009). T1 relaxation time and magnetic resonance imaging of inflamed gingival tissue. Dentomaxillofac Radiol, 38(4), 216-223. doi.org/10.1259/dmfr/75262837.
Țenț, P., Juncar, R., Onișor, F., Bran, S., Haranguș, A., & Juncar, M. (2019). The pathogenic microbial flora and its antibiotic susceptibility pattern in odontogenic infections. Drug Metabolism Reviews, 51, 340-355. doi.org/10.1080/03602532.2019.1602630.
Thol, F., Warwas, F., Spuck, N., Kramer, F.-J., & Heim, N. (2024). Microbial spectrum and resistance of odontogenic abscesses - microbiological analysis using next generation sequencing. Clinical Oral Investigations, 29. doi.org/10.1007/s00784-024-06097-0.
Trubiano, J., Vogrin, S., Chua, K., Bourke, J., Yun, J., Douglas, A., Stone, C., Yu, R., Groenendijk, L., Holmes, N., & Phillips, E. (2020). Development and Validation of a Penicillin Allergy Clinical Decision Rule. JAMA internal medicine. doi.org/10.1001/jamainternmed.2020.0403.
Vavro, M., Dvoranova, B., Czako, L., Simko, K., & Gális, B. (2024). Antibiotic susceptibility of orofacial infections in Bratislava: a 10-year retrospective study. Clinical Oral Investigations, 28. doi.org/10.1007/s00784-024-05937-3.
Workman, A. D., Granquist, E. J., & Adappa, N. D. (2018). Odontogenic sinusitis: developments in diagnosis, microbiology, and treatment. Curr Opin Otolaryngol Head Neck Surg, 26(1), 27-33. doi.org/10.1097/moo.0000000000000430.