Wie sicher sind zahnärztliche Lokalanästhetika?
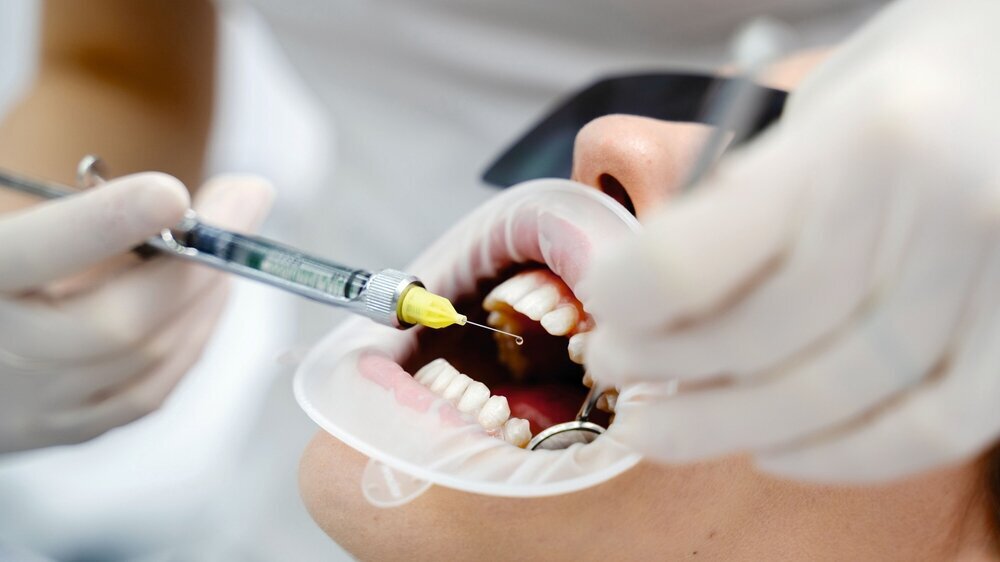
Lokalanästhetika sind ein unverzichtbarer Bestandteil der modernen Zahnmedizin. In Deutschland erhielten 2023 von 100 Patienten im Durchschnitt 16 Patienten eine Leitungs- und 38 eine Infiltrationsanästhesie [KZBV, 2024]. Man geht davon aus, dass hierzulande jährlich etwa 70 Millionen Injektionen zur Lokalanästhesie bei zahnmedizinischen Eingriffen durchgeführt werden.
Insgesamt ist die Komplikationsrate mit 4,5 Prozent bei örtlichen Betäubungen sehr niedrig, sie fällt aber bei Risikopatienten (zum Beispiel Multimedikation) mit 5,7 Prozent signifikant höher aus. Allerdings bestehen die meisten Komplikationen nur vorübergehend und erfordern keine spezielle Therapie [Daubländer et al., 1997].
Betrachtet man die Wirkstoffe, die zur zahnärztlichen Anästhesie verwendet werden, so fällt auf, dass in Deutschland fast ausschließlich Articain (Marktanteil 97 Prozent) eingesetzt wird. Der Anteil der Zubereitungen mit einem Adrenalinzusatz von 1:100.000 liegt bei etwa 44 Prozent, bei der Adrenalinkonzentration 1:200.000 sind es etwa 51 Prozent. Adrenalinfreie Zubereitungen spielen mit einem Anteil von drei Prozent nur eine sehr untergeordnete Rolle [Halling et al., 2021].
Wie bei jedem Arzneimittel besteht auch bei Lokalanästhetika die Möglichkeit einer Unverträglichkeit. Obwohl davon auszugehen ist, dass etwa acht Prozent der Bevölkerung über Arzneimittelunverträglichkeiten berichten [Sousa-Pinto et al., 2017], sind diesbezügliche Angaben bei Lokalanästhetika sehr rar.
In der Studie von Daubländer und Mitarbeitern wird die Häufigkeit allergischer Reaktionen bei 2.731 Patienten mit weniger als einem Prozent angegeben. Dabei wird jedoch darauf verwiesen, dass psychogene Reaktionen auch Allergien vortäuschen können [Daubländer et al., 1997]. Somit erscheint es sinnvoll, die möglichen Unverträglichkeiten und deren Häufigkeit bei zahnärztlichen Lokalanästhetika einmal näher zu beleuchten. Dabei ist es wichtig, die möglichen Wirkstoffe, die bei einer Lokalanästhesie appliziert werden, nämlich Articain und die Konservierungsstoffe Sulfit (meist Natriumbisulfit) und Methylparaben, getrennt zu betrachten.
Allergische Hypersensitivitätsreaktionen bei Articain
Unerwünschte Arzneimittelwirkungen (UAW, „adverse drug reactions“ [ADR], umgangssprachlich „Nebenwirkung“) sind Wirkungen, die aus den pharmakologischen Effekten des Arzneimittels resultieren. UAW werden in pharmakologisch bedingte unerwünschte Arzneimittelwirkungen („Typ A“) und unerwünschte Arzneimittelwirkungen aufgrund von Hypersensitivität („Typ B“) unterteilt [Doña et al., 2014].
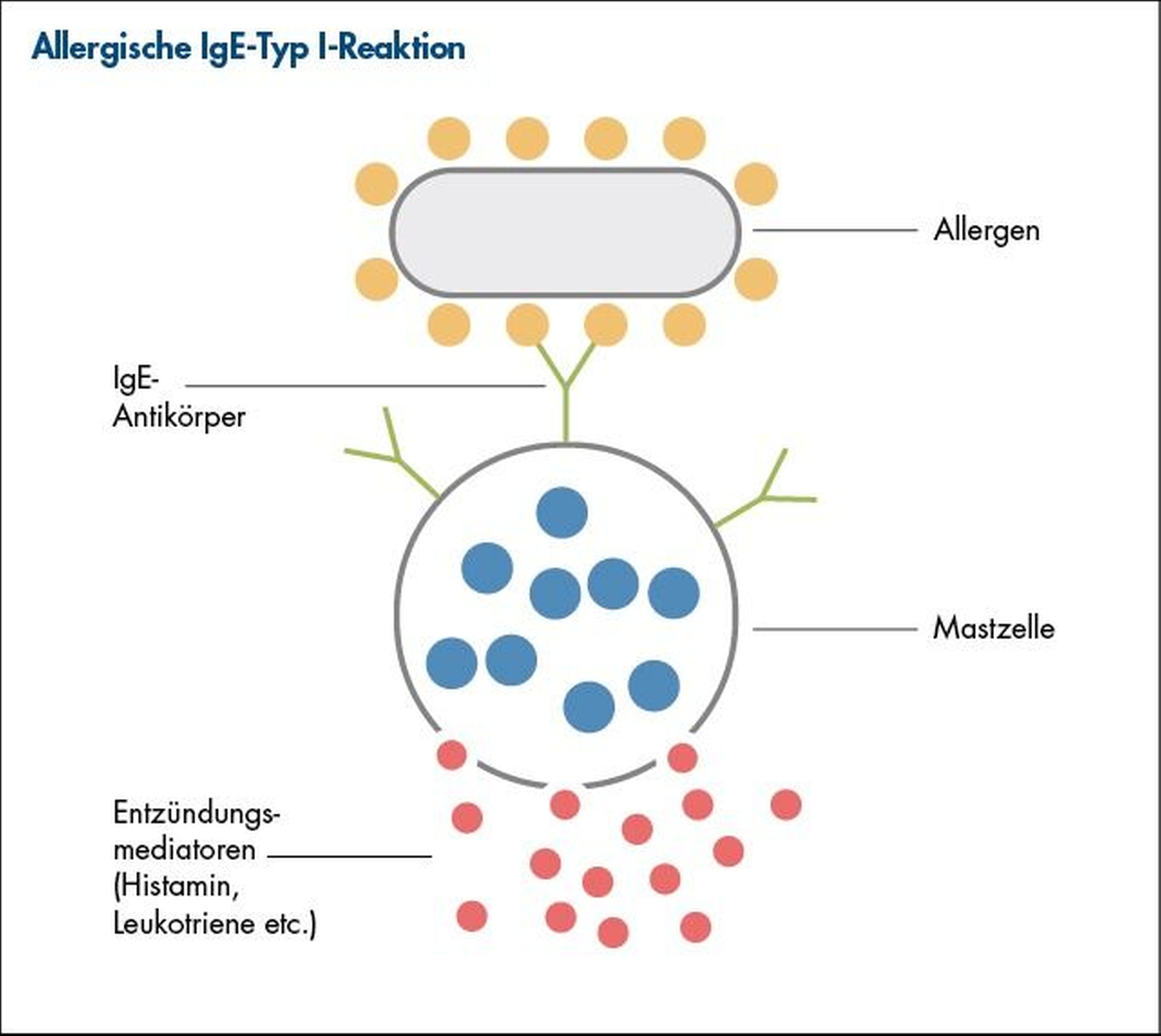
Ein bekanntes Typ-A-Beispiel sind Arzneimittel-induzierte Leberschäden, die zum Beispiel als Folge einer Paracetamol-Überdosierung auftreten [Athbhaiya et al., 2026]. Typ-B-Reaktionen werden ab Überschreitung einer geringen Schwellendosis in der Regel dosisunabhängig wahrgenommen [Böhm et al., 2018]. Die klassischen allergischen Hypersensitivitätsreaktionen werden in vier Typen unterteilt, wobei Typ I (Sofortreaktion mit Auftreten < 1 h nach Exposition) (Abbildung 1) und Typ IV (Spätreaktion mit Auftreten > 1 h nach Exposition) die am häufigsten auftretenden Formen sind [Coombs und Gell, 1968].
Die Typ-I-Reaktion wird über Immunglobulin E (IgE)-Antikörper vermittelt, die bei Allergenexposition Mastzellen und basophile Granulozyten zur Sekretion von Entzündungsmediatoren (zum Beispiel Histamin, Prostaglandine et cetera) anregen (Abbildung 1). Dies geschieht meist innerhalb weniger Minuten. Die Ausprägungsformen dieser Erkrankung sind urtikarielle Exantheme, Angioödeme, allergisches Asthma bronchiale, allergische Rhinokonjunktivitis und Anaphylaxie. Voraussetzung für eine Typ-I-Allergie ist ein vorher erfolgter Erstkontakt mit dem Allergen, der in der Regel symptomlos verläuft und als Sensibilisierung bezeichnet wird.
Die Typ-IV-Reaktion ist eine Form der Allergie, die zellulär durch sensibilisierte T-Lymphozyten vermittelt wird. Sie ist unabhängig von einer Antikörperbildung. Je nach den beteiligten Subgruppen von T-Zellen existieren verschiedene Untertypen. Häufige Varianten sind die Arzneimittel-induzierte Agranulozytose, Hautreaktionen sowie Arzneimittel-induzierte Leber- oder Nierenschädigungen [Böhm et al., 2018].
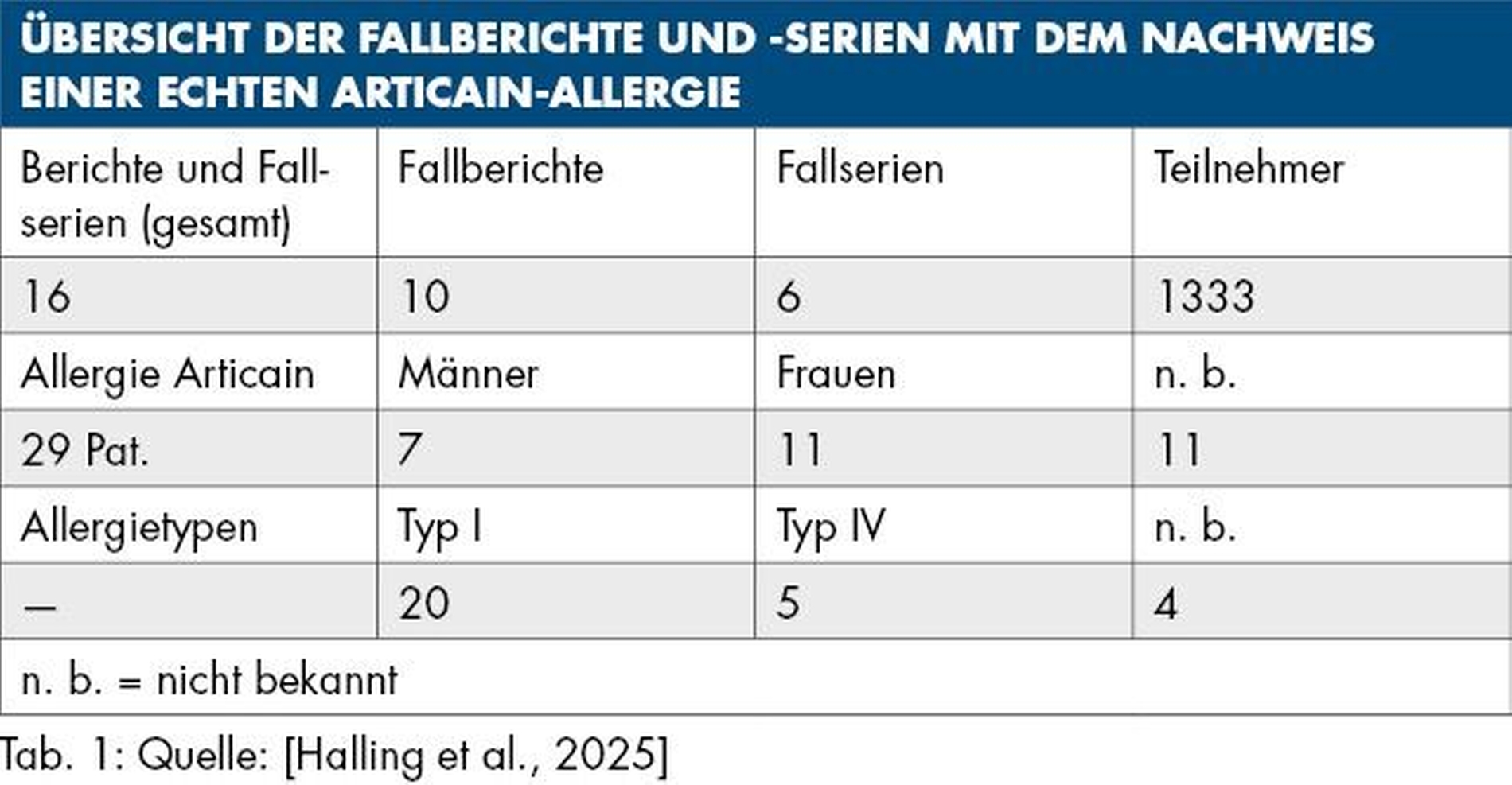
Obwohl lange bekannt ist, dass Articain nur sehr selten eine allergische Reaktion auslöst [Gall et al., 1996], fehlten bislang Daten, die die Häufigkeit einer solchen Allergie belegen. In einem aktuellen Review wurden in den vergangenen 25 Jahren 16 Fallberichte und -serien mit insgesamt 1.333 Teilnehmern gefunden, in denen Articain-Allergien erwähnt wurden [Halling et al., 2025]. Nur bei 29 Patienten konnte mittels klassischer allergologischer Diagnostik (Hauttestungen und/oder Provokationstest) tatsächlich eine echte Articain-Allergie nachgewiesen werden (Tabelle 1). Die Mehrzahl der betroffenen Patienten zeigte eine Typ-I-Allergie im Sinne einer Sofortreaktion. Nur in drei Fällen konnte eine Kreuzreaktivität mit anderen Lokalanästhetika vom Amid-Typ nachgewiesen werden.
Nichtallergische Hypersensitivitätsreaktionen
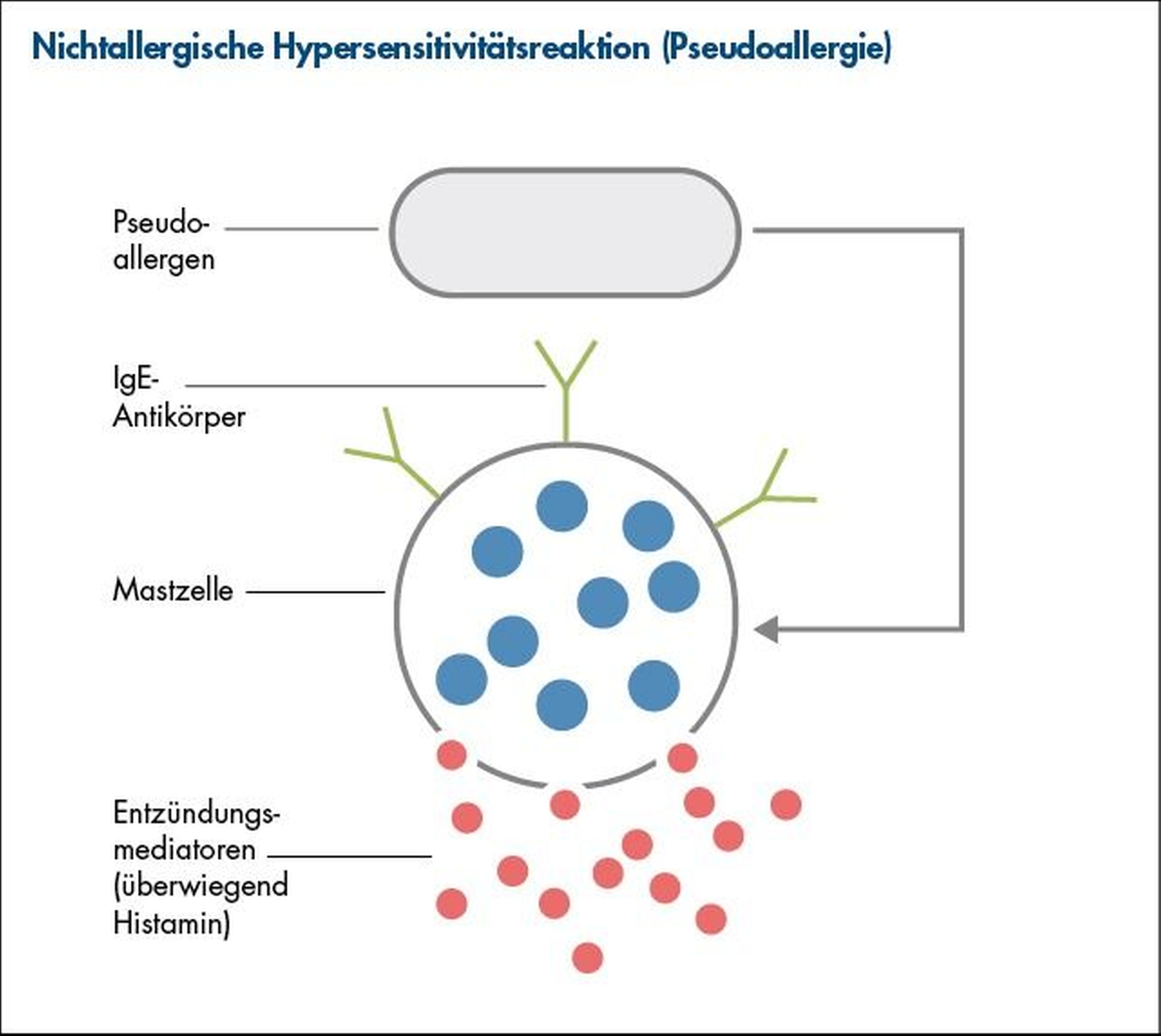
Etwa 77 Prozent aller Hypersensitivitätsreaktionen sind nichtallergischer Natur (auch als Pseudoallergien bezeichnet) [Demoly et al., 1999] (Abbildung 2). Sie werden durch zahlreiche Substanzklassen wie Penicilline und nichtsteroidale Antirheumatika hervorgerufen, aber auch durch Konservierungsstoffe wie Sulfite und Methyl-4-hydroxybenzoat (Methylparabene), die oft als Additiva Nahrungs- oder Arzneimitteln zugesetzt werden, [Wigand et al., 2012; Chatterjee et al., 2024].
Typischerweise ist bei Pseudoallergien das Immunsystem nicht über IgE-Antikörper an der Hypersensitivitätsreaktion beteiligt. Im Unterschied zur Allergie verursachen nicht Eiweißstoffe, sondern kleinmolekulare Substanzen wie Sulfite die pseudoallergene Reaktion [Bundesinstitut für Risikobewertung, 2023].
Die Mastzell-Aktivierung mit Ausschüttung von Histamin und anderen Entzündungsmediatoren erfolgt direkt und unspezifisch ohne vorherige Sensibilisierung und ohne Beteiligung oberflächlich gebundener Antikörper (Abbildung 2). Demzufolge sind diagnostische Haut- oder Bluttests üblicherweise negativ. Klinisch äußern sich die Pseudoallergien ähnlich wie Typ-I-Reaktionen mit Hautausschlag, Rhinitis, Dyspnoe und Krämpfen [Simon, 1996].
a) Sulfite
Lokalanästhetika mit Adrenalinzusatz enthalten je nach Hersteller Sulfite in einer Konzentration von 0,15–0,2 mg/ml. Sie dienen als Antioxidantien zur Stabilisierung des zugesetzten Katecholamins [Perusse et al., 1992]. In der Allgemeinbevölkerung werden Hypersensitivitäten auf Sulfite mit 2,9–4,5 Prozent angegeben [García-Gavín et al., 2012; Casciola et al., 2026].
Bei Patienten, die unter einem allergischen Asthma bronchiale leiden, entwickeln drei bis zehn Prozent eine besondere Überempfindlichkeit auf Sulfite mit Neigung zu Bronchospasmen unterschiedlicher Ausprägung [Vally et al., 2009]. Pérusse und Kollegen zeigten jedoch, dass Steroid-abhängige Asthmatiker ein zehnfach höheres Risiko für eine Sulfit-Überempfindlichkeit zeigten als nicht Kortison-abhängige Asthmatiker (8,4 Prozent versus 0,8 Prozent) [Pérusse et al., 1992].
Der Mechanismus, über den Sulfite zur Bronchokonstriktion beziehungsweise zum Asthma bronchiale führen, ist noch nicht genau bekannt. Da in Nahrungsmitteln Sulfite in wesentlich höher Konzentrationen als in Lokalanästhetika zugesetzt sind, sollte man nur beachten, dass Patienten, die eine Reaktion bei Nahrungsmitteln zeigten, möglicherweise auch bei Adrenalin-haltigen Lokalanästhetika überempfindlich reagieren könnten.
b) Methylparabene
Methyl-4-hydroxybenzoat (Methylparaben) ist ein bakteriostatisches Fungizid und wird nur noch bei Mehrfachentnahmeflaschen für Lokalanästhetika als Konservierungsstoff eingesetzt. In den üblichen 20-ml-Flaschen ist 1 mg des Konservierungsstoffs enthalten.
Aufgrund des zusätzlichen Allergierisikos von Methylparaben [Kajimoto et al., 1995; Decloux und Ouanounou, 2020] gelten Mehrfachentnahmeflaschen eher nicht als empfehlenswert [Kämmerer, 2024]. In vielen Ländern wie den USA und Skandinavien sind diese Zubereitungen nicht mehr erhältlich.
Fazit für die Praxis
Eine echte Allergie auf den Wirkstoff Articain ist äußerst selten, aber möglich. Nur vor dem Hintergrund einer differenzierten Anamnese und mit einer standardisierten allergologischen Diagnostik sind solche Allergien tatsächlich nachweisbar. Bei der Untersuchung auf Unverträglichkeiten ist zu beachten, dass Adrenalin-haltige Lokalanästhetikazubereitungen und Mehrfachentnahmeflaschen neben dem Lokalanästhetikum weitere Zusatzstoffe enthalten, die pseudoallergische Reaktionen hervorrufen können.
Im Rahmen einer strukturierten allergologischen Abklärung und in Absprache mit den entsprechenden Fachstellen sollte Patienten in unklaren Fällen zur Austestung eine Adrenalin-freie, eine Adrenalin-haltige Karpule sowie gegebenenfalls eine Mehrfachentnahmeflasche mitgegeben werden.
Patienten, bei denen eine Articain-Allergie nachgewiesen wurde, können alternativ mit Lidocain oder Mepivacain betäubt werden. Patienten, die auf die Zusatzstoffe reagieren, sollten möglichst mit Adrenalin-freien Zubereitungen anästhesiert werden.
Literaturliste
Athbhaiya, G., Tiwari, A., Choudhary, R. and P. K. Samal. Pharmacological and toxicological effects of paracetamol: current knowledge and a review. Drug Chem Toxicol, 2026. 5: p.1-24.
Böhm, R., Proksch, E., Schwarz, T. and I. Cascorbi, Drug hypersensitivity – diagnosis, genetics, and prevention. Dtsch Arztebl Int, 2018. 115: p.501–512.
Bundesinstitut für Risikobewertung (BfR), Schwefeldioxid und Sulfite: EFSA-Neubewertung sieht gesundheitliche Risiken bei hohem Verzehr; Datenlage weiterhin lückenhaft. www.bfr.bund.de/cm/343/schwefeldioxid-und-sulfite-efsa-neubewertung-sieht-gesundheitliche-risiken-bei-hohem-verzehr-datenlage-weiterhin-lueckenhaft.pdf (Letzter Zugriff am 10.02.2026)
Casciola, G., Stingeni, L. Bianchi, L., Agostinelli, D., Tramontana, M. and K. Hansel. Positive patch test reaction to sodium metabisulfite: prevalence, relevance and clinical implications. Contact Dermatitis, 2026. 94(2): p.166-172.
Chatterjee, S., Adhikary, S., Bhattacharya, S., Chakraborty, A., Dutta, S., Roy, D., Ganguly, A., Nanda, S. and P. Rajak. Parabens as the double-edged sword: Understanding the benefits and potential health risks. Sci Total Environ, 2024. 954:176547.
Coombs, R.R.A. and P. G. H. Gell. Classification of allergic reactions responsible for drug hypersensitivity reactions. In: Clinical Aspects of Immunology, 2nd ed.; Davis: Philadelphia 1968.
Daubländer, M., Müller, R. and M. D. Lipp. The incidence of complications associated with local anesthesia in dentistry. Anesth Prog, 1997. 44(4): p.132-141.
Decloux, D. and A. Ouanounou. Local anaesthesia in dentistry: a review. Int Dent J, 2020. 71(2): p.87–95.
Demoly, P., Lebel, B., Messaad, D., Sahla, H., Rongier, M., Daurès, J.P., Godard, P. and J. Bousquet. Predictive capacity of histamine release for the diagnosis of drug allergy. Allergy, 1999. 54: p. 500–506.
Doña, I., Barrionuevo, E., Blanca-Lopez, N., Torres, M.J., Fernandez, T.D., Mayorga, C., Canto, M. and G. Blanca. Trends in hypersensitivity drug reactions: more drugs, more response patterns, more heterogeneity. J Investig Allergol Clin Immunol, 2014. 24: p.143–153.
Gall, H., Kaufmann, R. and C. M. Kalveram. Adverse reactions to local anesthetics: analysis of 197 cases. J Allergy Clin Immunol, 1996. 97(4): p.933-937.
García-Gavín, J., Parente, J. and A. Goossens. Allergic contact dermatitis caused by sodium metabisulfite: a challenging allergen: a case series and literature review. Contact Dermatitis, 2012. 67(5): p.260-269.
Halling, F., Neff, A. and T. Ziebart. Local anesthetic usage among dentists: German and international data. Anesth Prog, 2021. 68(1): p.19-25.
Halling, F., Neff, A. and A. Meisgeier. True Allergies to Articaine: A 25-Year Analysis. Dent J (Basel), 2025. 13(5): p.180.
Kämmerer PW. Potenzielle Komplikationen bei der zahnärztlichen Lokalanästhesie. In: Schmerzkontrolle in der Zahnmedizin. Quintessenz, Berlin 2024.
Kajimoto, Y., Rosenberg, M. E., Kyttä, J., Randell, T., Tuominen, M., Reunala, T. and P. H. Rosenberg. Anaphylactoid skin reactions after intravenous regional anaesthesia using 0.5% prilocaine with or without preservative – a double-blind study. Acta Anaesthesiol Scand, 1995. 39(6): p.782-784.
Kassenzahnärztliche Bundesvereinigung (KZBV). Jahrbuch 2024. Berlin 2024, S. 102.
Pérusse, R., Goulet, J.P., and J.Y. Turcotte. Contraindications to vasoconstrictors in dentistry: Part II. Hyperthyroidism, diabetes, sulfite sensitivity, cortico-dependent asthma, and pheochromocytoma. Oral Surg Oral Med Oral Pathol, 1992. 74(5): p.687-691.
Simon, R. A. Adverse reactions to food and drug additives. Immunol Allergy Clin North Am, 1996. 16: p.137.
Sousa-Pinto, B., Fonseca, J.A. and E.R. Gomes. Frequency of self-reported drug allergy: A systematic review and meta-analysis with meta-regression. Ann Allergy Asthma Immunol, 2017. 119(4): p.362-373.e2.
Vally, H., Misso N.L. and V. Madan. Clinical effects of sulphite additives. Clin Exp Allergy, 2009. 39(11): p.1643-1651.
Wigand, P., Blettner, M., Saloga, J. and H. Decker. Prevalence of wine in tolerance: results of a survey from Mainz, Germany. Dtsch Arztebl Int, 2012. 109: p.437–444.