Die bakterielle Kontamination der Raumluft während einer AIRFLOW®-Behandlung
Patienten, zahnärztliches Personal und Zahnärzte sind Bakterien und Viren ausgesetzt, die zu Infektionserkrankungen vor allem der Mundhöhle und der Atemwege führen können. Wer sich für einen Beruf in der Zahnmedizin entschieden hat, dem war klar, dass zahnärztliche Behandlungen immer mit dem Risiko einer Infektion einhergehen. In der Zahnmedizin bedeutet der geringe Abstand zur Mundhöhle des Patienten, eine grundsätzliche Exposition gegenüber Speichel, Blut, Aerosolen und Sulkus-Flüssigkeit des Patienten [Peng et al., 2020]. Der Hauptübertragungsweg von Bakterien und Viren sind Speichel-Tröpfchen [Yang et al., 2020; Szymanska et al., 2005]. Aus diesen Gründen galten in der Zahnmedizin schon immer sehr strenge Hygieneregeln. In den vergangenen Jahrzehnten haben Zahnärzte das Risiko vor allem von Influenza, Tuberkulose, Hepatitis und AIDS beherrscht. Heute gilt es, das Risiko von SARS-CoV-2 ebenfalls erfolgreich zu handhaben.
Nahezu alle zahnärztlichen Instrumente, die bei gängigen zahnärztlichen Behandlungen verwendet werden, erzeugen Aerosole: Handstücke mit niedriger und/oder hoher Geschwindigkeit, Turbinen, Schall- und Ultraschallgeräte, Luft-Wasser-Spritzen und Pulver-Wasserstrahl-Geräte [Graetz et al.,2014]. Aerosole unterscheiden sich von Tröpfchen und Sprühnebel. Aufgrund ihrer geringeren Partikelgröße (< 50 μm) können Aerosole mehrere Meter weit getragen und längere Zeit in der Raumluft nachgewiesen werden [Drisko et al., 2000].
In der Zahnmedizin können Aerosole entstehen als Feststoffpartikel, Pulverstaub (nicht kontaminiert), Spritzer, die sich schnell absetzen (kontaminiert), Geräteaerosol (nicht kontaminiert), Behandlungsaerosol (kontaminiert). Das Risiko einer Kontamination hängt von der Art der Behandlung, dem Infektionsgrad des Patienten und den präventiven Hygienemaßnahmen zur Minimierung der Übertragung kontaminierter Aerosole ab. Bis heute fehlt die wissenschaftliche Evidenz, die zeigt, welches Risiko Aerosole erzeugen und welche Gefahr für Kliniker und Patienten sie darstellen [RKI, 2020]. Ein Grund dafür sind die Schwierigkeiten, den Grad der Kontamination mit Bakterien und Viren, die in Aerosolen transportiert werden, effektiv zu messen.
Über die virale und bakterielle Kontamination von Aerosolen während einer professionellen Zahnreinigung mit AIRFLOW® gibt es nach unseren Recherchen keine wissenschaftliche Literatur. Deshalb führten wir eine Praxis-Anwendungsbeobachtung durch, um das Risiko einer Aerosolkontamination durch den Einsatz der AIRFLOW®-Technologie besser zu verstehen.
Ziel
Ziel der Anwendungsbeobachtung war es, die bakterielle Belastung der Raumluft während einer AIRFLOW®-Behandlung zu messen, um Anhaltspunkte für die Einschätzung des Risikos für Behandler, Praxisteam und Patienten durch Aerosol-Kontaminationen während des Einsatzes der AIRFLOW®-Technologie in verschiedenen Situationen zu bekommen.
Material und Methoden
Die AIRFLOW®-Behandlungen wurden in den Prophylaxeräumen der Firma EMS (Nyon, Schweiz) durch eine Zahnärztin (Dr. Neha Dixit, EMS) durchgeführt. Das Messprozedere und die Rahmenbedingungen für die Ausführung der Prophylaxe waren zuvor von den Autoren konzipiert worden.
Behandelt wurden insgesamt 20 erwachsene Patienten im Alter von 30 bis 45 Jahren. Der Plaque-Index Quigley-Hein modifiziert nach Turesky [Turesky et al., 1970] lag im Durchschnittswert über alle 20 Patienten bei 0,80. Die Prophylaxesitzungen fanden an vier aufeinander folgenden Tagen mit jeweils fünf Patienten statt. Zwischen den Behandlungen wurden die Räume gründlich gelüftet, um verbliebene Aerosole zu entfernen und eine neutrale Ausgangssituation für die nächste Sitzung wiederherzustellen.
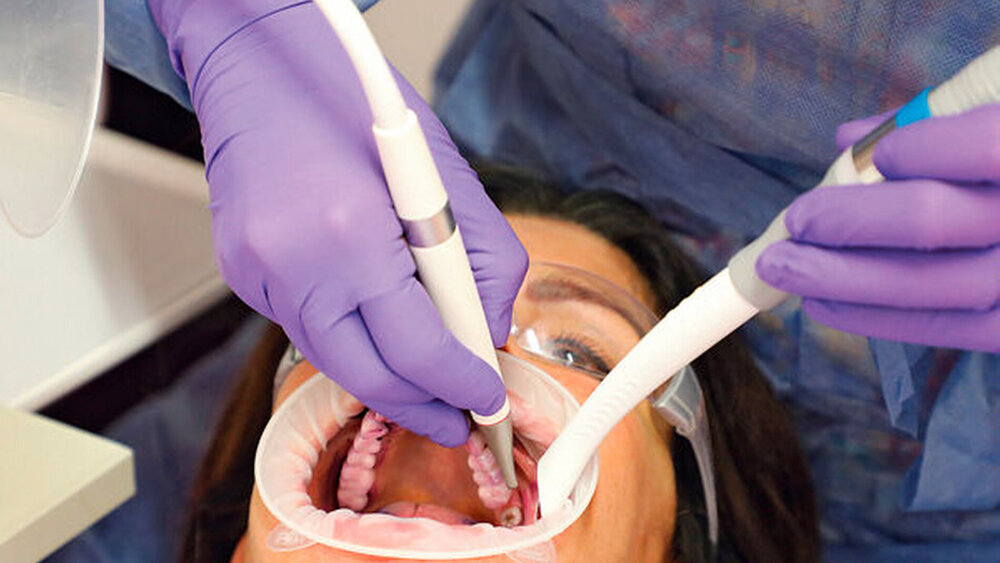
Das Aerosol wurde bei jeder AIRFLOW®-Behandlung exakt zehn Minuten gemessen. Zum Auffangen der Aerosole kam ein mit gefiltertem Wasser vorgefülltes Zyklon-System (PRELECT, Medentex GmbH, Bielefeld, Deutschland), das 20 cm neben dem Patientenmund platziert wurde, zum Einsatz (Abbildung 1). Mit einer Cattani Hochleistungs-Vakuum-Absaugung 900 l/min (Cattani Micro Smart, Parma, Italien) wurden 9 m3 des Luft-Aerosol-Gemischs während der zehnminütigen Behandlung abgesaugt. Unmittelbar nach der Behandlung wurde die bakterielle Kontamination des Aerosols mithilfe eines Adenosin-TriPhosphat-Systems (ATP) gemessen. Diese Methode erlaubt die Bestimmung der Menge aller lebenden Bakterien [Watanabe et al., 2019].
Für die Untersuchung wurden drei Messgruppen definiert:
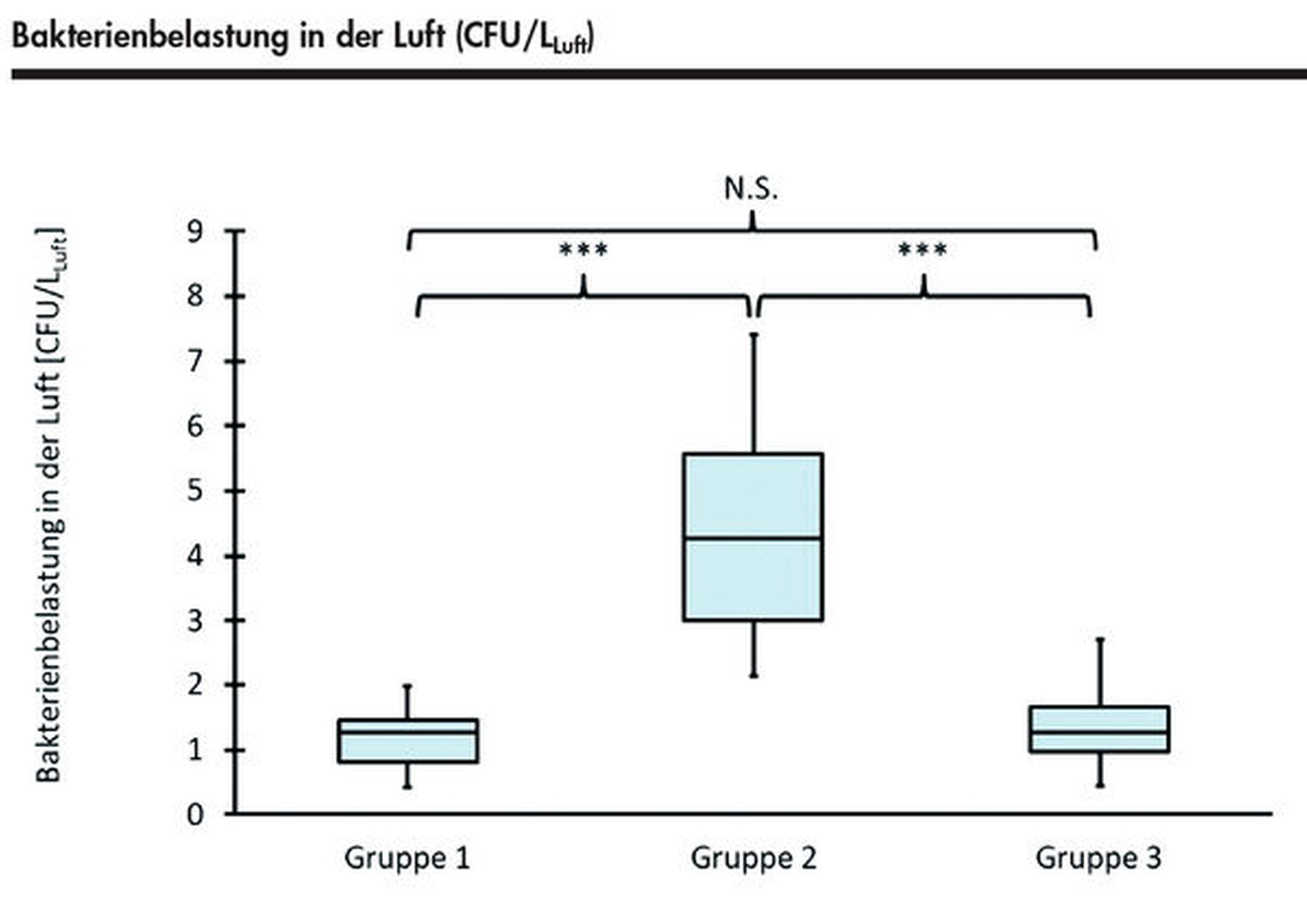
Gruppe 1 (Kontrolle): Raumluftmessung ohne Behandlung, Messung der bakteriellen Belastung von 9 m3 Luft im Behandlungsraum vor jeder Patientenbehandlung (20 Messungen)
Gruppe 2: Raumluftmessung bei einer AIRFLOW®-Behandlung mit Speichelzieher, ohne Mundspülung, ohne Hochvakuumabsaugung (10 Patienten)
Gruppe 3: Raumluftmessung bei einer AIRFLOW®-Behandlung mit Speichelzieher, mit Mund-spülung, mit Hochvakuumabsaugung (10 Patienten)
Entsprechend dem Ablaufprotokoll für die „Guided Biofilm Therapy“ (GBT) wurden die Patienten vor dem Beginn der Behandlung aufgefordert, 60 Sekunden lang mit Chlorhexidin (BacterX, EMS, Nyon, Schweiz) zu spülen (nur Gruppe 3). Nach der Erhebung der Patientenanamnese und der Erfassung der notwendigen Befunddaten wurde bei allen Patienten mit Augenschutz, Speichelzieher (Kaladent, St. Gallen, Schweiz), Optragate (Ivoclar Vivadent, Schaan, Liechtenstein) gearbeitet, zusätzlich in Gruppe 3 mit Purevac®-Hochvakuumabsaugung (Dentsply Sirona, York, Pennsylvania, U.S.A.). Der Biofilm wurde angefärbt (Biofilm Discloser, EMS) und sichtbar gemacht.
Er wurde mit dem AIRFLOW® PROPHYLAXIS MASTER (AFPM) und dem AIRFLOW®-Handstück mit auf Erythritol basierendem PLUS-Pulver (14 µm) entfernt. Das AFPM-Gerät wurde mit der zur Biofilmentfernung empfohlenen Leistung (Stufe 3) und maximaler Wassereinstellung verwendet.
Ergebnisse und Diskussion
Wir konnten mit der vorgestellten Methode reproduzierbar die bakterielle Kontamination von Aerosolen messen, die während einer AIRFLOW®-Behandlung erzeugt werden (Abbildung 2). Die Raumluftmessung bei den AIRFLOW®-Behandlungen mit Speichelzieher, Mundspülung und Hochvakuumabsaugung (Gruppe 3) zeigte dabei das gleiche Niveau bakterieller Kontaminationen, das für die Kontrollgruppe festgestellt wurde (p > 0,05). Mit dem Einsatz von Mundspülung und Hochvakuumabsaugung führte die AIRFLOW®-Behandlung nicht zu einer höheren bakteriellen Aerosol-Kontamination in der Raumluft.
Welchen Anteil die Mundspülung oder die Hochvakuumabsaugung an diesem Ergebnis haben, wurde nicht ermittelt.
Es war nicht das Ziel der Untersuchung, größere Tröpfchen aufzufangen und zu messen. Diese bleiben im Behandlungsumfeld und sind nicht Teil des Aerosols. Die Infektionsgefahr bei diesen Tröpfchen ist die Schmier- und nicht die Aerosolinfektion. Die Schmierinfektion ist schon lange bekannt und wird vom Zahnarztteam durch die Schutzmaßnahmen beherrscht [Watanabe et al., 2019].
Es ist zwingend erforderlich, die RKI-Richtlinien und Empfehlungen für persönliche Schutzausrüstung, für die Oberflächendesinfektion sowie für die korrekte Technik und sachgemäße Anwendung der Geräte strikt zu befolgen.
Schlussfolgerung
Die AIRFLOW®-Behandlung mit der Verwendung von Optragate, einer geeigneten Mundspülung und einer Hochvakuumabsaugung führt zu keinem erhöhten bakteriellen Kontaminationsrisiko für das Praxisteam und die Patienten. Darüber hinaus konnte gezeigt werden, dass mit der „Zweihand-Absaugtechnik“ mit einer Hochvakuumabsaugung in unmittelbarer Nähe des Behandlungsbereichs Aerosole wirksam kontrolliert werden können.
Anmerkung der Autoren:
Weitere aktuelle, noch unveröffentlichte Untersuchungen der Autorengruppe, die unter dem gleichen Ablaufprotokoll mit dem piezokeramischen Scaler PIEZON PS durchgeführt wurden, zeigen, dass bei Verwendung der Schutzmaßnahmen auch von dieser Technologie kein erhöhtes bakterielles Kontaminationsrisiko für das zahnärztliche Personal und die Patienten ausgeht. Auch hier wurde vor der Behandlung mit BacterX gespült und es wurden die Hochvakuumabsaugung und die Zweihandtechnik angewendet. Der Abschlussbericht wird veröffentlicht, sobald die Tests abgeschlossen sind.
Dr. Marcel Donnet
EMS Electro Medical Systems
Chemin de la Vuarpillière 31, 1260 Nyon, Schweiz
mdonnet@ems-ch.com
Prof. Dr. Magda Mensi
Università degli Studi di Brescia, Servizio di Odontostomatologia
5123 Brescia, Italien
Dr. Klaus-Dieter Bastendorf
Praxis Dr. Strafela-Bastendorf
Gairenstr. 6, 73054 Eislingen
Prof. Dr. Adrian Lussi
Universitätsklinikum Freiburg, Klinik für Zahnerhaltungskunde und Parodontologie
Hugstetter Str. 55, 79106 Freiburg
und Zahnmedizinische Kliniken der Universität Bern
Freiburgstr. 7, CH-3010 Bern