Mundbodenabszess ohne dentogenen Fokus – die ungeklärte Ätiologie
Eine 26-jährige Frau stellte sich mit einer ausgeprägten submentalen Schwellung in der Klinik und Poliklinik für Mund-, Kiefer- und Gesichtschirurgie der Universitätsmedizin Mainz vor. Die Patientin berichtete über eine Progredienz der Erkrankung über eine Woche. Ursprünglich sei sie unter der Verdachtsdiagnose einer Sialadenitis der linken Glandula submandibularis antibiotisch therapiert worden, woraufhin sich jedoch keine Besserung gezeigt habe.
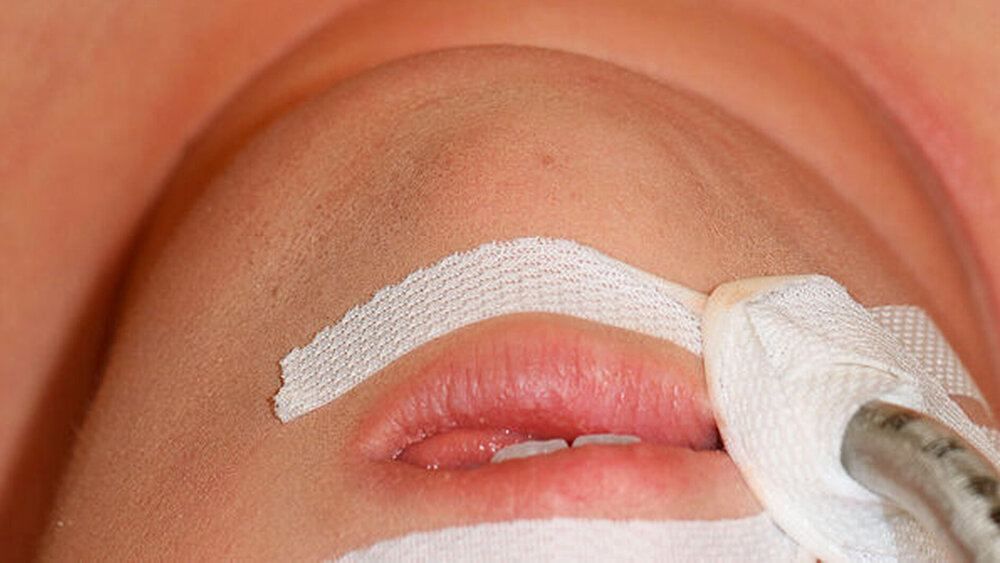
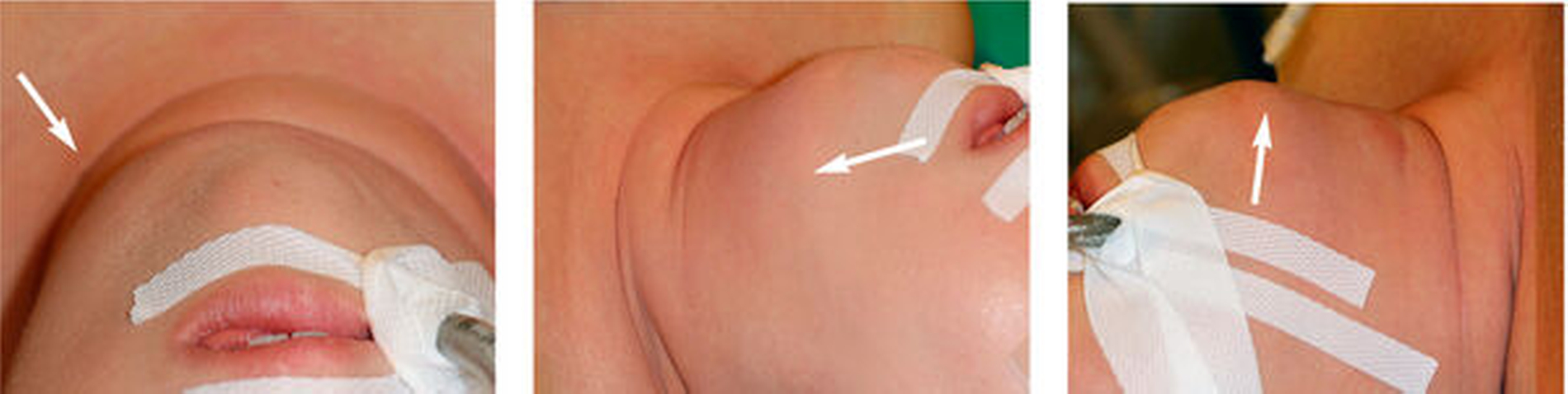
Klinisch war eine deutliche, etwas linksbetonte Schwellung von submental bis zur Klavikula reichend zu beobachten (Abbildung 1). Zum Vorstellungszeitpunkt beklagte die Patienten Schmerzen, Schluck- und beginnende Atembeschwerden. In der klinischen Untersuchung zeigte sich ein konservierend versorgtes, vollständiges Gebiss. Keiner der Zähne war gelockert, perkussionsempfindlich oder avital. Neben dem fehlenden Zahnfokus war außerdem weder ein Speichelsee noch eine von enoral sichtbare Mundbodenschwellung auszumachen. Die Ausführungsgänge sämtlicher Speicheldrüsen zeigten sich unauffällig und förderten klares Sekret; eine Okklusionssymptomatik wurde verneint. Außer einer Neurodermitis war die Allgemeinanamnese der Patientin leer.
In der Labordiagnostik zeigte sich ein deutlicher Anstieg der Entzündungsparameter oberhalb des Normwerts mit einem CRP-Wert von 119 mg/l (Norm: < 5 mg/l) und Leukozytenzahlen von 14,8/nl (Norm: 3,5–10/nl).
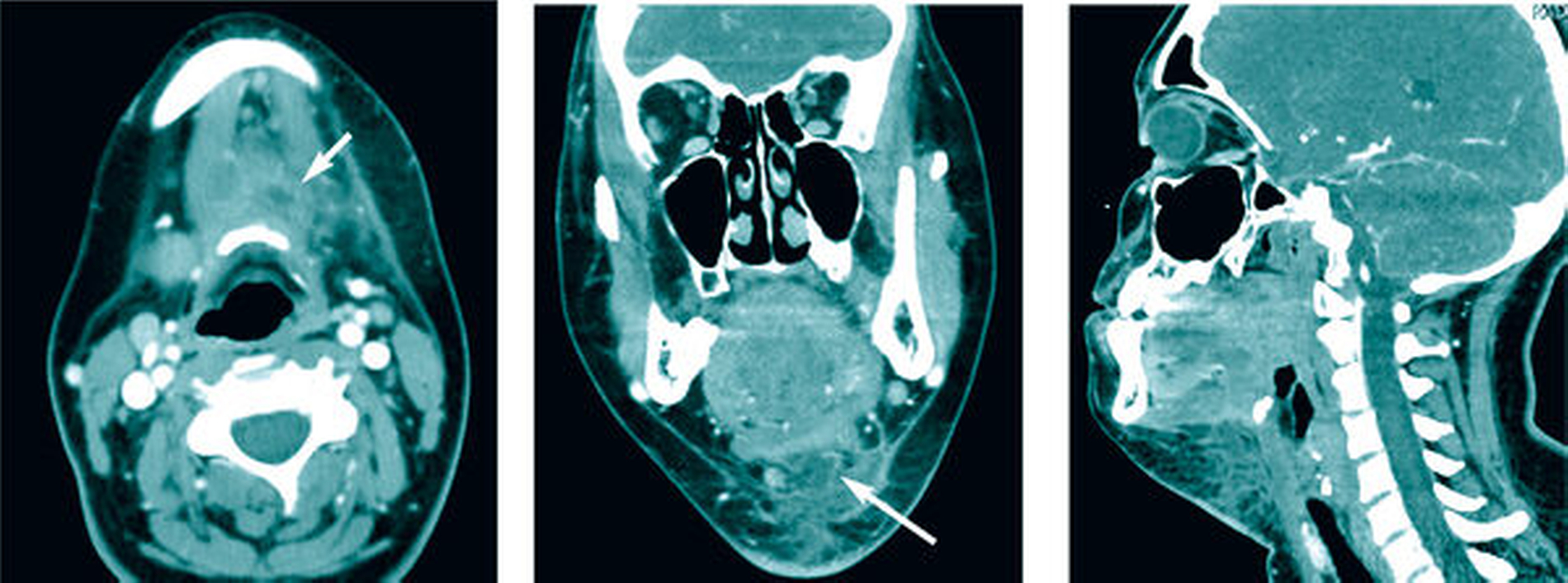
Da die Ursache der starken Schwellung ungeklärt war, wurde eine Computertomografie des Kopf-Hals-Bereichs durchgeführt. Diese zeigte links paramedian eine entzündliche Formation von 2,5 cm x 3 cm, die an den muskulären Mundboden heranreichte. In der Umgebung waren vergrößerte zervikale Lymphknoten darstellbar.
Eine entzündliche Mitbeteiligung des perilaryngealen Weichgewebes sowie der supraglottischen Larynx-Wand war zu beobachten (Abbildung 2).
Kämmerer
Aufgrund der massiven klinischen Symptomatik und der radiologisch abgrenzbaren entzündlichen Formation wurde die Indikation zur operativen Eröffnung des submentalen Abszesses in Intubationsnarkose gestellt. Nach Einzeichnen der relevanten Grenzen wurde eine Inzision zwei Querfinger submental gewählt. Das Gewebe wurde stumpf bis direkt kaudal des Musculus mylohyoideus präpariert, woraufhin sich rahmiger Eiter aus der Abszesshöhle entleerte (Abbildung 3).
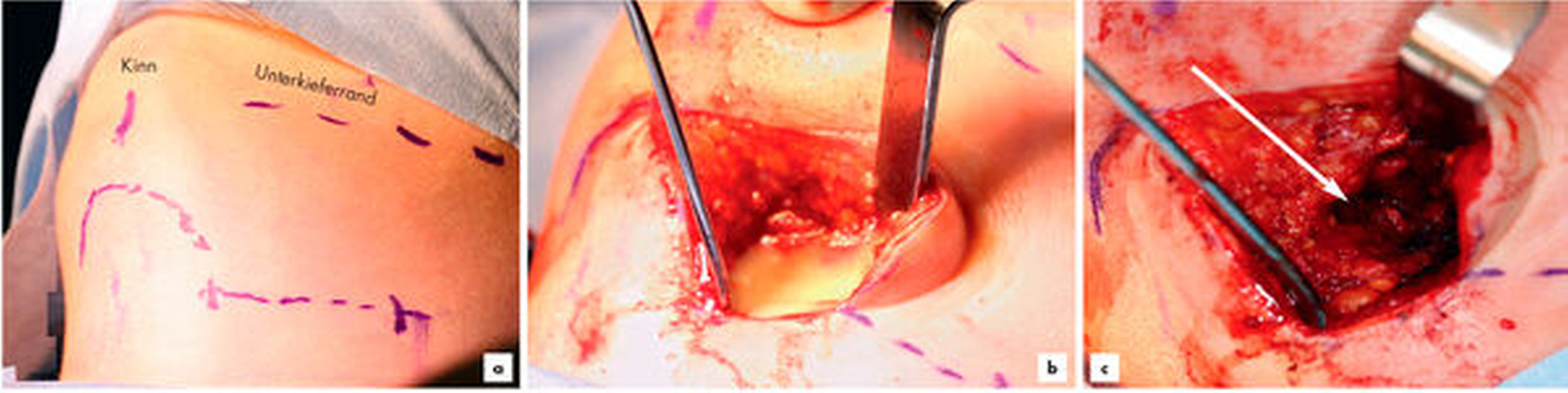
Kämmerer
Wegen der ungeklärten Abszessursache wurden ein Abstrich des Sekrets und Gewebeproben zur weiteren Analyse an das mikrobiologische und pathologische Institut versandt. Unter Einlage von Röhrchen zur Sicherung des Eiterabflusses wurde die Operation beendet. Die eingesendeten Materialien zeigten das Vorhandensein zahlreicher Granulozyten ebenso wie des Bakteriums Staphylokokkus aureus innerhalb einer insgesamt hoch aktiven, florid-granulierenden Entzündung, jedoch keine weitergehenden Befunde inklusive fehlendem Hinweis auf Malignität.
Unter Fortführung der antibiotischen Therapie mit Amoxicillin/Clavulansäure zeigten sich die laborchemischen und klinischen Infektparameter deutlich rückläufig. Der weitere postoperative Verlauf gestaltete sich regelrecht, so dass die eingelegten Drainageröhrchen nach drei Tagen entfernt und die Patientin in die ambulante Weiterbetreuung entlassen werden konnte.
Diskussion
Abszesse werden als Weichgewebsinfektion mit Eiteransammlung in einem durch Gewebszerfall entstandenen Hohlraum definiert [Gujer et al., 2013]. Die Prävalenz odontogener Infektionen liegt zwischen zwei und elf Prozent und ist in niedergelassenen Zahnarztpraxen höher als in Kliniken. Auch werden deutliche regionale Unterschiede beschrieben [Al-Nawas und Karbach, 2016]. Typischerweise treten odontogene Infektionen zwischen dem 20. und dem 40. Lebensjahr auf; Männer scheinen etwas häufiger betroffen zu sein als Frauen.
Meist gehen Infektionen von den ersten oder den dritten Molaren aus, wobei die Zähne des Unterkiefers viel häufiger Ursache des Krankheitsbildes sind als die des Oberkiefers. In den meisten Fällen handelt es sich um ein lokal begrenztes Geschehen, das ambulant therapiert werden kann. Komplikationen hingegen sollten stationär behandelt werden [Al-Nawas und Karbach, 2016].
Es wird zwischen Infiltraten, lokalen odontogenen Infektionen ohne Ausbreitungstendenz – wie der apikalen Parodontitis oder einem submukösen Abszess – und lokalen odontogenen Infektionen mit Ausbreitungstendenz – wie Logenabszessen – unterschieden. Logenabszesse können sub-/para-/perimandibulär, submental, bukkal, temporal oder parapharyngeal lokalisiert sein. Im Fall einer weiteren Ausbreitung sind systemische Komplikationen möglich, etwa eine Osteomyelitis, eine Sinusitits, eine Orbitaphlegmone, ein Hirnabszess bis hin zur Sepsis, eine Endokarditis, eine Mediastinitis oder eine nekrotisierende Fasziitis [Al-Nawas und Karbach, 2016].
Ursachen odontogener Infektionen können eine Karies profunda, eine Pulpitis, eine apikale Parodontitis, eine Periimplantitis, verlagerte und retinierte Zähne oder infiziertes Augmentationsmaterial sein [Al-Nawas und Karbach, 2016].
Eine Studie an Patienten mit einem tiefen Halsabszess untersuchte die Ursachen und Umstände eines solchen Geschehens. In der untersuchten Kohorte war die Tonsillitis die häufigste Ursache eines Abszesses der Kopf-Hals-Region. Odontogene Ursachen folgten auf Platz zwei, während in circa 15 Prozent der Fälle die Ursache des Abszesses ungeklärt blieb. Andere Autoren berichten über ungeklärte Abszessursachen in bis zu 50 Prozent der Fälle.
Zu den am häufigsten betroffenen Bereichen zählen in dieser Studie die Ausbreitung über multiple Regionen, gefolgt von einem peritonsillären oder – wie im vorliegenden Fall – submandibulären Abszessgeschehen [Brito, 2017]. Demgegenüber wird der perimandibuläre Abszess von anderen Autoren als der häufigste Logenabszess des Kopf-Hals-Bereichs angesehen. Dieser entsteht in über 90 Prozent der Fälle durch eine Infektion der Unterkiefer-Molaren. Direkt darauf folgt der submandibuläre Abszess, der anterior durch den M. digastricus und kranial durch die Unterkieferbasis abgegrenzt wird und in zwei Dritteln der Fälle von den Unterkiefer-Molaren ausgeht.
Meist entsteht eine Infektion vor Extraktion der Zähne. Hier besteht das Risiko einer Ausbreitung nach sublingual mit Anhebung des Mundbodens oder nach parapharyngeal mit Vorwölbung des Gaumenbogens. Mundbodenabszesse entstehen meist odontogen, können aber auch nicht-odontogen durch Verletzungen, Tumore, Zysten und Speichelsteine entstehen [Gujer et al., 2013].
Das bakterielle Spektrum der odontogenen Infektion entspricht in aller Regel der Bakterienbesiedlung der Mundhöhle. Die am häufigsten nachgewiesenen Bakterienspezies sind Streptokokkus viridans, Staphylokokkus aureus, Neisseria species und Klebsiella species. Aufgrund der vorhandenen Mischflora werden Antibiotika eingesetzt, die auch Anaerobier erfassen [Al-Nawas und Karbach, 2016].
Klinisch zeigt sich eine apikale Parodontitis durch eine starke Aufbissempfindlichkeit und eine negative Sensibilitätsprobe des betroffenen Zahns. Ein Infiltrat kann hiervon durch die lokale Schwellung abgegrenzt werden. Bei Ausbreitungstendenz der Infektion können außerdem eine Kieferklemme, Schluckbeschwerden, eine deutliche – auch extraorale – Schwellung (nicht mehr durchtastbarer Unterkiefer, angehobener Mundboden) oder eine kloßige Sprache vorkommen. Durch die Verlegung der Atemwege ist eine odontogene Infektion mit Ausbreitungstendenz potenziell lebensbedrohlich [Al-Nawas und Karbach, 2016].
Die Ausbreitung des Infektionsgeschehens in die Logen des Kopf-Hals-Bereichs kann zu systemischen Symptomen – Reduktion des Allgemeinzustands, Kopfschmerzen, Übelkeit, Erbrechen und systemische Komplikationen – führen. Patienten mit Allgemeinerkrankungen sind im Hinblick auf das Auftreten schwerwiegender Komplikationen generell stärker gefährdet. Zu den für einen potenziell komplizierten Verlauf prädisponierenden Allgemeinerkrankungen zählen Diabetes mellitus, Asthma bronchiale sowie die lokale (Radiotherapie) und systemische Immunsuppression (Tumorpatienten, Chemotherapie, Zustand nach Stammzell- oder Organtransplantation, HIV). Auch chronischer Abusus von Drogen und Alkohol stellen Risikofaktoren dar [Al-Nawas und Karbach, 2016].
Die Untersuchung des Patienten sollte aus diesem Grund aus einer ausführlichen allgemeinen und speziellen Anamnese, mit Fokus auf den Allgemeinerkrankungen des Patienten und der Abfrage gerinnungshemmender Substanzen oder familiärer Gerinnungsstörungen bestehen. Eine extra- und enorale Untersuchung inklusive der Vitalitäts- und Perkussionsprobe der Zähne ist unerlässlich.
Eine Ausbreitungstendenz ist anhand einer starken Mundöffnungseinschränkung, eines Druckschmerzes im Bereich des Kieferwinkels oder des Augenwinkels, einer fehlenden Durchtastbarkeit des Unterkiefers, von Schluck- und Atembeschwerden ebenso wie anhand eines angehobenen Mundbodens, einer kloßigen Sprache und Fieber zu erkennen. An die klinische schließt sich schließlich auch eine radiologische Diagnostik mit Identifikation einer odontogenen Ursache an.
Bei fehlender odontogener Ursache oder einer Verschlechterung trotz adäquater Therapie sollte eine weiterführende Bildgebung (Computertomografie, Magnetresonanztomografie, Digitale Volumentomografie) veranlasst werden. Die Empfehlung der Leitlinie zu odontogenen Infektionen lautet hier: „Kann keine odontogene Ursache nachgewiesen werden, insbesondere wenn nach Inzision kein Eiter fließt oder verläuft die Therapie nicht adäquat, sollte eine bakterielle / nicht bakterielle Entzündung oder ein gut- oder ein bösartiger Tumor ausgeschlossen werden“ [Al-Nawas und Karbach, 2016]. Zu den nicht-odontogenen Ursachen zählen unter anderem hämato-onkologische Krankheitsbilder (Leukämie, Lymphome), Karzinome, Sarkome, Metastasen und infizierte Zysten.
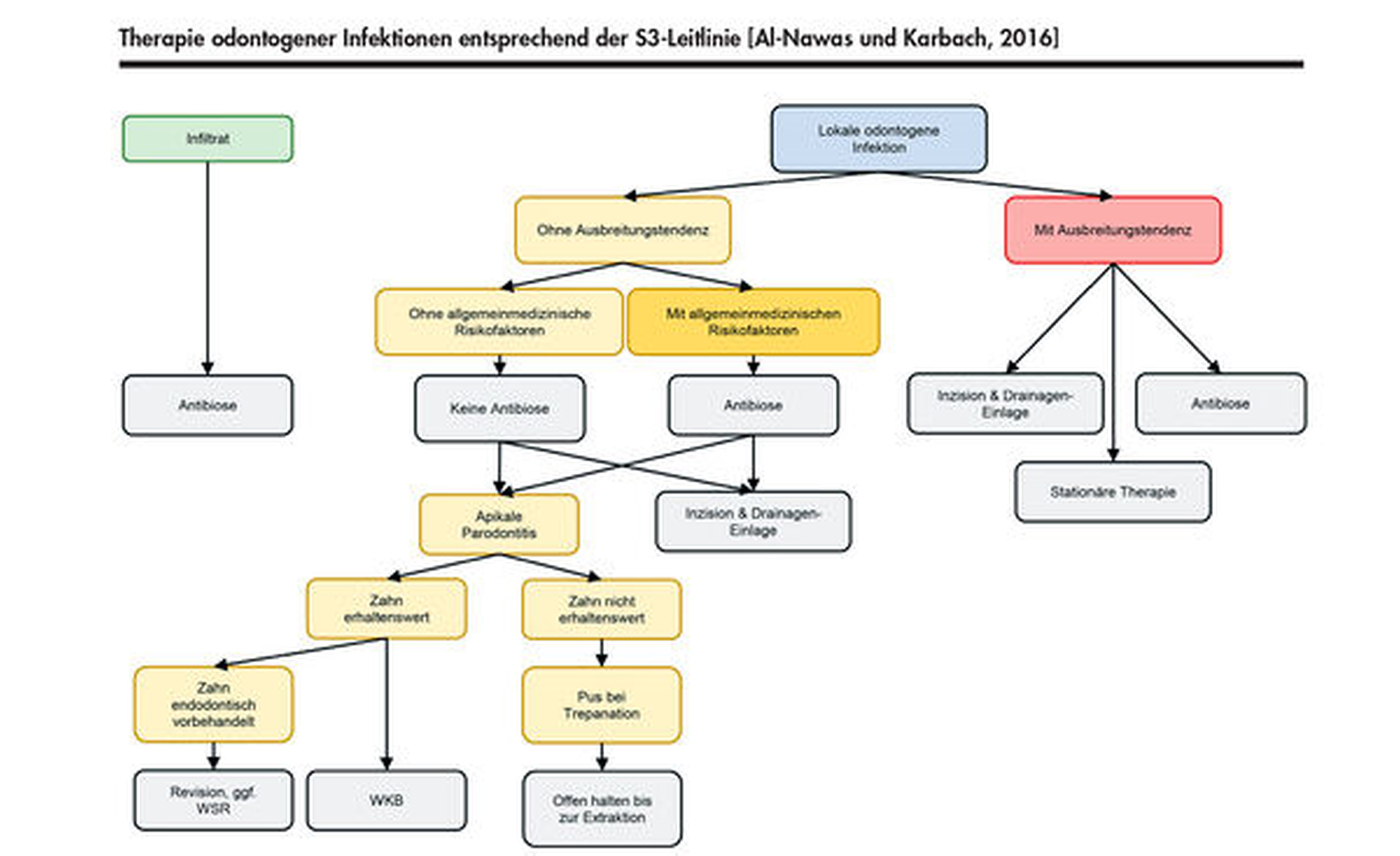
Die Therapie odontogener Infektionen ist entsprechend des therapeutischen Grundsatzes „ubi pus, ibi evacua“ („Wo Eiter ist, dort entleere ihn“) in der Regel primär chirurgisch [Hausamen et al., 2012]. Abbildung 4 gibt einen Überblick über die möglichen Therapieoptionen entsprechend der Leitlinie zu odontogenen Infektionen.
In aller Regel ist eine rein antibiotische Therapie bei Infiltraten ohne Eiteransammlung indiziert, während bei allen anderen lokalen Infektionen mit Eiteransammlung primär die Entlastung des Geschehens im Vordergrund steht. Handelt es sich lediglich um eine lokale odontogene Infektion ohne Ausbreitungstendenz bei einem allgemeinmedizinisch gesunden Patienten, kann von einer antibiotischen Therapie abgesehen werden.
Ist der Zahn erhaltenswert, sollte dieser trepaniert und gespült werden. Schon endodontisch vorbehandelte Zähne können revidiert oder – wenn dies nicht möglich oder sinnvoll erscheinen sollte – wurzelspitzenreseziert werden. Nicht erhaltungswürdige Zähne können trepaniert und offengehalten werden, um den Eiterabfluss sicherzustellen, bis der Zahn zu einem späteren Zeitpunkt extrahiert wird [Al-Nawas und Karbach, 2016].
Die chirurgische Intervention in Form einer Schleimhautinzision erfolgt ab der subperiostalen Phase der Ausbreitung einer apikalen Parodontitis. Hier wird die Schleimhaut an adäquater Stelle eröffnet und das Periost anschließend mit dem Raspatorium vom Knochen gelöst, um eine Entlastung des Abszesses zu ermöglichen [Hausamen et al., 2012]. Wichtig ist es, hierbei darauf zu achten, dass die später eingelegte Drainage die Inzision nicht tamponiert. Eine alleinige antibiotische Therapie ist bei akuten odontogenen Infektionen ohne Ausbreitungstendenz nicht sinnvoll und kann zur Chronifizierung des Geschehens führen [Al-Nawas und Karbach, 2016].
Die Therapie der Wahl bei odontogenen Infektionen mit Ausbreitungstendenz ist die chirurgische Therapie in Form einer kombinierten intra- und extraoralen Eröffnung in Allgemeinanästhesie mit simultaner Entfernung der odontogenen Ursache. Anschließend sollten eine stationäre Überwachung des Patienten bis zur klinischen Besserung und eine intravenöse Antibiotikatherapie erfolgen [Al-Nawas und Karbach, 2016].
Fazit für die Praxis
In bis zu 50 Prozent der zervikalen Abszesse ist die Ursache der Erkrankung unbekannt.
Odontogene Infektionen werden in Infiltrate und lokale odontogene Infektionen mit und ohne Ausbreitungstendenz unterschieden. Insbesondere die Unterscheidung zwischen komplikationsfreien und potenziell komplikationsträchtigen Verläufen ist wegen der möglichen schwerwiegenden Folgeerkrankungen und dem Risiko der Atemwegsverlegung von hoher Relevanz.
Die Therapie eitriger odontogener Infektionen besteht in der chirurgischen Eröffnung der Abszesshöhle und einer anschließenden Drainage. Bei Vorliegen von Risikofaktoren oder einer Ausbreitungstendenz sollten außerdem systemische Antibiotika, vorzugsweise Penicillin oder Aminopenicilline, gegebenenfalls auch in Kombination mit Betalaktamasehemmern Anwendung finden.
Das häufigste in Deutschland in Zahnarztpraxen verwendete Antibiotikum zur Therapie odontogener Infektionen ist Clindamycin, gefolgt von Penicillin und Aminopenicillinen. Bei Clindamycin werden Resistenzraten von 21 bis 50 Prozent, bei Penicillin von 7 bis 33 Prozent beschrieben. Auf Grundlage dieser Daten wird eine empirische antibiotische Therapie mit Penicillin und Amoxicillin aufgrund der gegenüber Clindamycin geringeren Nebenwirkungsrate und der besseren Effektivität empfohlen. Bei Vorliegen einer Ausbreitungstendenz sollte die Kombination mit einem Betalaktamasehemmer erwogen werden. Clindamycin sollte bei einer Penicillinallergie Anwendung finden.
Die Nachsorge des Patienten sollte bis zum Abklingen der klinischen Symptome durchgeführt werden – zur Verlaufskontrolle werden dabei klinische (Mundöffnung, Temperatur) und laborchemische (C-reaktives Protein, Leukozytenanzahl) Infektparameter erfasst. Bei ambulant geführten Patienten ist eine eingelegte Drainage alle zwei bis drei Tage zu wechseln [Al-Nawas und Karbach, 2016].
Zusammenfassung
Anhand des vorliegenden Falls wird die Bedeutung des Zahnarztes als Erstbehandler und diagnostischer Weichensteller deutlich: Nicht selten ist der Fokus eines Abszessgeschehens unbekannt und erfordert eine dezidierte Anamnese und klinische Untersuchung durch den behandelnden Zahnarzt, um eine Überweisung in die richtige Fachabteilung zu ermöglichen. Hierbei sind die anatomischen Kenntnisse der Logen für eine adäquate Einordnung des Falls unabdingbar. In Anbetracht potenziell schwerwiegender Verläufe bei Ausbreitung lokaler Infektionen ist das Erkennen und umgehende Handeln des Zahnarztes von hoher Relevanz. n
Diana Heimes
Klinik und Poliklinik für Mund-, Kiefer und Gesichtschirurgie, Plastische Operationen,
Universitätsmedizin Mainz
Augustusplatz 2, 55131 Mainz
PD Dr. Dr. Peer W. Kämmerer, MA, FEBOMFS
Leitender Oberarzt und stellvertretender Klinikdirektor
Klinik und Poliklinik für Mund-, Kiefer- und Gesichtschirurgie, Plastische Operationen,
Universitätsmedizin Mainz
Augustusplatz 2, 55131 Mainz
peer.kaemmerer@unimedizin-mainz.de