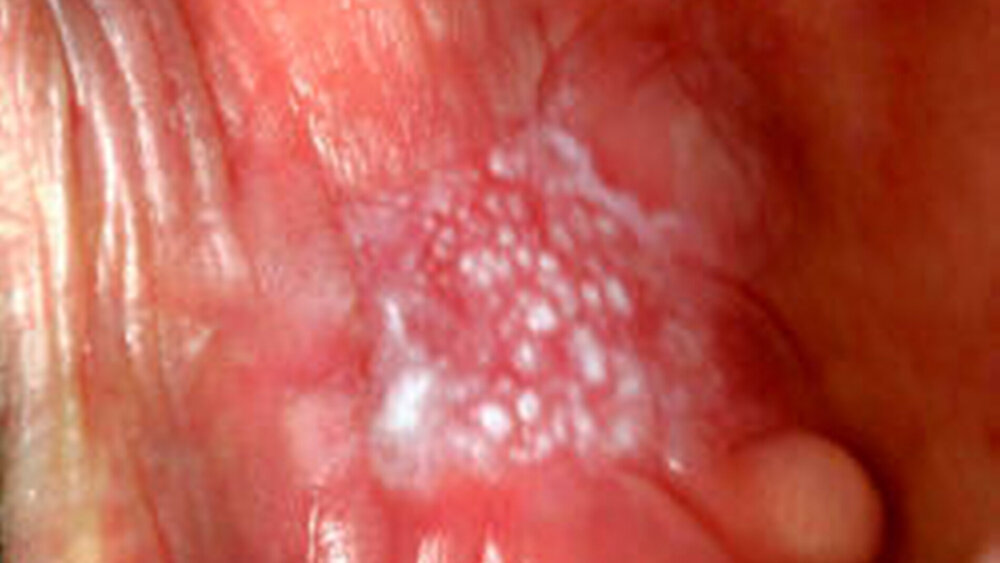
Orale Leukoplakie/Erythroplakie
Definition: Orale Leukoplakie
Die orale Leukoplakie (O.L.) ist die häufigste prämaligne (potenziell maligne) Veränderung der Mundschleimhaut. In der 2005 erschienenen WHO-Klassifikation der Tumoren (Pathology and Genetics, Head and Neck Tumors) wird sie unter der Bezeichnung „epithelial precursor lesions“ beschrieben [1]. Während die orale Leukoplakie zu den „precancerous lesions“ gehört, werden so genannte „precancerous conditions“ (prämaligne Konditionen) davon unterschieden, die die Eisenmangelanämie (sideropenische Dysphagie), den oralen Lichen planus, die orale submuköse Fibrose, die Syphilis, das Xeroderma pigmentosum, den Lupus erythematodes und die Epidermolysis bullosa dystrophicans beinhalten [2]. In der WHO-Klassifikation von 2005 wurde auf eine neue Definition der O.L. verzichtet, so dass diejenige von 1994 [3] unverändert gilt: „Die orale Leukoplakie ist eine vorwiegend weiße Veränderung der Mundschleimhaut, die weder klinisch noch histopathologisch als eine andere definierbare Schleimhautveränderung charakterisiert werden kann“.
Die Bezeichnung „orale Leukoplakie“ dient lediglich als Beschreibung des klinischen Befundes und sollte nicht als histopathologische Diagnose verwendet werden. Im Gegensatz dazu sollten auch die Begriffe „Hyperkeratose“ oder „Dyskeratose“, die den histopathologischen Befund charakterisieren, als nicht klinische Begriffe angewandt werden.
Epidemiologie
Inzidenz und Prävalenz der O.L. variieren weltweit stark. Die Prävalenzen liegen zwischen 0,2 und 5 Prozent, wobei deutliche regionale Unterschiede auftreten. So wurden für Indien Prävalenzen von 0,2 bis 4 Prozent ermittelt [4]. In Schweden betrug die Prävalenz 3,6 Prozent [5], in Holland 1,4 Prozent [6]. In einer in Deutschland durchgeführten epidemiologischen Studie konnte eine Prävalenz für Männer von 2,3 Prozent und für Frauen von 0,9 Prozent ermittelt werden [7]. Orale Leukoplakien werden am häufigsten bei Männern mittleren oder älteren Lebensalters beobachtet. Die Geschlechtsverteilung hängt von geografischen Unterschieden ab. In den meisten Ländern sind Männer häufiger betroffen, obwohl dieses für die westliche Welt nicht immer zutrifft.
Klinisches Bild
Orale Leukoplakien können isoliert oder multipel auftreten. Die O.L. wird in allen Bereichen der Mundhöhle beobachtet, ist aber am häufigsten an der Wangenschleimhaut, der Mukosa des Alveolarfortsatzes, dem Mundboden, der Zunge, den Lippen und dem Gaumen anzutreffen. Zwei klinische Varianten der Leukoplakie sind zu unterscheiden: die homogenen und inhomogenen Formen, die miteinander auftreten können. Die homogene O.L. wird als vorwiegend weiße Veränderung definiert. Sie hat ein einheitliches flaches und dünnes Erscheinungsbild. Flache Furchen können auftreten. Die Oberfläche ist glatt, faltig oder wellig und zeigt eine weitgehend konsistente Textur. Die homogene O.L. ist meist asymptomatisch. Die inhomogene O.L. wurde als vorwiegend weiße oder als weiße und rote Veränderung (Erythroleukoplakie) definiert. Diese kann unregelmäßig flach, nodulär oder exophytisch sein (verruköse Leukoplakie). Diese Formen der Leukoplakie können zu leichten Beschwerden wie Schmerzen oder Brennen der Mundschleimhaut führen.
Eine Sonderform ist die idiopathische Leukoplakie, bei der keine ätiologischen Faktoren vorliegen. Darüber hinaus ist die proliferative verruköse Leukoplakie beschrieben worden [2, 8]. Hierbei handelt es sich um eine aggressive Form der O.L., die in fast allen Fällen maligne transformiert. Sie ist gekennzeichnet durch ausgedehnte und multifokale, zunächst homogene, später verruköse Veränderungen. Häufig liegen keine bekannten Risikofaktoren vor. Im Allgemeinen unterliegen inhomogene Leukoplakien einer höheren malignen Transformationsrate. Mundhöhlenkarzinome können sich aber aus jeder Form der Leukoplakie entwickeln. Zu bedenken ist ebenfalls, dass ein großer Teil der Mundhöhlenkarzinome ohne erkennbare assoziierte Leukoplakie entstehen kann [9].
Die meisten Leukoplakien unterliegen keiner malignen Transformation und können sich zurückbilden, wenn ätiologische Faktoren vermieden werden [10].
Ätiopathogenese
Die Ätiologie der O.L. ist bis heute nicht vollkommen geklärt, obwohl Tabak als Hauptfaktor angesehen wird [11-14]. Die Assoziation mit Tabak liegt aber nicht in allen Fällen vor (idiopathische Leukoplakie). Alkohol ist ein Co-Faktor der vor allem zu einer Permeabilitätsveränderung des oralen Epithels führt, so dass toxische Produkte des Tabaks, der bis zu 90 unterschiedliche Karzinogene enthält, leichter in die subepithelialen Kompartimente übertreten können. Damit ergibt sich ein Synergismus zwischen Tabak und Alkohol, wie er für das Mund höhlenkarzinom ebenfalls gilt. Gerauchter Tabak (Zigaretten, Zigarren, Pfeife) scheint einen deutlicheren Einfluss zu haben als „smokeless tobacco“ (Kautabak), wie er in den USA und Skandinavien verwendet wird. Durch diesen „smokeless tobacco“ hervorgerufene Leukoplakien scheinen eine sehr niedrige Transformationsrate zu haben [15].
Eine höhere Transformationsrate scheint bei Candida-infizierten O.L. vorzuliegen. Bis heute besteht keine Einigkeit dazu, ob diese Veränderung als Candida-Leukoplakie oder als hyperplastische Candidiasis zu bezeichnen sei. Auch ist unklar, ob die Candida-Infektion die Ursache der Leukoplakie ist oder ob es sich um eine Superinfektion einer präexistenten Schleimhautveränderung handelt. Neben Tabak und Alkohol wurde immer wieder die Rolle humaner Papillomviren (HPV) und anderer Viren als möglicher Faktor diskutiert. Hochrisiko-HPVs wie HPV 16 und 18 sind mit dem Mundhöhlenkarzinom assoziiert [16-18]. Andere Faktoren wie der bereits erwähnte Alkohol, schlechte Ernährungsgewohnheiten, Vitaminmangel (Vitamin A, C) Arecanuss (Betel), unterschiedliche Mundspülungen, chronisch traumatische Irritationen, schlechte Mundhygiene, niedriger sozio-ökonomischer Status, Galvanismus und genetische Faktoren sind als mögliche Begleitfaktoren für die Entstehung eines O.L. diskutiert worden.
Diagnose
Die vorläufige Diagnose der O.L. beruht auf dem klinischen Erscheinungsbild bei Erstvorstellung, wobei Inspektion und Palpation die einzigen diagnostischen Hilfsmittel sind.
Die definitive klinische Diagnose beruht auf Persistenz der Veränderung nach Ausschaltung möglicher ätiologischer Faktoren mit einer Beobachtungszeit von zwei bis vier Wochen (gelegentlich ist ein längerer Zeitraum notwendig). Die definitive Diagnose wird durch Biopsie und histopathologische Untersuchung bestätigt. Die histopathologische Untersuchung einer O.L. ermöglicht dem Kliniker: 1. andere Erkrankungen der Mundschleimhaut auszuschließen und 2. Informationen über den Grad der Epitheldysplasie zu bekommen.
werden die heute gebräuchlichen Schemata der histologischen Charakterisierung von epithelialen Vorläuferveränderungen (orale Leukoplakie, orale Erythroplakie) gegeneinandergestellt. Die WHO-Klassifikation basiert auf der herkömmlichen Einteilung in Hyperplasie, leichte Dysplasie, mittelschwere und schwere Dysplasie sowie carcinoma in situ. Dagegen stehen die heute ebenfalls angewendeten Schemata der oralen intraepithelialen Neoplasie (OIN) sowie die Ljubljana-Klassifikation der plattenepithelialen intraepithelialen Läsion. Der Grad der Dysplasie ist hinsichtlich möglicher Transformationen von großer Bedeutung. Es wird angenommen, dass dysplastische Veränderungen auf genetischen Mutationen beruhen. Je ausgeprägter die Dysplasie, umso höher die Wahrscheinlichkeit der malignen Transformation [1, 19]. Dies trifft insbesondere für die Erythroplakien zu [20].
Differenzialdiagnose
Differenzialdiagnostisch müssen die folgenden Erkrankungen mit eingeschlossen werden: oraler Lichen planus, Lupus erythematodes, Leuködem, orale Candidiasis, weißer Schwammnävus, orale Haarleukoplakie, friktionsbedingte Veränderungen, Wangen- oder Lippenbeißen (Morsicatio), lichenoide Reaktionen und der Rauchergaumen.
Genetische Aspekte
Bis heute stehen keine „Marker“ zur Verfügung, die eine maligne Transformation verlässlich voraussagen können. Molekularbiologische Techniken, mit denen die besten Voraussagen für eine mögliche maligne Transformation zur Verfügung stehen, sind Untersuchungen zum Genomstatus (DNAPloidie) und Verlust der Heterozygosität. Ploidie-Studien dysplastischer Leukoplakien haben gezeigt, dass die meisten Plattenepithelkarzinome aus aneuploiden Veränderungen entstehen, im Gegensatz zu 60 Prozent tetraploider Veränderungen und nur 3 Prozent diploider Läsionen [21]. Studien zum Verlust der Heterozygosität zeigten, dass zwei Chromosomenarme, 3P und 9P, für eine mögliche Progression der Veränderung von Bedeutung zu sein scheinen [22].
Andere diagnostische Methoden, wie die Anwendung von Toluidinblau oder Exfoliativ- Zytologie können hilfreich sein, ersetzen allerdings die Biopsie nicht. Die Methodik der Bürstenbiopsie (brush biopsy) basiert zum einen auf dem Prinzip der DNA-Zytometrie sowie zum anderen auf dem CDx- Verfahren. Eine endgültige Bewertung für beide Verfahren steht noch aus [23-26].
Prognose
Die maligne Transformationsrate der O.L. variiert zwischen 0,9 und 17,5 Prozent [27]. Insgesamt transformieren 3 bis 8 Prozent aller Leukoplakien über einen Zeitraum von fünf Jahren [28]. Grundsätzlich kann jede O.L. transformieren, auch wenn sie zunächst histologisch keine Epitheldysplasien aufweist. Obwohl eine maligne Transformation nicht verlässlich vorausgesagt werden kann, sind einige Faktoren bekannt, die ein höheres Transformationsrisiko darstellen, vor allem wenn sie:
1. Frauen betreffen2.seit langem bestehen3.bei Nichtrauchern auftreten4.im Mundboden oder an der Zunge entstehen5. bei Patienten auftreten, die bereits früher ein Plattenepithelkarzinom im Kopf-Halsbereich entwickelten6.Inhomogenität zeigen7.Candida-infiziert sind8.Epitheldysplasie aufweisen9.DNA-Aneuploidie zeigen.
Einige O.L. zeigen eine erhöhte Rezidivrate, vor allem die proliferative verruköse Leukoplakie. Im Gegensatz dazu können sich O.L. auch spontan, ohne spezielle Therapie zurückbilden.
Ein regelmäßiges Follow-up von Patienten mit O.L. ist unumgänglich. Patienten sollten grundsätzlich alle sechs Monate kontrolliert werden. Dies gilt für behandelte wie auch für unbehandelte Patienten, dabei sind kürzere Intervalle bei Patienten mit inhomogenen Formen der O.L. empfehlenswert.
Therapie
Bis heute gibt es keine allgemein akzeptierten Leitlinien zur Therapie der O.L. [29]. Es werden verschiedene Therapien zur Behandlung der O.L. eingesetzt, die mit unterschiedlichen Ergebnissen zu werten sind. Keine der heute gebräuchlichen Therapien kann das Risiko einer malignen Transformation grundsätzlich ausschließen. Die Initialtherapie besteht in der Entfernung möglicher ätiologischer Faktoren wie Tabak, Alkohol, Candidainfektion unter anderen. Die vollständige und definitive Aufgabe des Tabakabusus muss als obligatorisch für Patienten mit O.L. gelten (siehe Prävention). Die komplette chirurgische Entfernung einer O.L. im Gesunden wird für alle Fälle mit Epitheldysplasie empfohlen [29]. In Fällen ohne Epitheldysplasie hängt die Entscheidung, ob eine Behandlung durchgeführt werden soll oder nicht, von der Lokalisation und dem Ausmaß der O.L. sowie vom allgemeinmedizinischen Zustand des Patienten ab. Neben der chirurgischen Exzision sind andere Therapiemodalitäten, wie die CO2- Laserchirurgie, die Kryochirurgie, die photodynamische Therapie sowie die systemische Therapie mit Retinoiden und Betakarotin, möglich. Bleomycin und Calcipotriol wurden ebenfalls neben vielen anderen Therapien angewendet. Die Hauptnachteile der meisten dieser Therapien sind häufige Nebenwirkungen und Rezidive nach Absetzen der Therapie.
Prävention
Verfügung, um die Entwicklung von oralen Leukoplakien oder oralen Plattenepithelkarzinomen zu verhindern. Eine gesunde Lebensführung mit Tabakabstinenz ist die beste Möglichkeit, um einer O.L. oder einem oralen Plattenepithelkarzinom vorzubeugen. Die WHO sowie die FDI und viele nationale Zahnärztekammern fordern die Zahnärzteschaft und das zahnärztliche Team darüber hinaus auf, Tabakprävention auch in die zahnärztliche Praxis einzuführen [30]. Eine gesunde Ernährung mit frischen Früchten und Gemüse hat eine mögliche protektive Wirkung bei der Primärprävention des Mundhöhlenkarzinoms und seiner Vorstufen. Die frühzeitige Diagnose und Therapie der Leukoplakie führt darüber hinaus zu einer Reduktion an Morbidität und Mortalität verursacht durch das Mundhöhlenkarzinom. Screeningprogramme (gezieltes Screening) sollten sich vor allem auf Risikoindividuen erstrecken. Dieses sind Menschen höheren Lebensalters (40 bis 70 Jahre, Männer) sowie Risikofaktoren wie Tabak und Alkohol [30].
Prof. Dr. Peter A. Reichart,Charite- Universitätsmedizin BerlinCampus Virchow-Klinikum,Zentrum für ZahnmedizinAbteilung für Oralchirurgie und zahnärztlicheRöntgenologieAugustenberger Platz 113353 Berlinpeter-a.reichart@charite.de
Nachdruck mit freundlicher Genehmigung aus dzz 1/2007