Die vierte Therapiestufe – Sicherung des Therapieerfolgs
Wie in den vorhergehenden drei Beiträgen zur systematischen Therapie (zm 6, 7, 8/2021) beschrieben, stellt die Parodontitis eine komplexe Entzündungserkrankung dar. Es konnte aufgezeigt werden, dass durch adäquate, an den Schweregrad und die Risikofaktoren angepasste individuelle Maßnahmen der ersten bis dritten Therapiestufe das Entzündungsgeschehen kontrollierbar wird und somit die Destruktion des Zahnhalteapparats gestoppt oder zumindest entscheidend verlangsamt werden kann.
Aber wie bei vielen chronischen Entzündungserkrankungen sind es die Risikofaktoren, die in der Mehrzahl eine aktive Beteiligung der betroffenen Patienten erfordern, um langfristig die Therapieerfolge zu sichern. Daher müssen diese auch die Grundlage für eine individuell gestaltete (risikoadaptierte) Therapiestufe 4, die sogenannte unterstützende Parodontaltherapie (UPT), sein. Vor Beginn der Therapiestufe 4 muss im Rahmen einer abschließenden Beurteilung der vorhergehenden Therapiestufen festgestellt werden, ob und inwieweit die Therapieziele erreicht wurden.
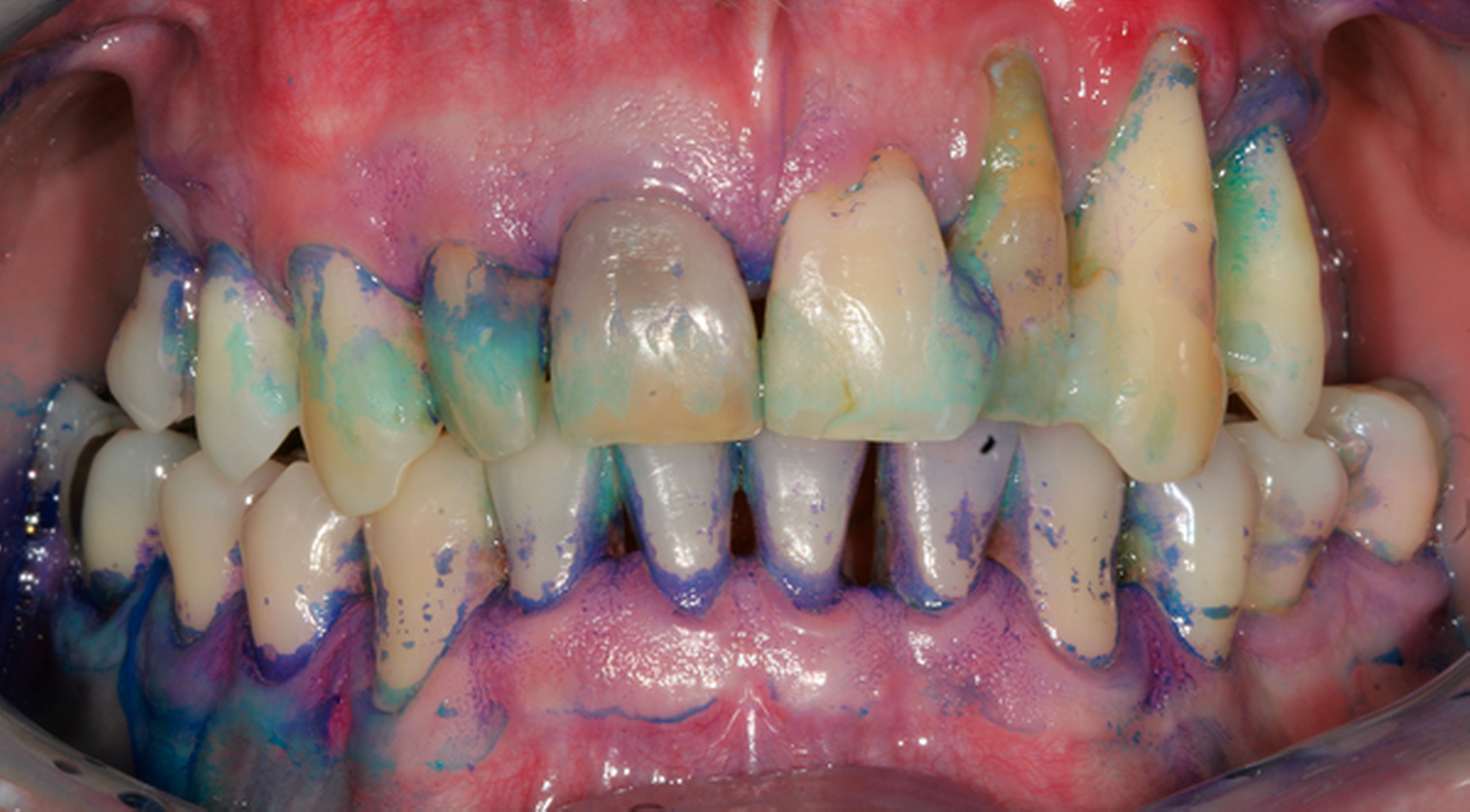
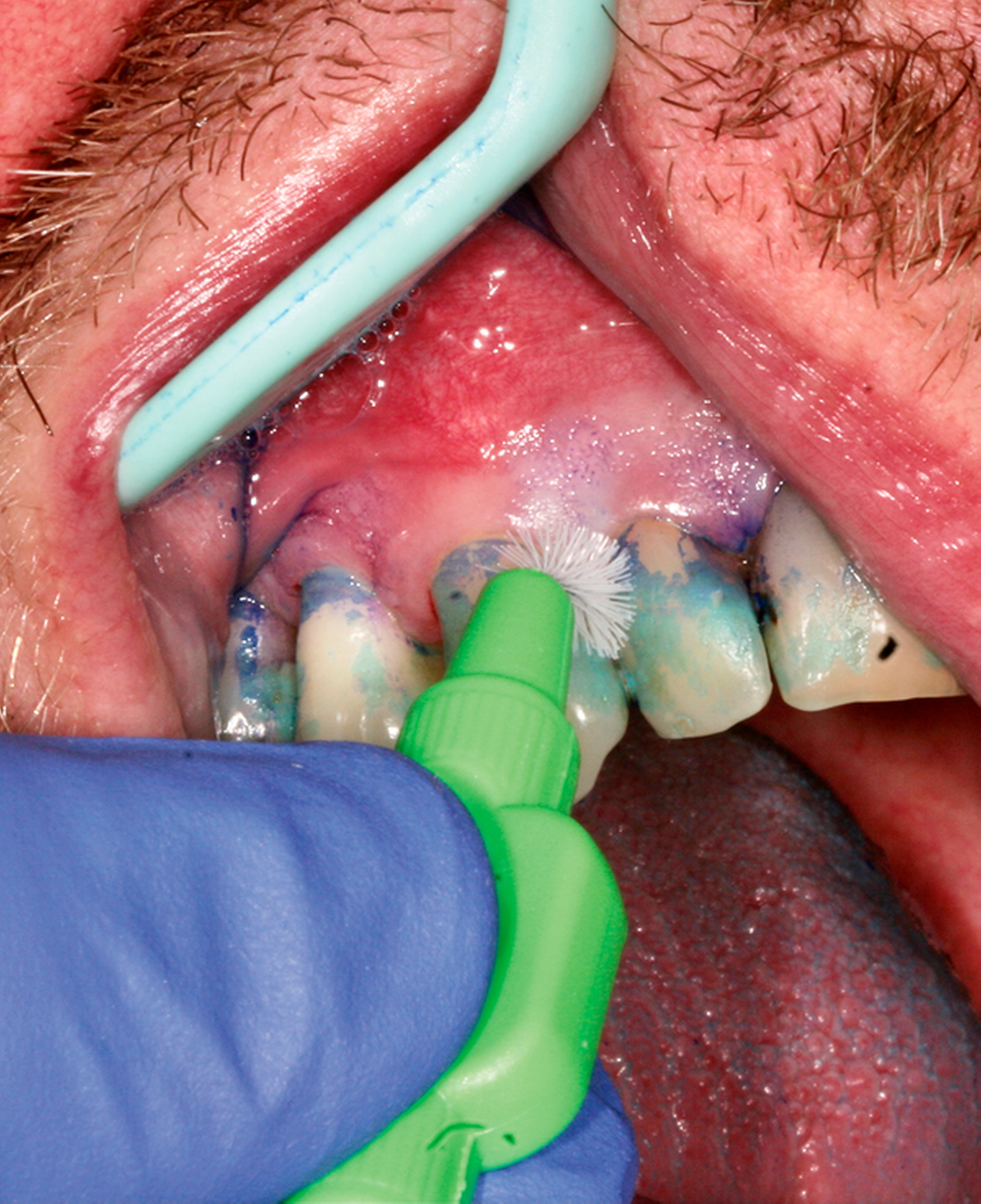
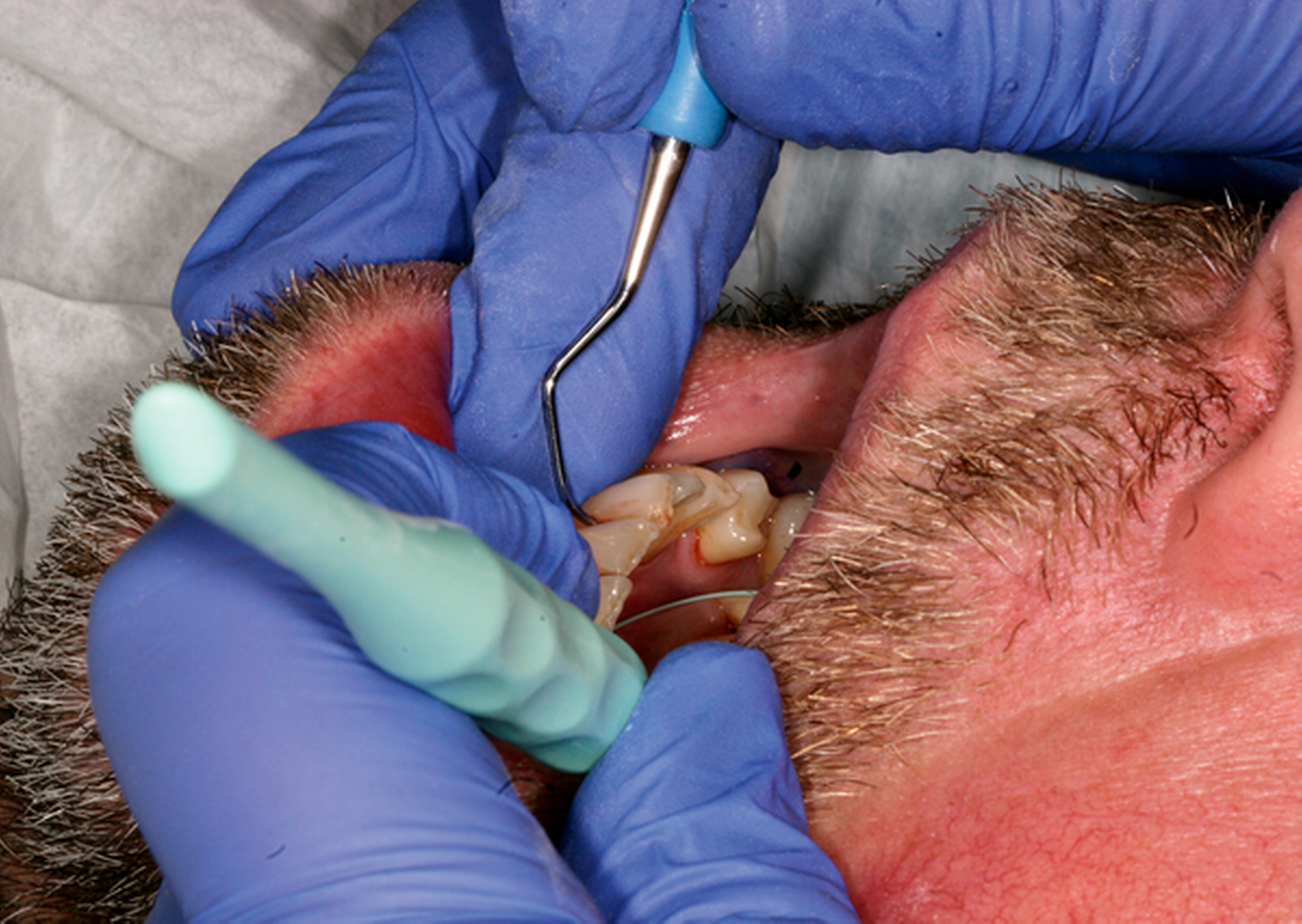
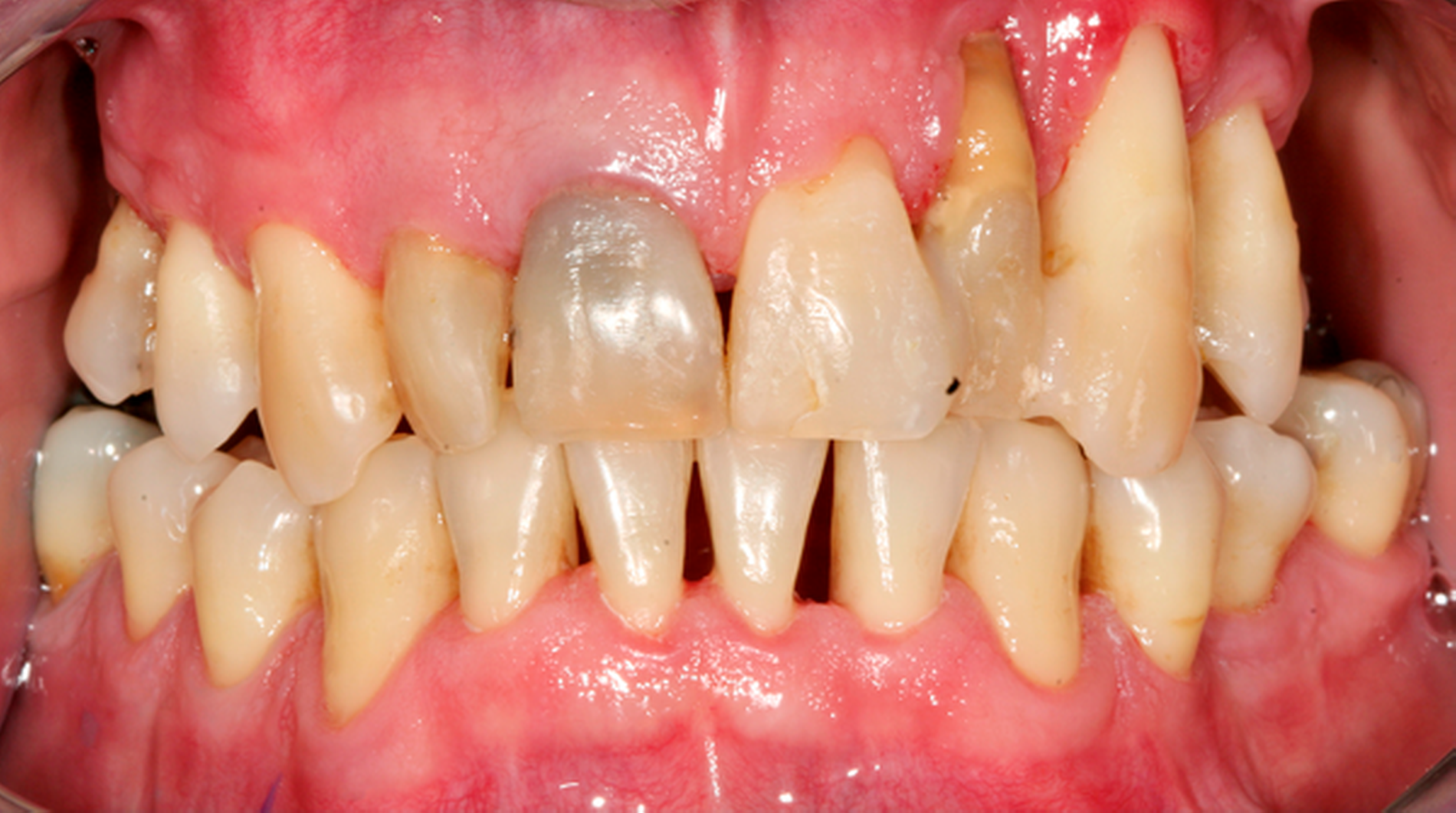
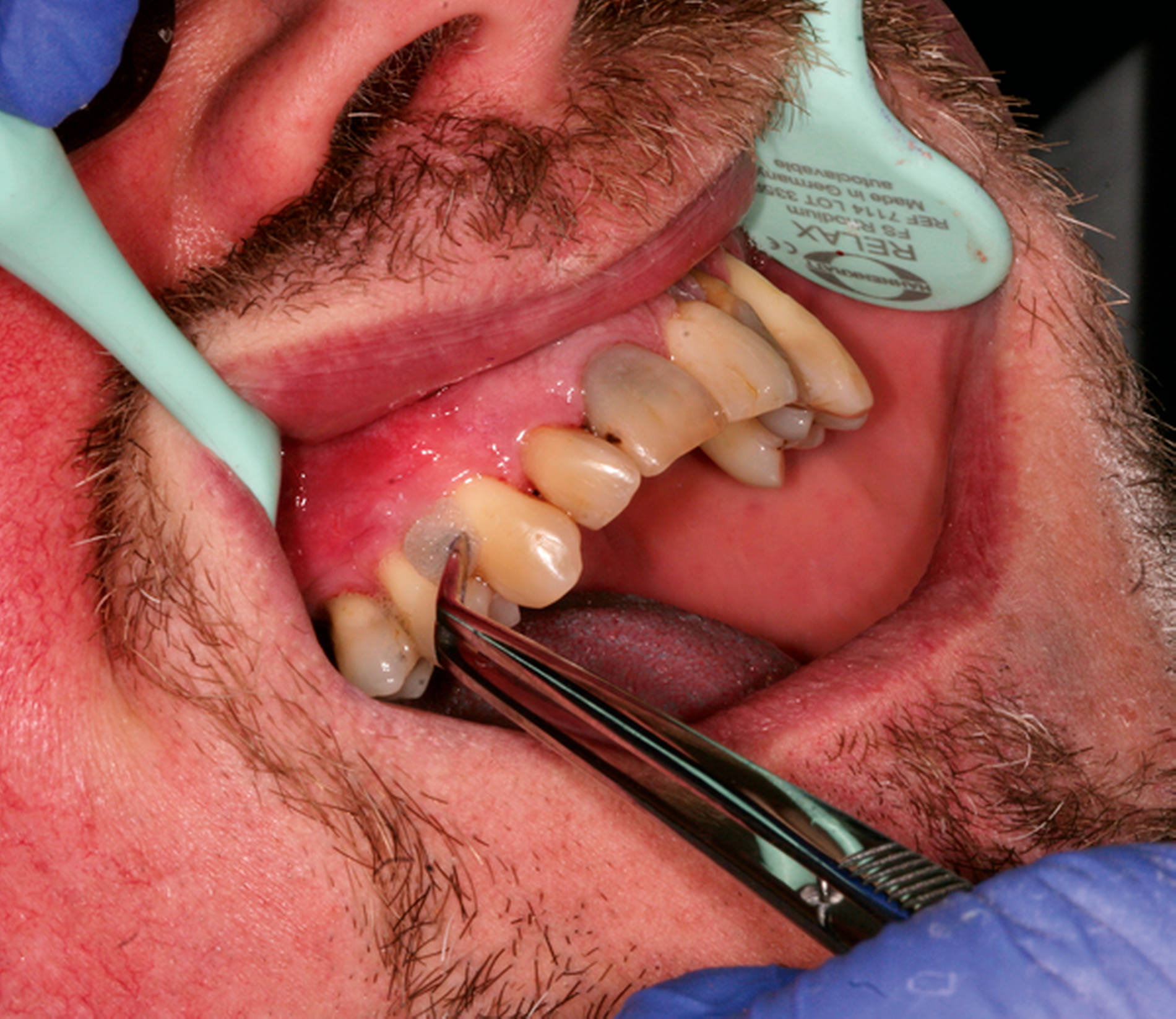
Abb. 1: Interventionen zur Instruktion und Motivation des häuslichen supragingivalen Biofilmmanagments im Rahmen einer UPT-Sitzung: Der 50-jährige Patient befindet sich im dritten Jahr nach der zweiten Therapiestufe und hat ein reduziertes, aber gesundes Parodont.
Häufig können – beispielsweise bei Patienten mit Parodontitis Stadium III oder IV – nicht alle Therapieziele vollständig bei allen Zähnen realisiert werden. Deshalb müssen unter Berücksichtigung der wissenschaftlichen Evidenz individuelle Interventionen in der UPT ergriffen werden, die abhängig vom gingivalen und parodontalen Status sind und dabei die präventiven und therapeutischen Interventionen aus der ersten und der zweiten Therapiestufe kombinieren. Diese professionellen Maßnahmen müssen durch eine Aufrechterhaltung der Motivation zur kontinuierlichen Mitarbeit der Patienten flankiert werden. Das bedingt eine regelmäßige, individuell an die Bedürfnisse des Patienten angepasste Betreuung.
Ziel der vierten Therapiestufe ist, die parodontale Stabilität aufrechtzuerhalten. Die UPT ist dennoch keine „passive“ Therapiestufe, denn bei jeder UPT-Sitzung und bei jedem Patienten kann ein Wiederauftreten der Erkrankung eine erneute Therapie nötig werden lassen, was eine kontinuierliche Kontrolle der parodontalen Situation und entsprechend abgestimmte Interventionen nach sich zieht.
Vorüberlegungen zu den klinischen Empfehlungen
Für die nachfolgenden Empfehlungen ist zu beachten, dass die Parodontitispatienten nach Abschluss der ersten drei Therapiestufen in zwei diagnostische Gruppen unterteilt werden können (Tabelle 1):
mit reduziertem, aber gesundem Parodont oder
mit gingivaler Entzündung [Caton et al., 2018; Chapple et al., 2018].
In beiden Fällen muss mittels der spezifisch angepassten UPT aus der Kombination von präventiven und therapeutischen Maßnahmen das Risiko eines Rezidivs oder einer Progression abgefangen werden. Hierzu zählen die Bewertung und Überwachung der systemischen und der parodontalen Gesundheit, die Stärkung der Mundhygieneinstruktionen, patientenspezifische Verhaltensanweisungen, die Patientenmotivation zur kontinuierlichen Kontrolle von Risikofaktoren, die professionelle mechanische Plaquereduktion (PMPR) und die lokalisierte subgingivale Instrumentierung bei Resttaschen.
Die professionellen Interventionen benötigen ein strukturiertes Recall-System mit Besuchen von etwa 45 bis 60 Minuten, die an den Bedarf des einzelnen Patienten individuell angepasst sind. Dabei sollte beachtet werden, dass weder eine Über- noch eine Untertherapie erfolgt, weshalb die UPT-Intervalle in Abständen von drei bis maximal zwölf Monaten geplant werden sollten (Konsensbasierte Empfehlung 4.1 mit starkem Konsens der Leitliniengruppe) und fortlaufend individuell an das Risikoprofil und den parodontalen Status des Patienten angepasst werden [Polak et al., 2020; Ramseier et al., 2019; Sanz et al., 2015; Trombelli et al., 2015; Trombelli et al., 2020]. Die Empfehlung, den Patienten zur Einhaltung seiner UPT-Intervalle zu motivieren, fand ebenfalls einen starken Konsens (Konsensbasierte Empfehlung 4.2), da dies für die parodontale Langzeitstabilität und mögliche weitere Verbesserungen des parodontalen Zustands von entscheidender Bedeutung ist [Costa et al., 2014; Sanz et al., 2015; Trombelli et al., 2015]. Zusätzliche Strategien zur Motivation werden analog den entsprechenden Empfehlungen der ersten Therapiestufe eingesetzt.
1. Intervention: Häusliche Kontrolle des supragingivalen dentalen Biofilms
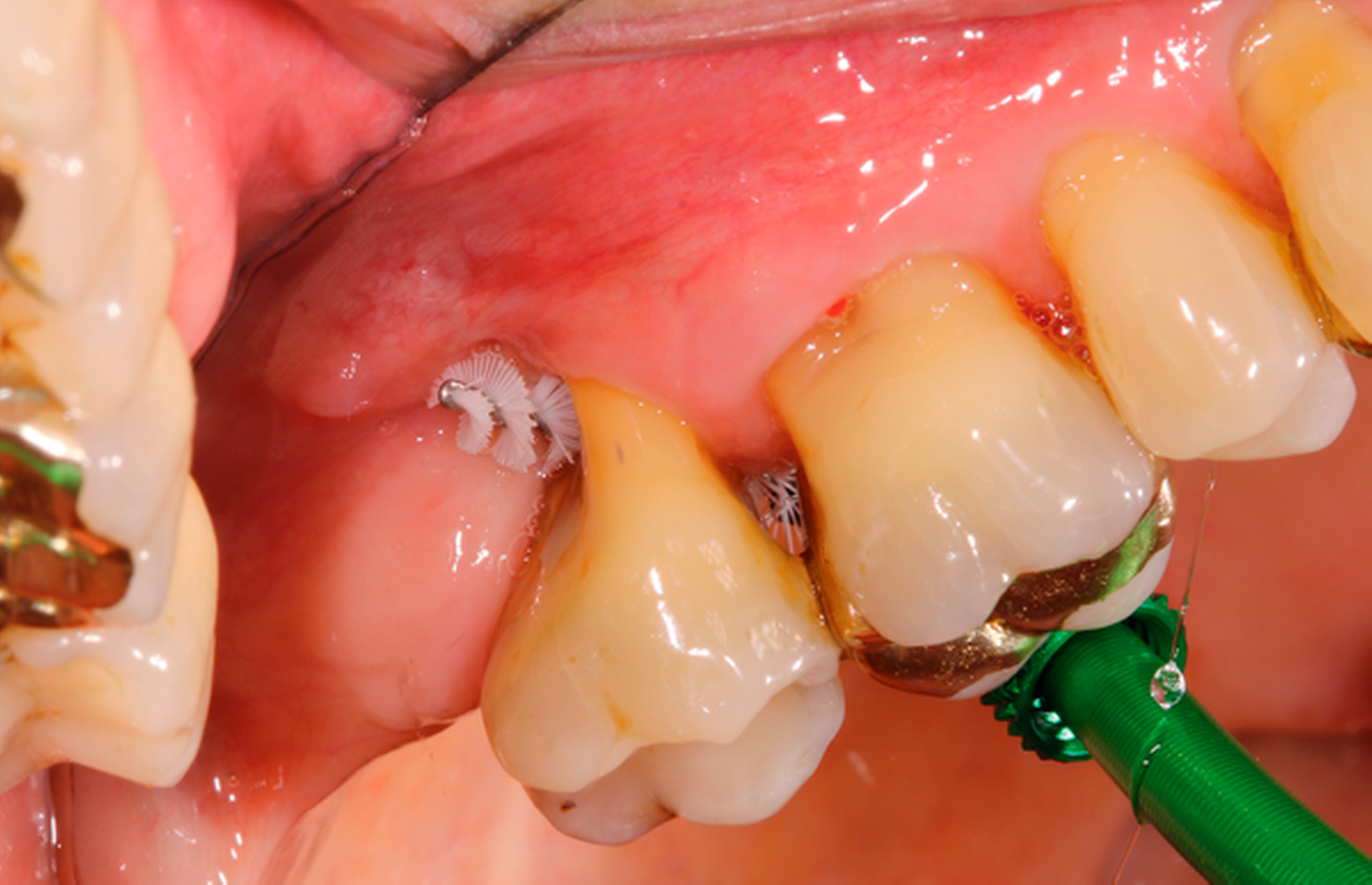
Die Empfehlungen für die Intervention in der vierten Stufe sind analog denen aus der ersten Stufe zu formulieren. Die häusliche mechanische Entfernung des Biofilms bildet die Grundlage der Behandlung einer gingivalen Entzündung. Alle Zahnflächen, die der Bildung des oralen Biofilms ausgesetzt sind, müssen effektiv mechanisch gereinigt werden. Einige können aber selbst unter optimalen Bedingungen nicht durch Zahnbürsten erreicht werden. Deshalb ist zum Erhalt der Gesundheit der interproximalen Gingiva die interdentale Reinigung unerlässlich – insbesondere im Rahmen der sekundären Prävention.
Beachtet werden sollte aber, dass bei einzelnen Empfehlungen der Mangel oder das Fehlen von Evidenz nicht gleichzusetzen ist mit einer fehlenden Wirksamkeit der Produkte. Es sollten immer die Methoden und Instrumente gewählt werden, die den Fertigkeiten und Präferenzen des Patienten entsprechen (Kompromisslösung), da die Akzeptanz durch den Patienten für den dauerhaften Nutzen in einer fortwährenden UPT entscheidend ist [Steenackers et al., 2001]. Um Traumatisierungen durch einen unsachgemäßen Gebrauch der Hilfsmittel zu vermeiden, ist eine fortlaufende individuelle Anleitung und Anpassung an die jeweilige Situation unerlässlich.
2. Intervention: Adjuvante Therapien bei gingivaler Entzündung
Als Teil eines personalisierten Therapieansatzes kann in bestimmten Fällen das mechanische Biofilmmanagement durch ergänzende Maßnahmen begleitet werden. Um eine gingivale Entzündung in der UPT unter Kontrolle zu halten, wurde der Gebrauch von verschiedenen Zusatzmitteln vorgeschlagen. Dazu zählen zumeist antimikrobielle Wirkstoffe in Form von Zahnpasten oder Mundspüllösungen oder in Kombination von beidem. Die begleitende Anwendung von antimikrobiellen Wirkstoffen wurde nur für die speziellen Fälle vorgeschlagen, wenn Patienten trotz intensiver Bemühungen nicht in der Lage sind, den supragingivalen Biofilm adäquat und effektiv allein durch mechanische Zahnreinigung zu entfernen.
Aufgrund fehlender Evidenz darf dies aber nicht auf die Bevölkerungsebene verallgemeinert werden, sondern sollte Teil des personalisierten Ansatzes der Patientenversorgung sein. Beurteilen Sie lokale Faktoren (wie Erreichbarkeit für die Reinigung) und allgemeine Faktoren (wie Allgemeingesundheit, Gebrechlichkeit oder manuelles Geschick / höheres Lebensalter). Andererseits sollten in der Empfehlung an den Patienten auch dessen Präferenzen (Kosten, Geschmack) und etwa zu erwartende ungewollte Nebenwirkungen (Zahnverfärbung, brennendes Gefühl bei Verwendung) berücksichtigt werden. Die anzuwendenden Interventionen entsprechen denen in der ersten Therapiestufe.
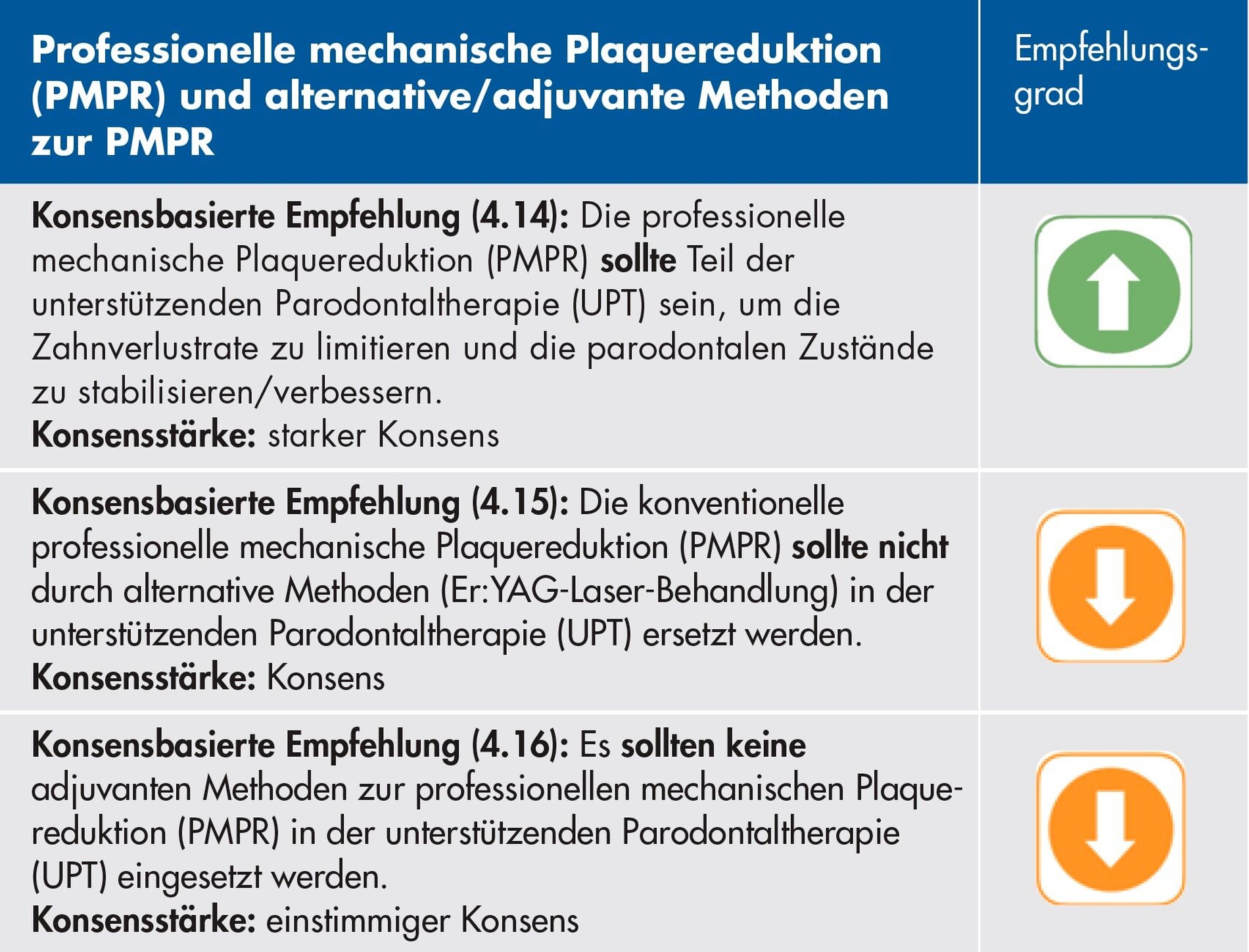
3. Intervention: Professionelle mechanische Plaquereduktion (PMPR)
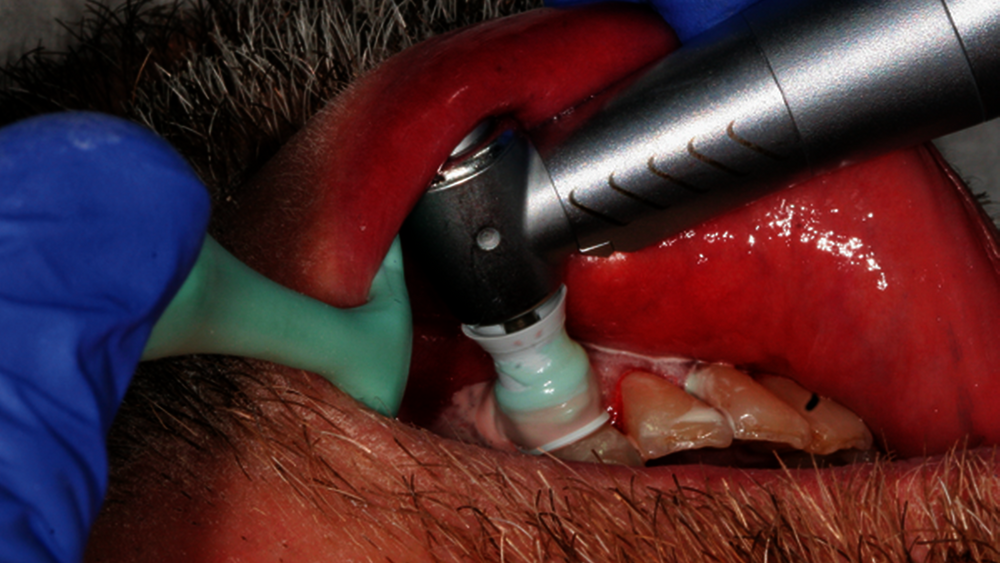
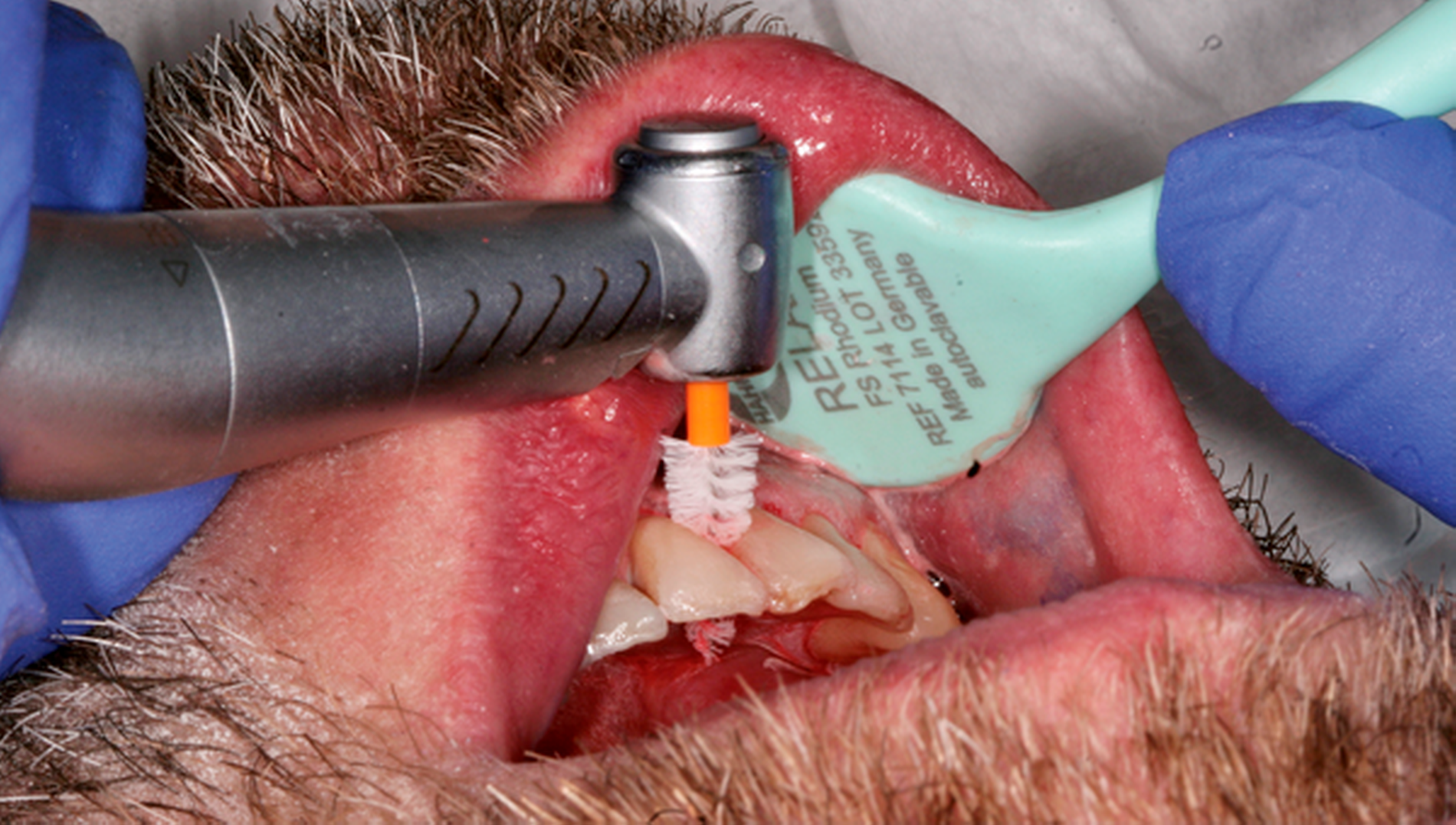
Als zentraler Bestandteil einer regelmäßig durchgeführten UPT ist die professionelle mechanische Plaquereduktion (PMPR) mit dafür verantwortlich, dass kurz- und auch langfristig nachweislich geringere Zahnverlustraten und geringere Änderungen des klinischen Attachmentlevels (CAL) erreicht werden können [Heasman et al., 2002; Trombelli et al., 2015]. Es muss aber beachtet werden, dass in den meisten Studien die PMPR in der UPT in Kombination mit anderen Interventionen (zum Beispiel wiederholte Mundhygieneinstruktionen, zusätzliche aktive Therapie) untersucht wurde, was einen direkten Rückschluss auf deren alleinigen Effekt für den Zahnerhalt und die Stabilität der parodontalen Zustände sowie deren Einflussgröße erschwert [Trombelli et al., 2015].
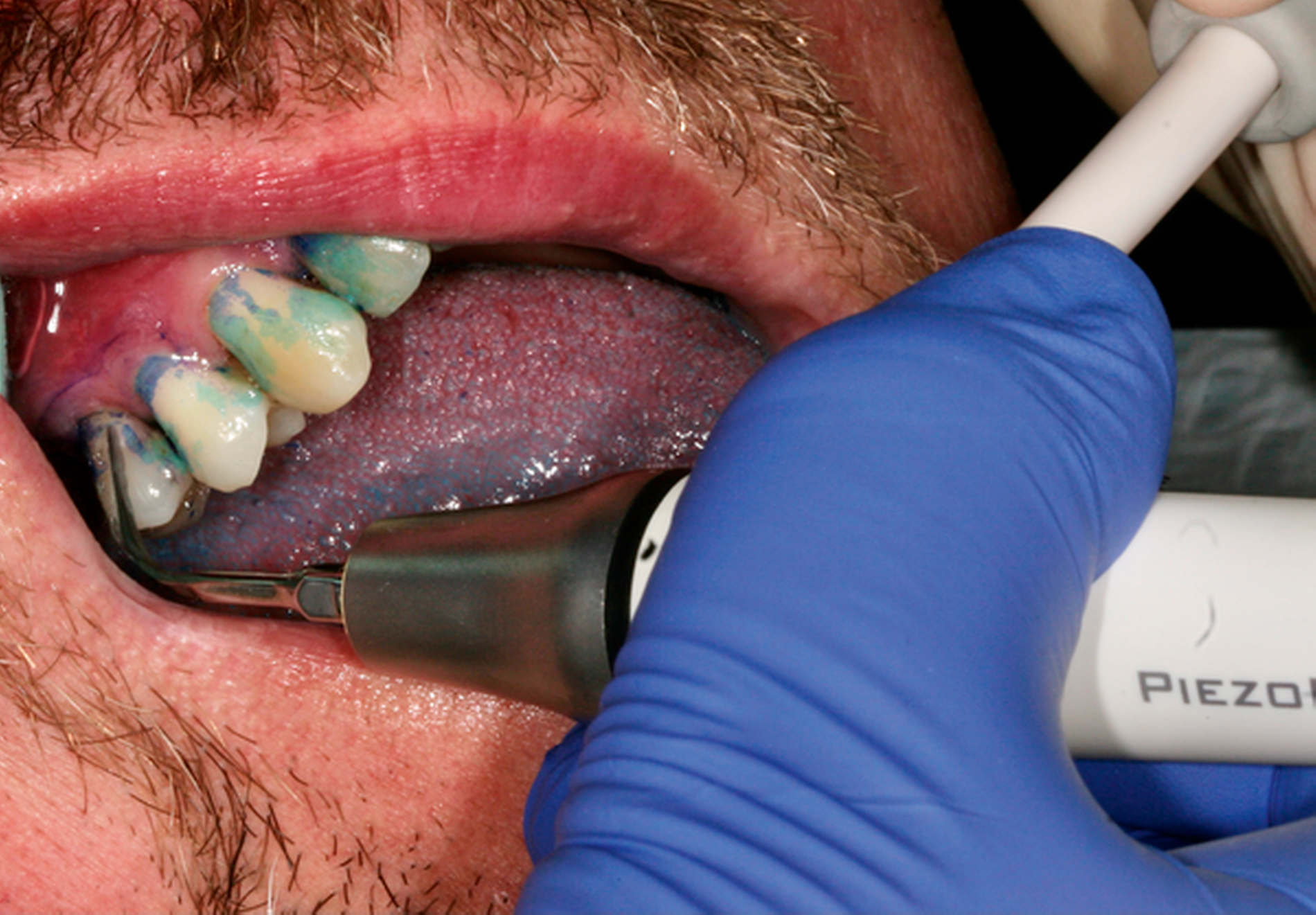
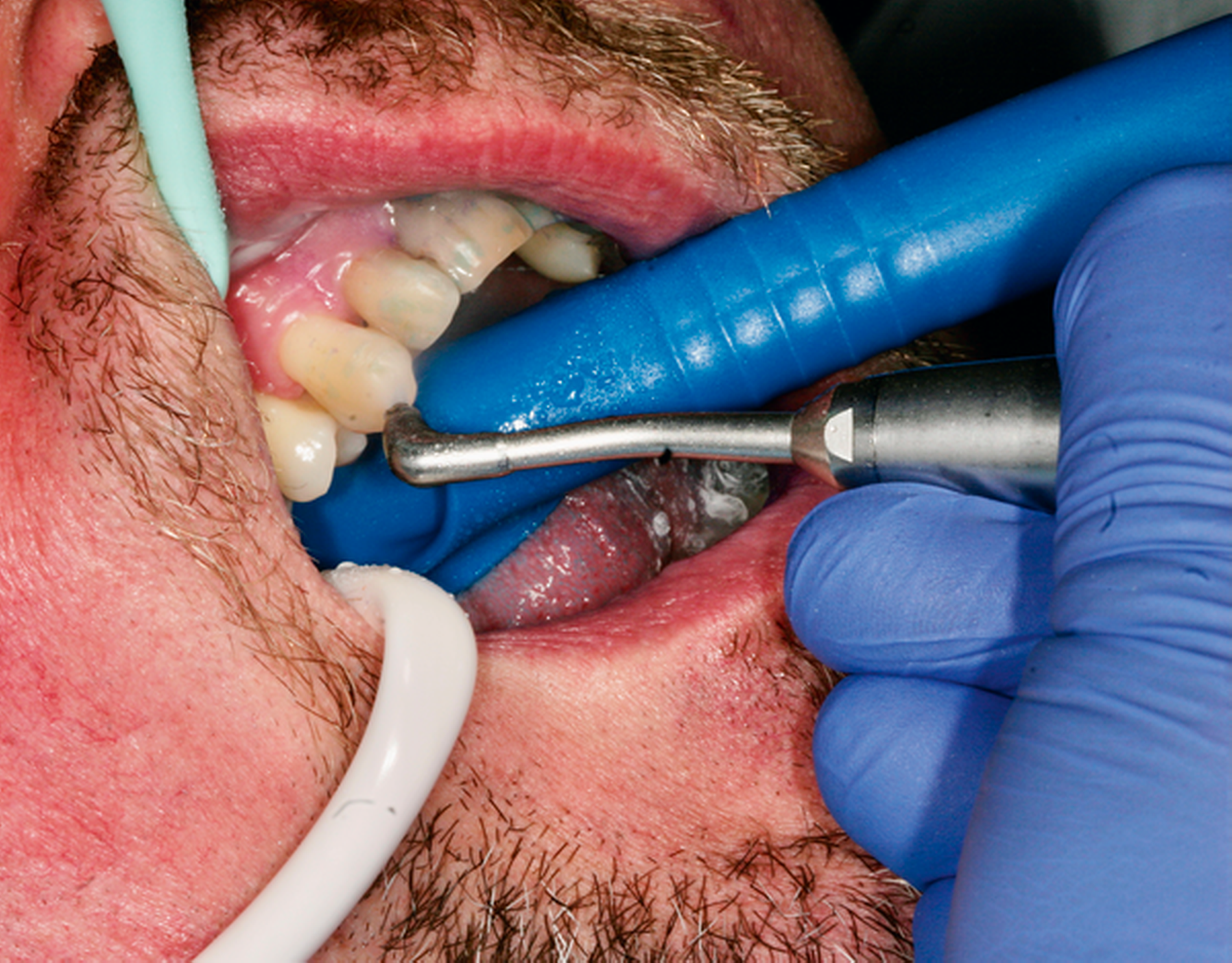
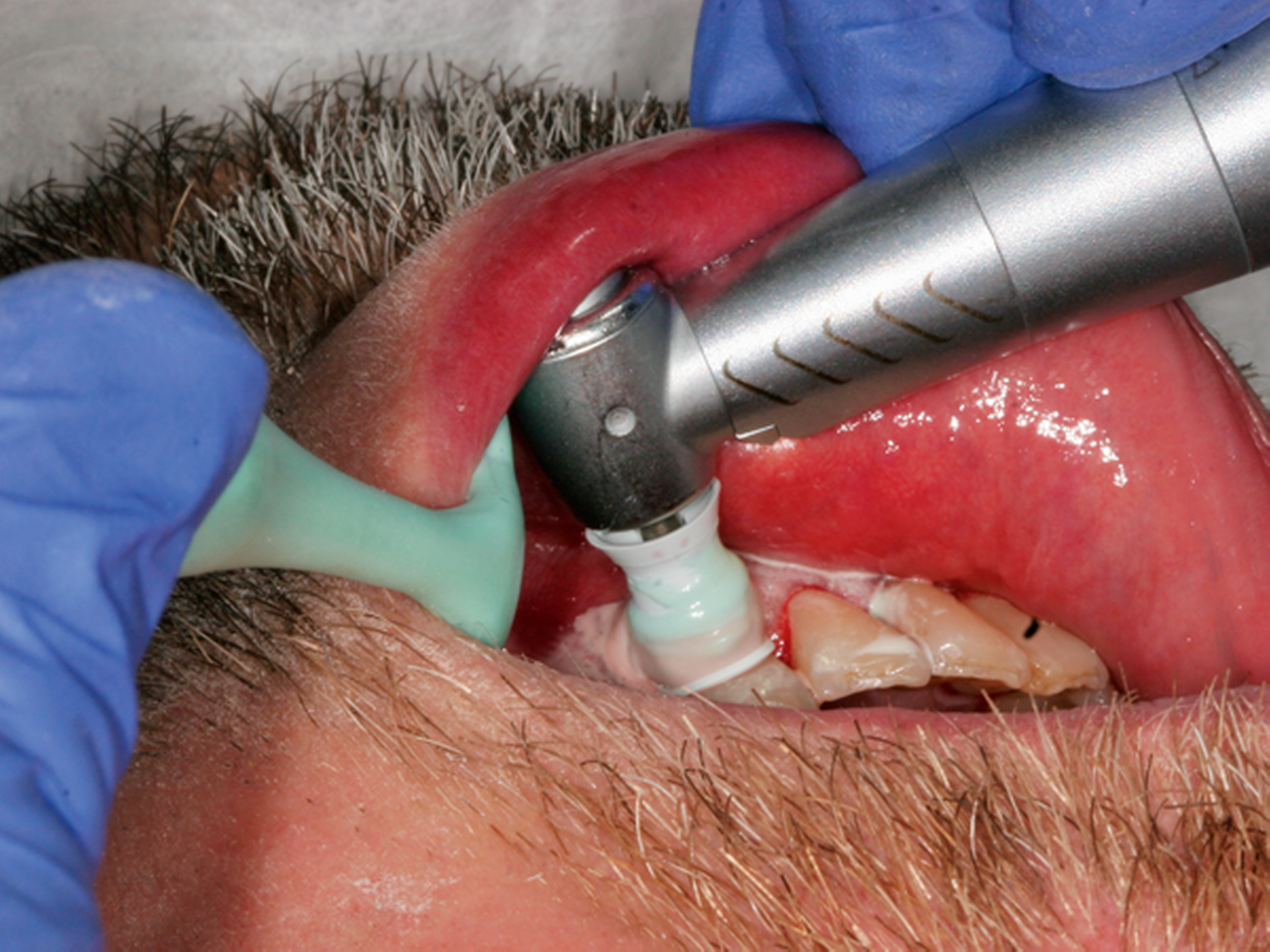
Abb. 2: Professionelle mechanische Plaquereduktion während einer UPT-Sitzung bei einem 50-jährigen Patienten mit reduziertem, aber gesundem Parodont im dritten Jahr nach zweiter Therapiestufe:
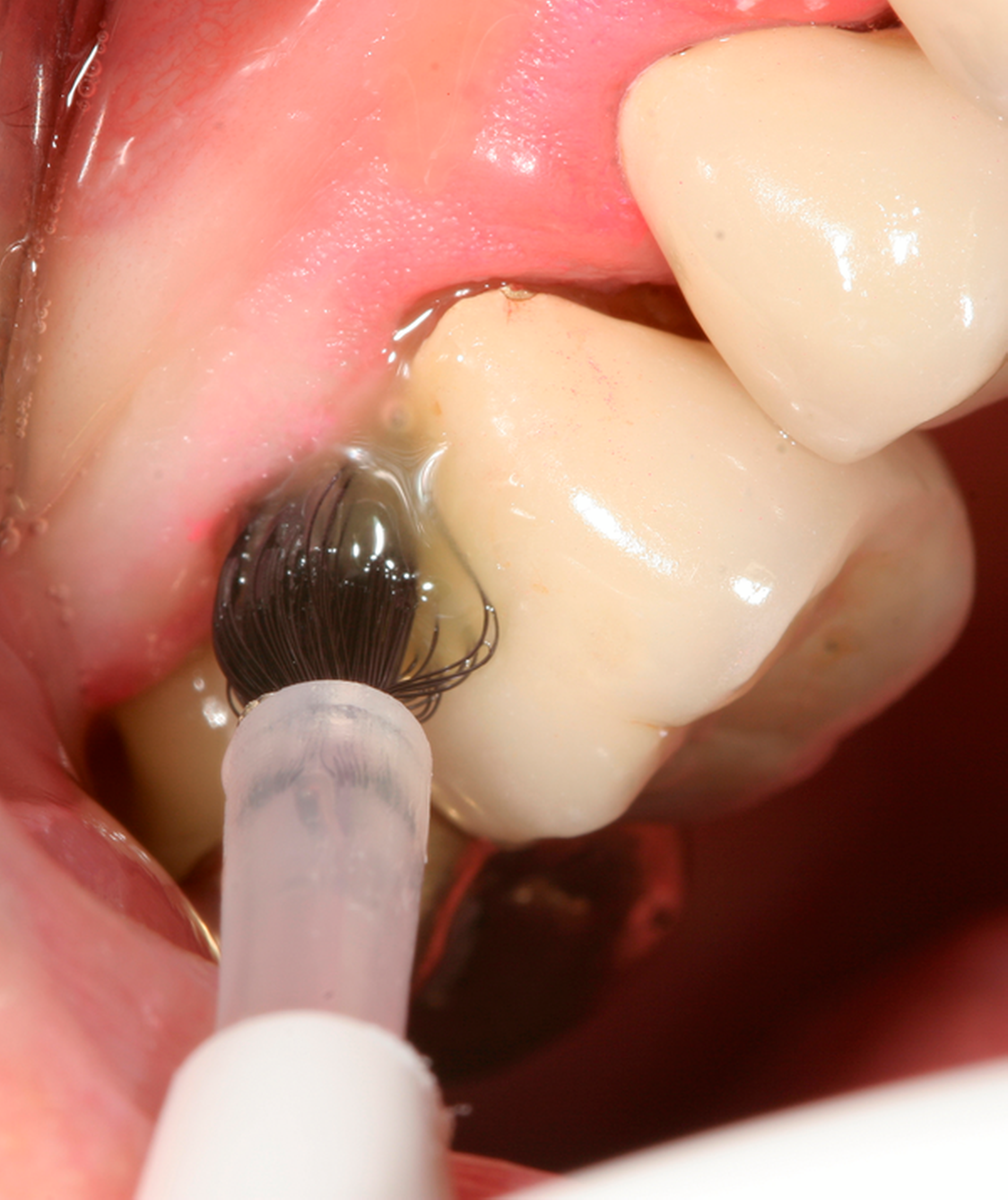
Weiterhin sollte bei der Betrachtung der Empfehlungen zu adjuvanten Maßnahmen zur PMPR – wie der antimikrobiellen Photodynamischen Therapie (aPDT) oder alternativer Verfahren wie der Er:Yag-Laseranwendung – beachtet werden, dass sich in der zugrunde liegenden systematischen Analyse von klinischen Studien von Trombelli et al. für diese Verfahren keine größeren klinischen Effekte nachweisen ließen [Trombelli et al., 2020].
Eine vorhergehende spezifische systematische Analyse zur aPDT aus dem Jahr 2017 von elf klinischen Studien konnte zumindest kurzfristig (drei Monate) eine zusätzliche Taschenreduktion von 0,12 mm zur PMPR nachweisen [Xue et al., 2017]. Unberücksichtigt blieben in all diesen Untersuchungen aber relevante Betrachtungen zur Kosten-Nutzen- und Kosten-Effektivität-Relation. Auch ist der Zulassungsstatus der bei der aPDT verwendeten Farbstoffe/Photosensitizer in Deutschland für die subgingivale Applikation unklar und subantimikrobielles Doxycyclin (SDD) besitzt in Deutschland gar keine Zulassung, weshalb eine modifizierte Empfehlung 4.16 erfolgte.
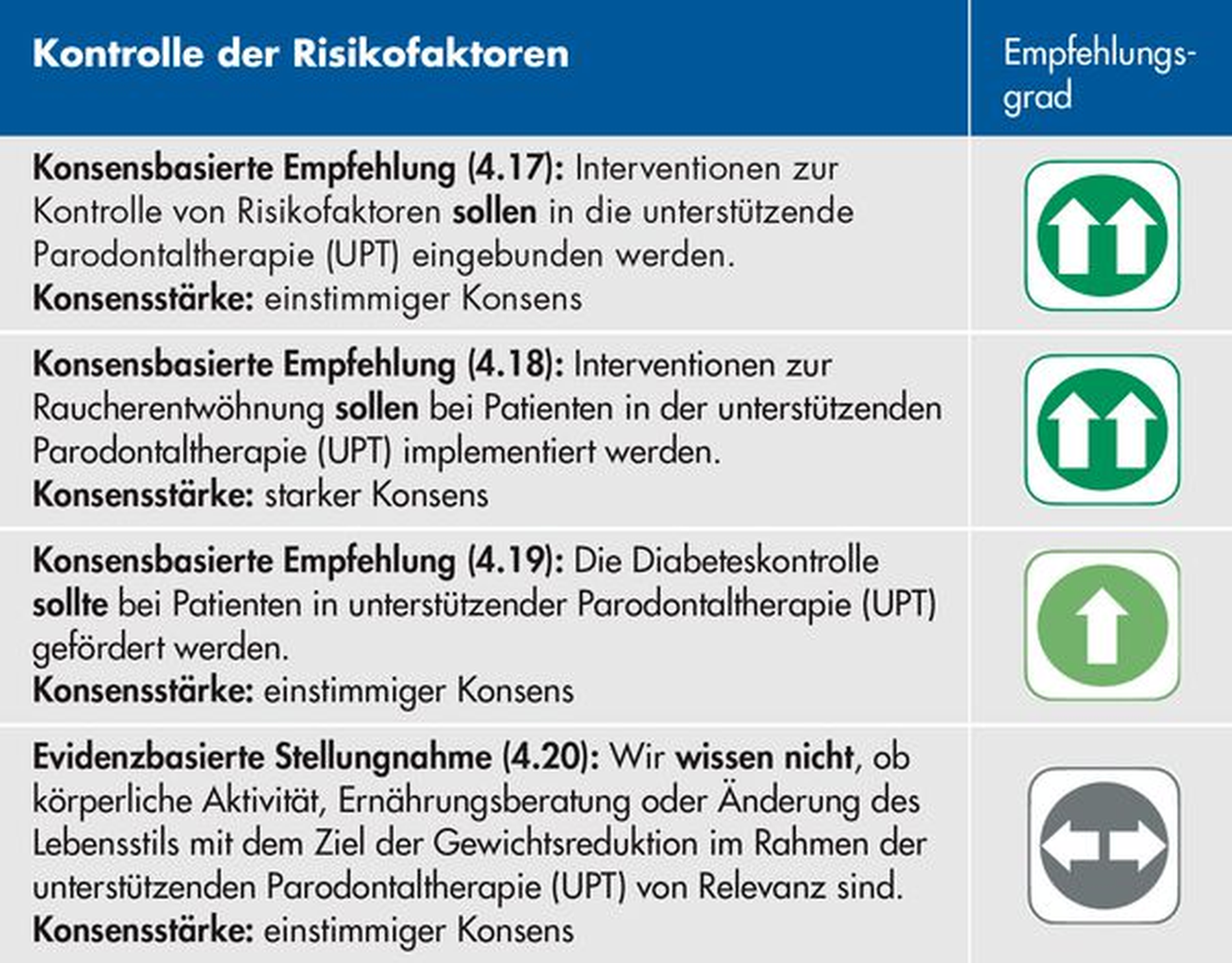
4. Intervention: Kontrolle der Risikofaktoren
Wie bereits für die erste Therapiestufe ausführlich erläutert (zm 6, 7, 8/2021), profitieren Parodontitispatienten hinsichtlich ihrer parodontalen Stabilität von zusätzlichen Maßnahmen (wie einer Überweisung zur weiterführenden Beratung oder einer Pharmakotherapie zur Kontrolle ihrer Risikofaktoren Rauchen und Diabetes mellitus), die schrittweise und individuell an die Bedürfnisse des Patienten angepasst empfohlen werden sollen [Ramseier et al., 2020]. Hingegen sind weitere Forschungsaktivitäten notwendig zur Spezifikation der Form der Patientenaufklärung/-interaktion, wie zum Beispiel diese speziell auf das Alter und den allgemeinen Gesundheitszustand auszurichten [Ramseier et al., 2020; Billings et al., 2018].
Fazit
Zusammenfassend sei betont, dass all diese vielfältigen Interventionen im Rahmen der UPT nur optimalen Nutzen entfalten können, wenn sie risikobasiert und individuell an die Bedürfnisse des Patienten angepasst werden. Das betrifft auch die patientenindividuelle Anpassung der Recallintervalle im Rahmen einer strukturiert angelegten Nachsorge. In der Literatur konnte gezeigt werden, dass eine regelmäßige UPT im Vergleich zur unregelmäßig durchgeführten UPT mit einem geringeren Zahnverlust assoziiert ist [Fardal und Grytten, 2014]. Die Stabilität der parodontalen Verhältnisse muss immer wieder neu zusammen mit dem Patienten und einem engagierten zahnärztlichen Team erarbeitet werden – die UPT ist ein unverzichtbarer und entscheidender Erfolgsfaktor für die gesamte Parodontitistherapie.
PD Dr. med. dent. Christian Graetz
Klinik für Zahnerhaltungskunde und Parodontologie,
Universitätsklinikum Schleswig-Holstein
Arnold-Heller-Str. 3 (Haus 26), 24105 Kiel
Prof. Dr. Moritz Kebschull
Chair of Restorative Dentistry The School of Dentistry, University of Birmingham
5 Mill Pool Way, Edgbaston
Birmingham B5 7EG, England
moritz@kebschull.me
Prof. Dr. Bettina Dannewitz
Gemeinschaftspraxis Dres. Dannewitz & Glass
Langgasse 36-38, 35781 Weilburg
und
Poliklinik für Parodontologie, Zentrum der Zahn-, Mund- und Kieferheilkunde (Carolinum),
Johann Wolfgang Goethe Universität Frankfurt am Main
Theodor-Stern-Kai 7, 60596 Frankfurt/Main
dannewitz@med.uni-frankfurt.de
Literaturliste
Billings, M., Holtfreter, B., Papapanou, P. N., Mitnik, G. L., Kocher, T. & Dye, B. A. (2018) Age-dependent distribution of periodontitis in two countries: Findings from NHANES 2009 to 2014 and SHIP-TREND 2008 to 2012. J Clin Periodontol 45 Suppl 20, S130-S148. doi:10.1111/jcpe.12944.
Caton, J. G., Armitage, G., Berglundh, T., Chapple, I. L. C., Jepsen, S., Kornman, K. S., Mealey, B. L., Papapanou, P. N., Sanz, M. & Tonetti, M. S. (2018) A new classification scheme for periodontal and peri-implant diseases and conditions - Introduction and key changes from the 1999 classification. J Periodontol 89 Suppl 1, S1-S8. doi:10.1002/JPER.18-0157.
Chapple, I. L. C., Mealey, B. L., Van Dyke, T. E., Bartold, P. M., Dommisch, H., Eickholz, P., Geisinger, M. L., Genco, R. J., Glogauer, M., Goldstein, M., Griffin, T. J., Holmstrup, P., Johnson, G. K., Kapila, Y., Lang, N. P., Meyle, J., Murakami, S., Plemons, J., Romito, G. A., Shapira, L., Tatakis, D. N., Teughels, W., Trombelli, L., Walter, C., Wimmer, G., Xenoudi, P. & Yoshie, H. (2018) Periodontal health and gingival diseases and conditions on an intact and a reduced periodontium: Consensus report of workgroup 1 of the 2017 World Workshop on the Classification of Periodontal and Peri-Implant Diseases and Conditions. J Clin Periodontol 45 Suppl 20, S68-S77. doi:10.1111/jcpe.12940.
Costa, F. O., Lages, E. J., Cota, L. O., Lorentz, T. C., Soares, R. V. & Cortelli, J. R. (2014) Tooth loss in individuals under periodontal maintenance therapy: 5-year prospective study. J Periodontal Res 49, 121-128. doi:10.1111/jre.12087.
Fardal, O. & Grytten, J. (2014) Applying quality assurance in real time to compliant long-term periodontal maintenance patients utilizing cost-effectiveness and cost utility. J Clin Periodontol 41, 604-611. doi:10.1111/jcpe.12252.
Heasman, P. A., McCracken, G. I. & Steen, N. (2002) Supportive periodontal care: the effect of periodic subgingival debridement compared with supragingival prophylaxis with respect to clinical outcomes. J Clin Periodontol 29 Suppl 3, 163-172; discussion 195-166. doi:10.1034/j.1600-051x.29.s3.9.x.
Polak, D., Wilensky, A., Antonoglou, G. N., Shapira, L., Goldstein, M. & Martin, C. (2020) The Efficacy of Pocket Elimination/Reduction Compared to Access Flap Surgery: A Systematic Review and Meta-analysis. J Clin Periodontol. doi:10.1111/jcpe.13246.
Pretzl, B., Wiedemann, D., Cosgarea, R., Kaltschmitt, J., Kim, T. S., Staehle, H. J. & Eickholz, P. (2009) Effort and costs of tooth preservation in supportive periodontal treatment in a German population. J Clin Periodontol 36, 669-676. doi:10.1111/j.1600-051X.2009.01409.x.
Ramseier, C. A., Nydegger, M., Walter, C., Fischer, G., Sculean, A., Lang, N. P. & Salvi, G. E. (2019) Time between recall visits and residual probing depths predict long-term stability in patients enrolled in supportive periodontal therapy. J Clin Periodontol 46, 218-230. doi:10.1111/jcpe.13041.
Ramseier, C. A., Woelber, J. P., Kitzmann, J., Detzen, L., Carra, M. C. & Bouchard, P. (2020) Impact of risk factor control interventions for smoking cessation and promotion of healthy lifestyles in patients with periodontitis: a systematic review. J Clin Periodontol. doi:10.1111/jcpe.13240.
Sanz, M., Baumer, A., Buduneli, N., Dommisch, H., Farina, R., Kononen, E., Linden, G., Meyle, J., Preshaw, P. M., Quirynen, M., Roldan, S., Sanchez, N., Sculean, A., Slot, D. E., Trombelli, L., West, N. & Winkel, E. (2015) Effect of professional mechanical plaque removal on secondary prevention of periodontitis and the complications of gingival and periodontal preventive measures: consensus report of group 4 of the 11th European Workshop on Periodontology on effective prevention of periodontal and peri-implant diseases. J Clin Periodontol 42 Suppl 16, S214-220. doi:10.1111/jcpe.12367.
Schwendicke, F., Biffar, A. S. & Graetz, C. (2017) Long-term treatment costs for aggressive periodontitis in a German population. J Clin Periodontol 44, 1245-1252. doi:10.1111/jcpe.12814.
Schwendicke, F., Engel, A. S. & Graetz, C. (2018) Long-term treatment costs of chronic periodontitis patients in Germany. J Clin Periodontol 45, 1069-1077. doi:10.1111/jcpe.12984.
Steenackers, K., Vijt, J., Leroy, R., De Vree, H. & De Boever, J. A. (2001) Short-term clinical study comparing supragingival plaque removal and gingival bleeding reduction of the Philips Jordan HP735 to a manual toothbrush in periodontal patients in a maintenance program. J Clin Dent 12, 17-20.
Trombelli, L., Farina, R., Pollard, A., Claydon, N., Franceschetti, G., Khan, I. & West, N. (2020) Efficacy of alternative or additional methods to professional mechanical plaque removal during supportive periodontal therapy: A systematic review and meta-analysis. J Clin Periodontol 47 Suppl 22, 144-154. doi:10.1111/jcpe.13269.
Trombelli, L., Franceschetti, G. & Farina, R. (2015) Effect of professional mechanical plaque removal performed on a long-term, routine basis in the secondary prevention of periodontitis: a systematic review. J Clin Periodontol 42 Suppl 16, S221-236. doi:10.1111/jcpe.12339.
Xue, D., Tang, L., Bai, Y., Ding, Q., Wang, P. & Zhao, Y. (2017) Clinical efficacy of photodynamic therapy adjunctive to scaling and root planing in the treatment of chronic periodontitis: A systematic review and meta-analysis. Photodiagnosis Photodyn Ther 18, 119-127. doi:10.1016/j.pdpdt.2017.01.183.