Herpes-Zoster-assoziierte Osteonekrose des Kiefers
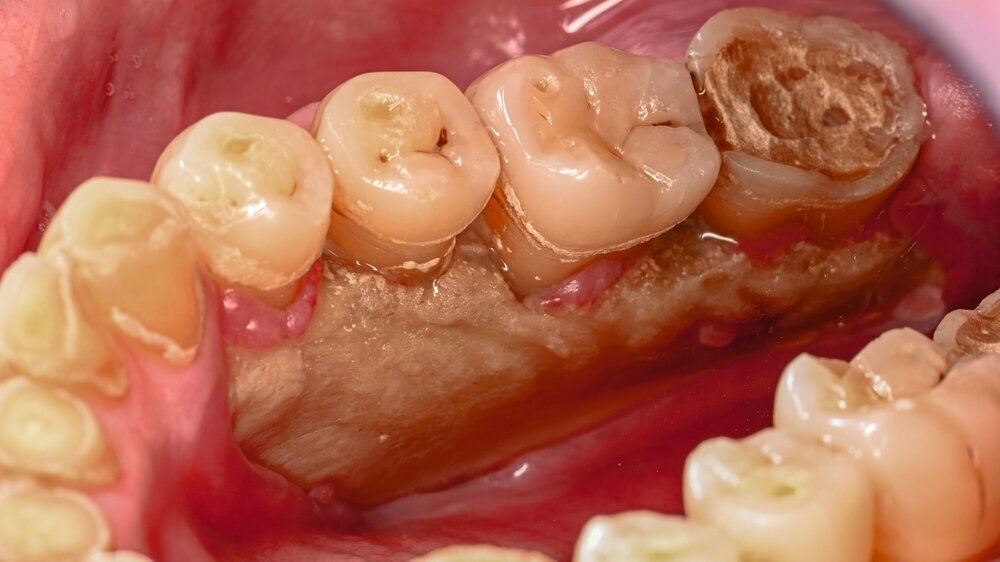
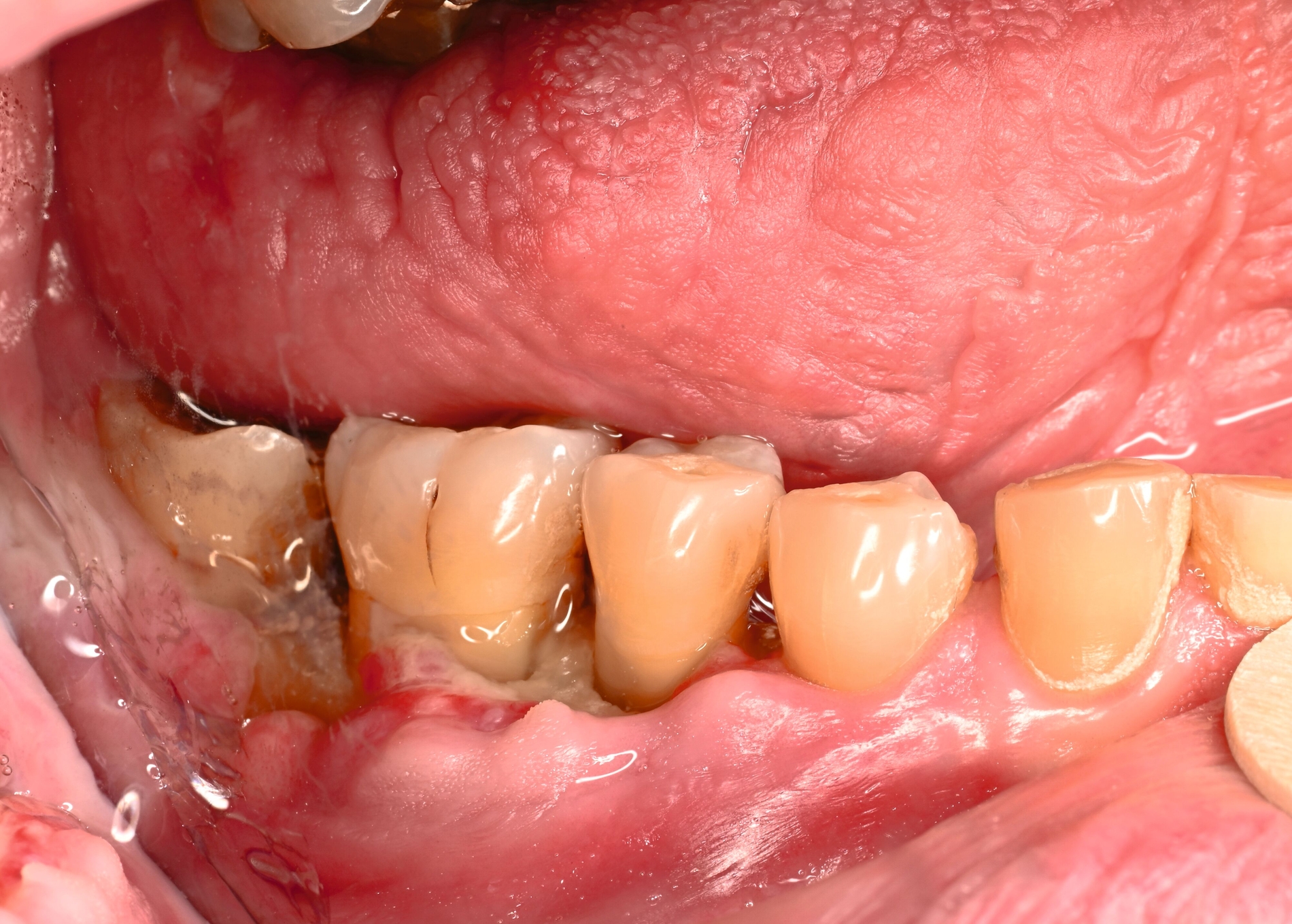
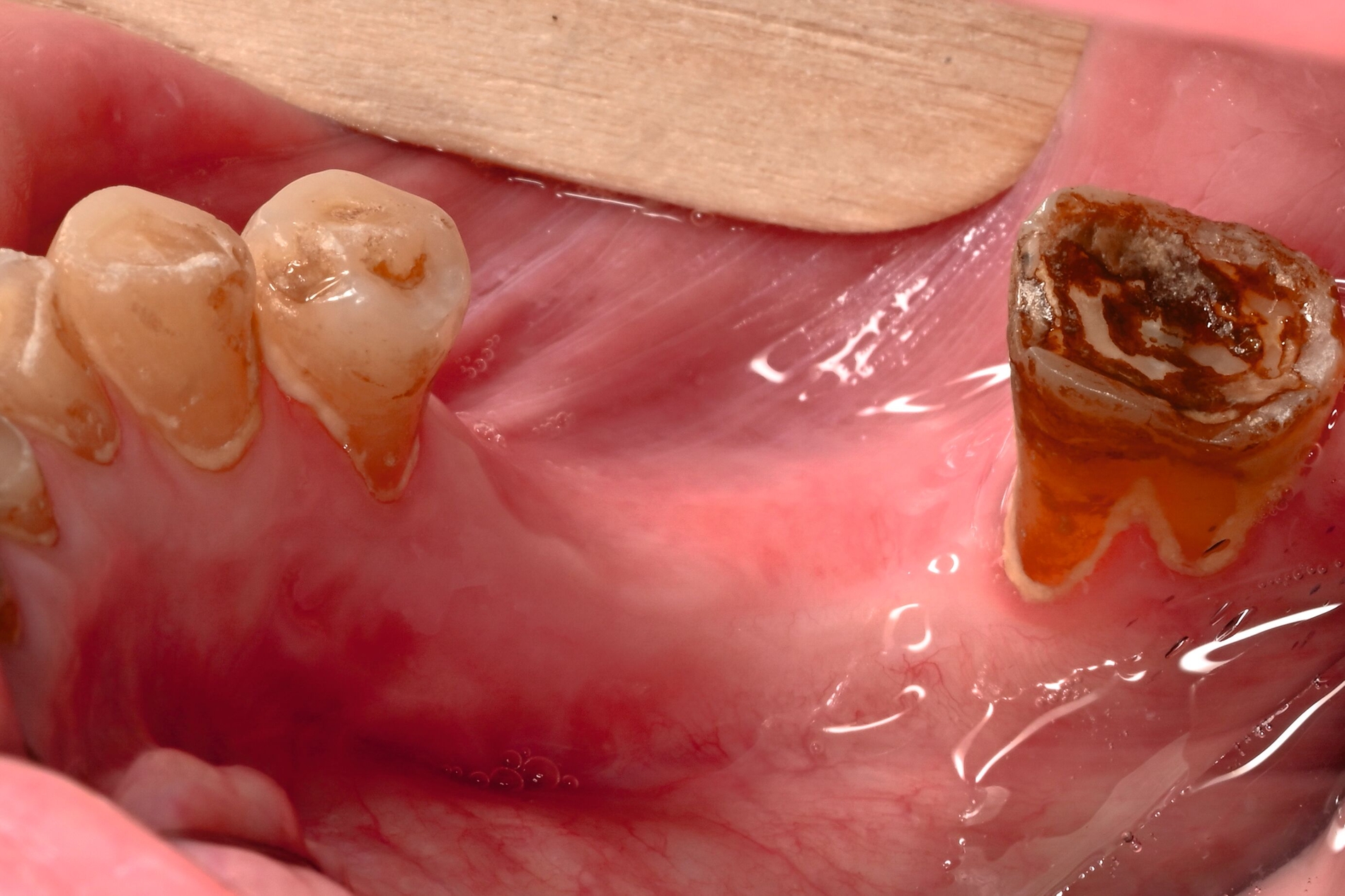
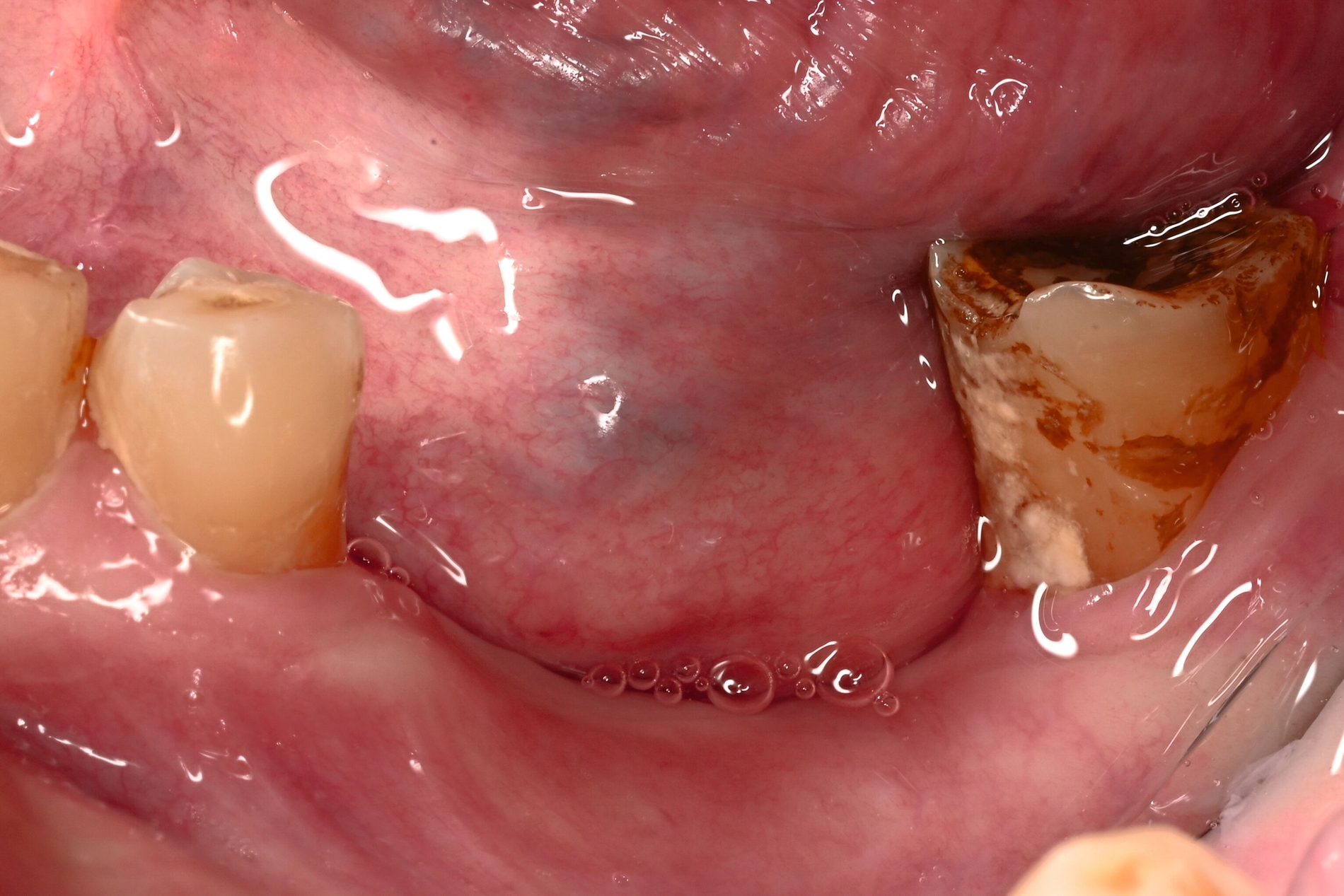
Der Patient stellte sich mit freiliegendem Knochen in Regio 43 bis 47 und mehreren gelockerten Zähnen vor. 45 und 46 waren devital. Als klinische Besonderheit fiel auf, dass sich innerhalb der Nekrosezone kleinflächige Weichgewebsareale darstellten, die in dieser Form bei klassischen Osteonekrosen üblicherweise nicht beobachtet werden. Eine klassische Vincent-Symptomatik bestand nicht. Drei Wochen zuvor war eine Herpes-Zoster-Infektion dermatologisch diagnostiziert und zunächst stationär behandelt worden. Der Patient erhielt eine intravenöse, antivirale Therapie, die bei Entlassung oralisiert wurde.
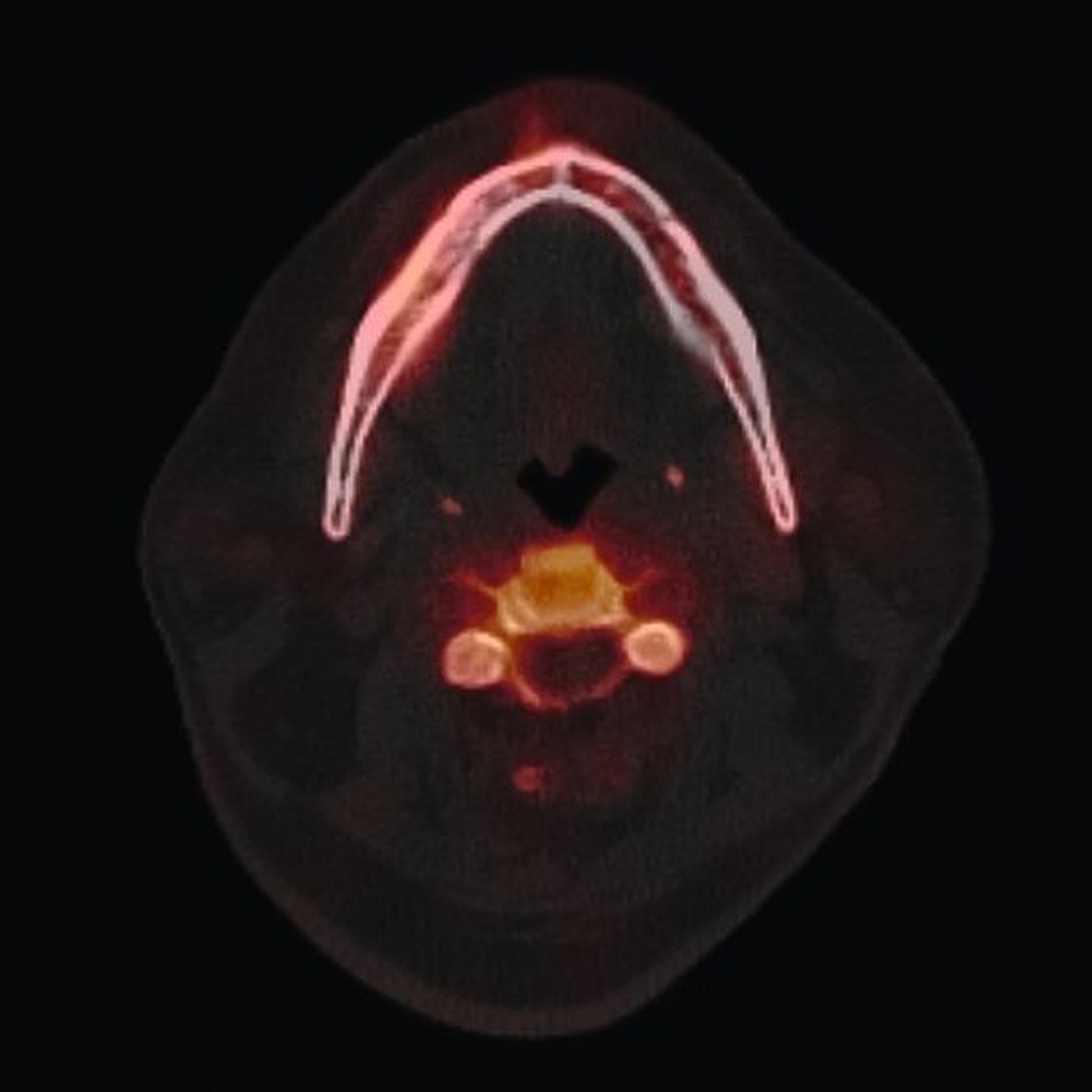
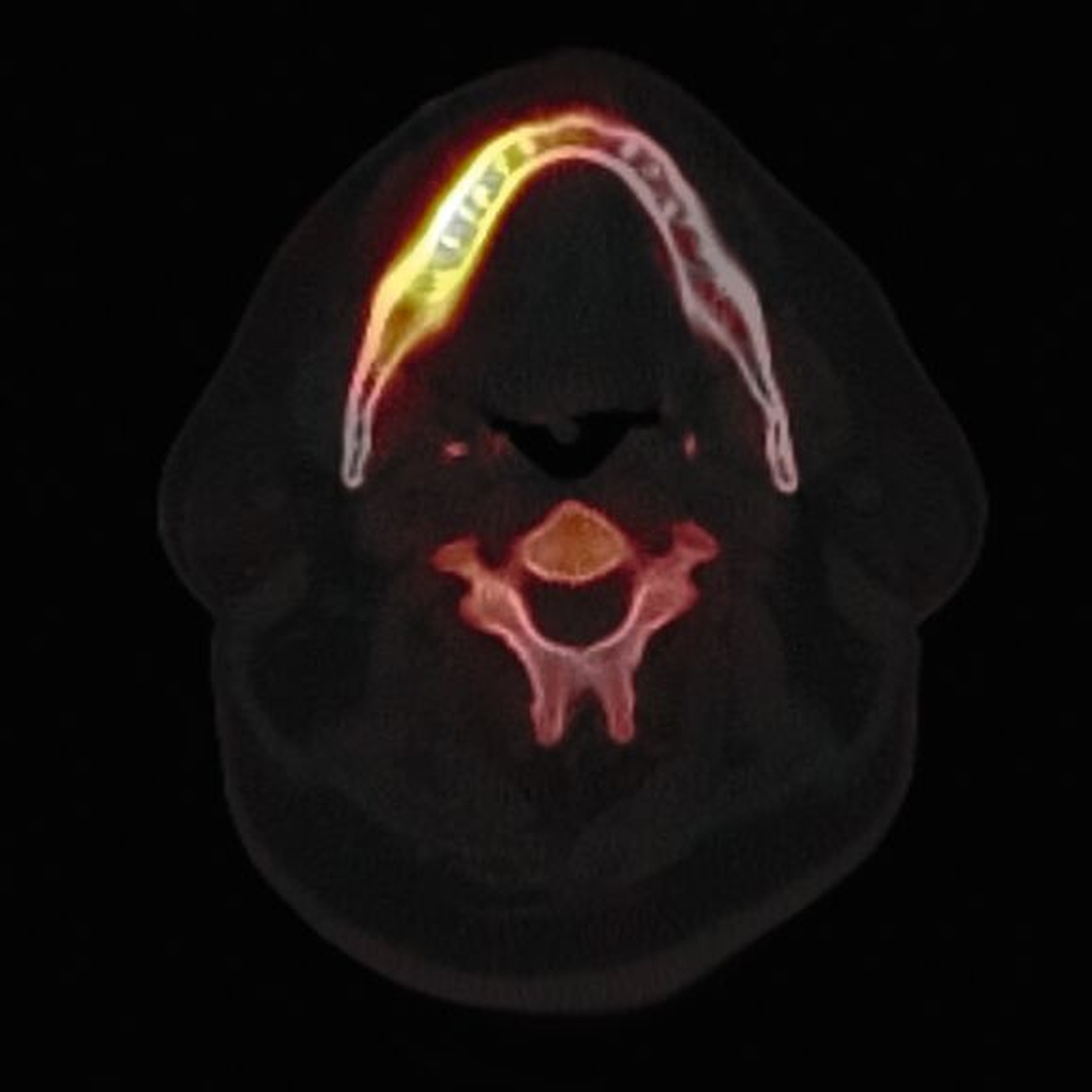
Zum Zeitpunkt der Erstvorstellung in der kieferchirurgischen Ambulanz zeigten sich keine klassischen Herpes-Zoster-Effloreszenzen im Gesicht. Eine antiresorptive Therapie oder Bestrahlung lag nicht vor, sodass eine Herpes-Zoster-assoziierte Osteonekrose im Sinne einer Ausschlussdiagnose festgestellt wurde. Anamnestisch bestand ein gut eingestellter Diabetes mellitus Typ 2 als potenziell immunkompromittierende Grunderkrankung. Die Knochenszintigrafie zeigte eine deutliche Stoffwechselsteigerung im betroffenen Bereich, vereinbar mit einer infizierten Osteonekrose.
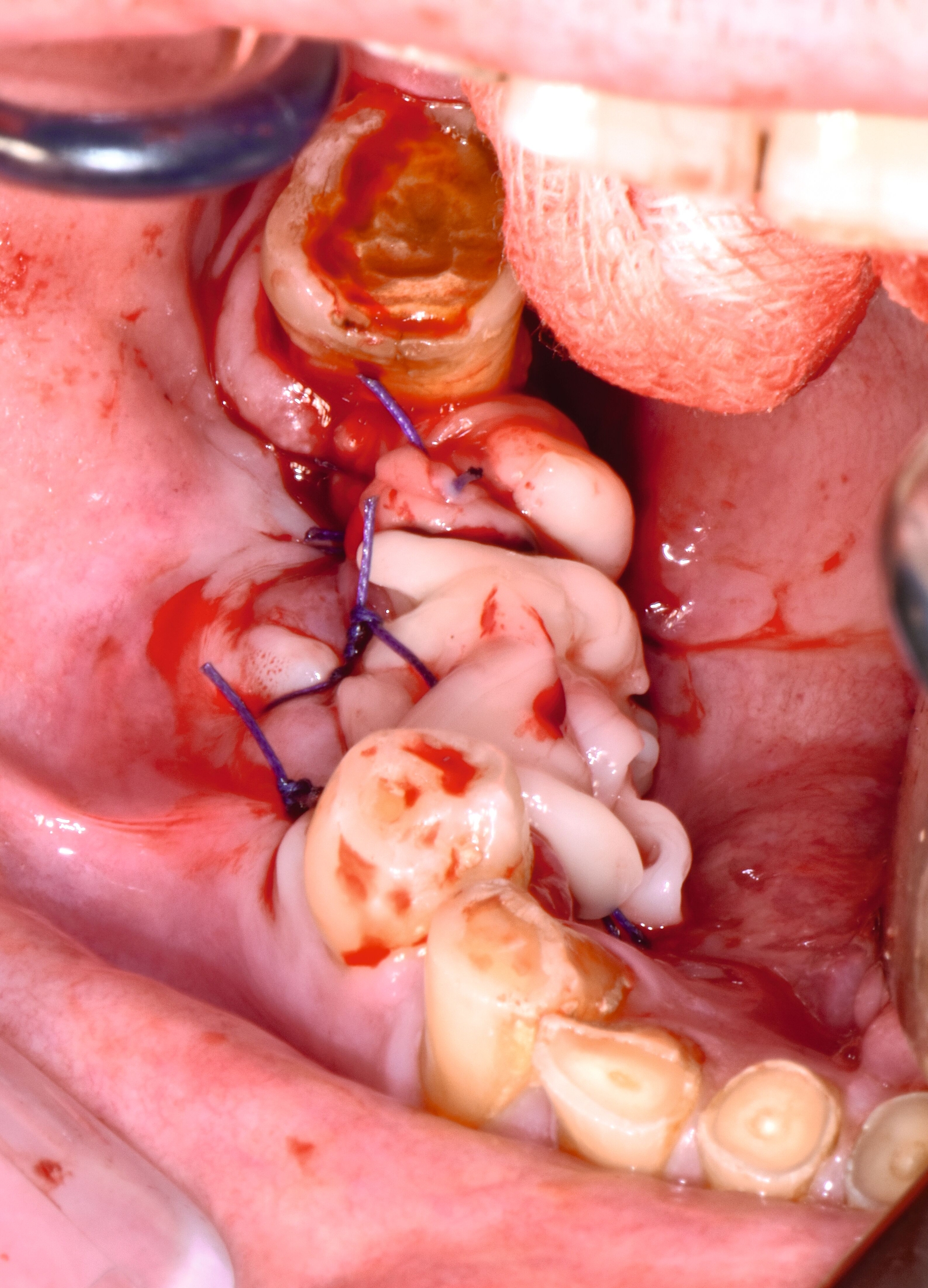
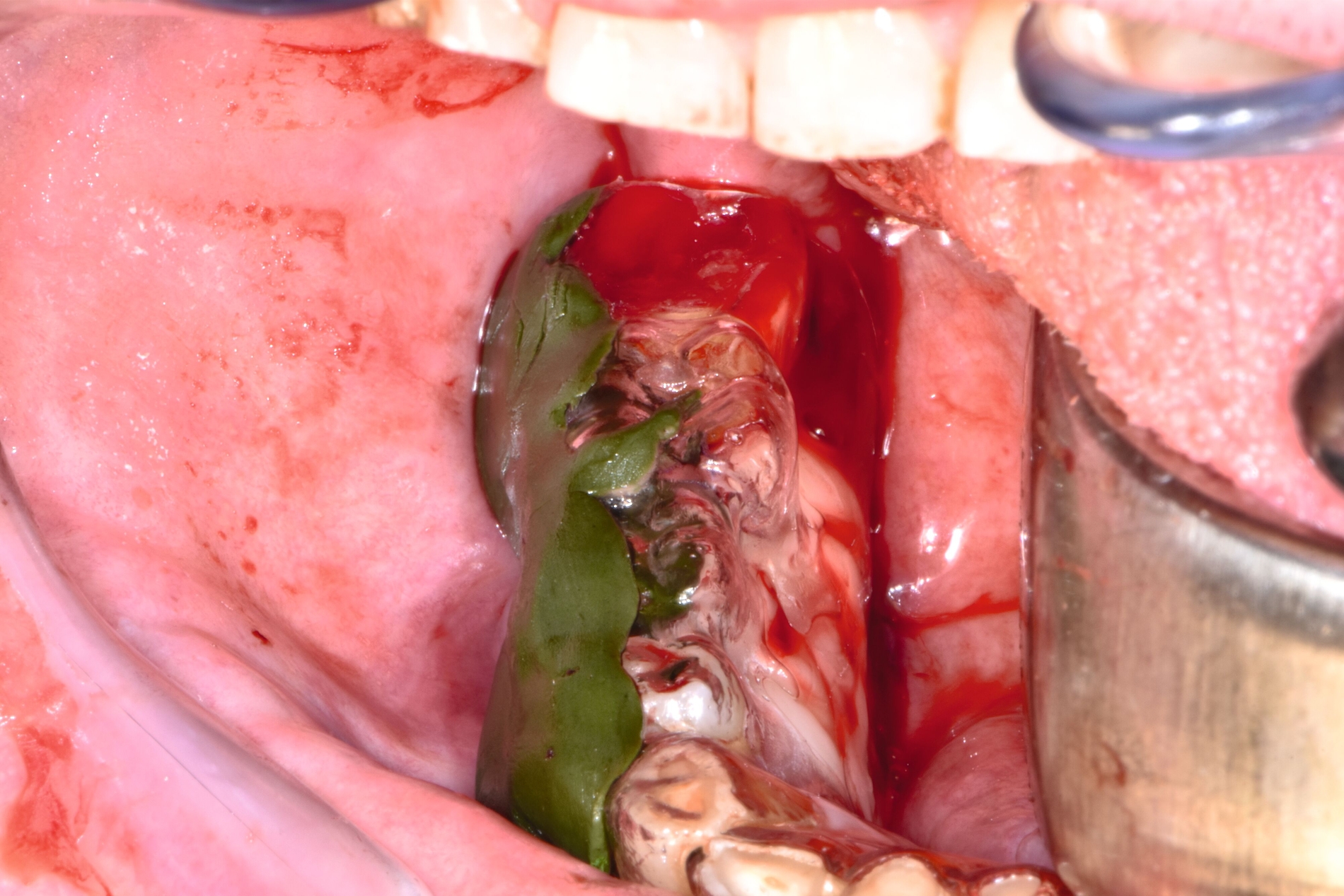
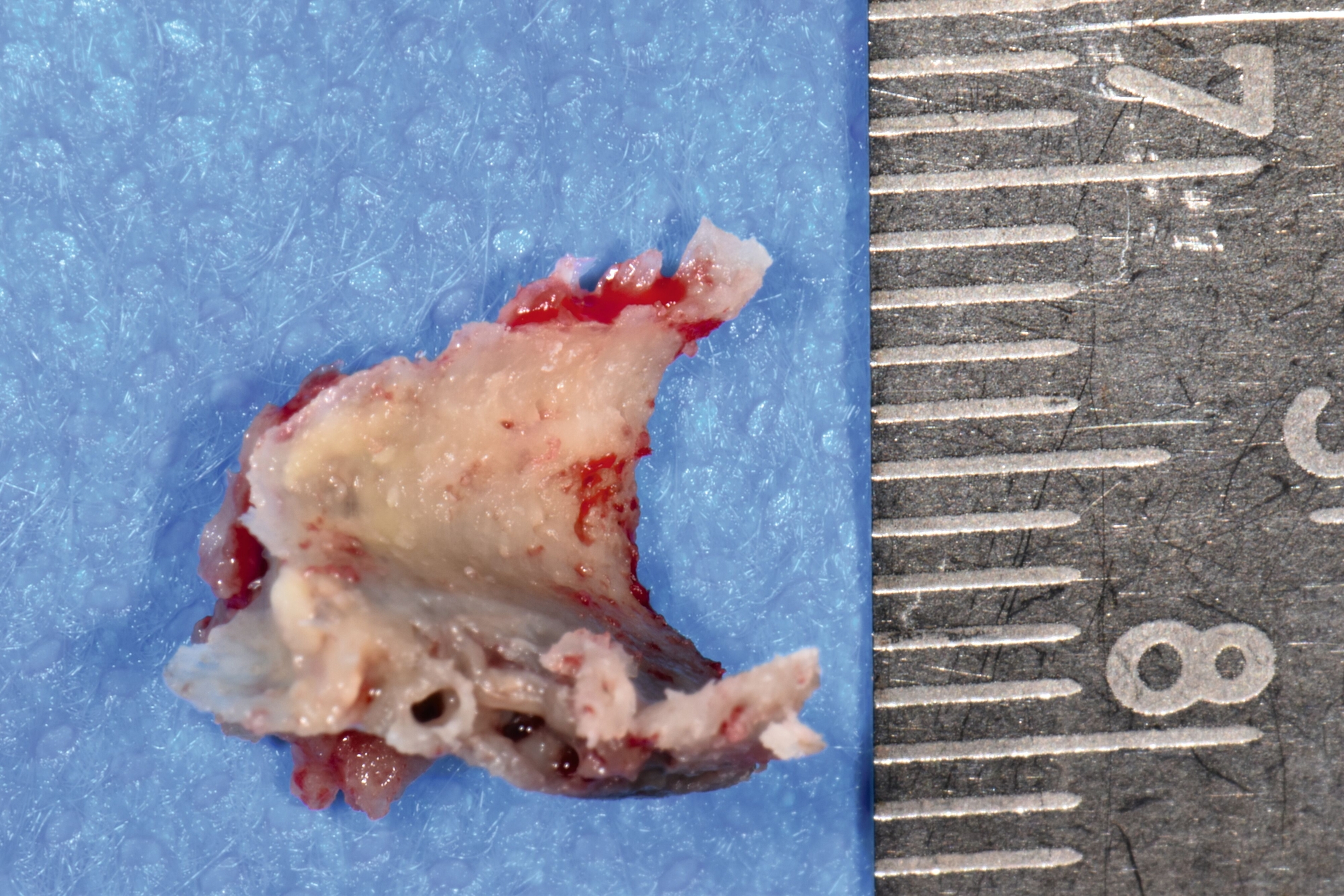
Therapeutisch erfolgte eine gezielte Sequestrotomie und nur zwei Zahnentfernungen. Auf eine plastische Deckung wurde bewusst verzichtet. Stattdessen wurde Platelet-Rich Fibrin (PRF) auf die Wundfläche appliziert und mit einer Verbandplatte geschützt. Unter vorübergehender enteraler Ernährung über eine Magensonde zeigte sich eine nahezu vollständige Schleimhautregeneration innerhalb weniger Wochen. Eine kleine Restläsion in Regio 44 lingual heilte unter lokaler Therapie mit Chlorhexidin und einer Occlusivpaste vollständig ab. Eine Kontrollszintigrafie nach sechs Monaten bestätigte die weitgehende Ausheilung.
Diskussion
Die Osteonekrose des Kiefers (ONJ) ist eine klinisch relevante Komplikation, die unterschiedliche Ursachen haben kann. Während Medikamenten- oder Strahlen-induzierte Formen häufig beschrieben sind, stellt die Herpes-Zoster-assoziierte Osteonekrose (HZ-ONJ) eine außergewöhnlich seltene Variante dar. Sie wurde erstmals von Rose im Jahr 1908 beschrieben, der über Knochenveränderungen im Zusammenhang mit Herpes Zoster berichtete [Singh, 2020]. In den folgenden Jahrzehnten erschienen mehrere Fallberichte, die das Auftreten von Kiefernekrosen und Zahnverlusten nach Herpes-Zoster-Infektionen im Versorgungsgebiet des Nervus trigeminus bestätigten. Wright et al. lieferten schließlich die erste histopathologisch belegte Beschreibung einer alveolären Osteonekrose infolge einer Zoster-Reaktivierung [1983].
Die Pathophysiologie der HZ-ONJ ist komplex und bislang nicht vollständig geklärt. Das Varicella-Zoster-Virus (VZV) persistiert nach einer Primärinfektion in den sensorischen Ganglien und kann bei eingeschränkter Immunkompetenz reaktiviert werden [Gershon, 2015]. Die klinische Manifestation im Bereich des Nervus trigeminus führt zu typischen Hautläsionen, in seltenen Fällen auch zu oralen und ossären Komplikationen. Die derzeitigen Hypothesen zur Pathogenese favorisieren eine durch das Virus induzierte Vaskulitis, die zu thrombotischen Verschlüssen kleiner arterieller Gefäße und zur lokalen Ischämie des alveolären Knochens führt [Wright, 1983; Park, 2024]. Histopathologische Untersuchungen zeigen eine fibrinoide Degeneration der Gefäßwände, Lumenverschlüsse und Nekrosen der Intima. Ergänzend wird auch eine neuronale Beteiligung angenommen: Das Virus breitet sich nach dieser Vorstellung entlang des N. alveolaris inferior aus und kann eine trophische Schädigung des Knochens hervorrufen.
Die Kombination aus vaskulärer Ischämie, neuraler Schädigung und bakterieller Superinfektion schafft eine pathologische Situation, die der Medikamenten- oder Strahlen-induzierten Osteonekrose ähnelt, die jedoch ohne die entsprechenden Risikofaktoren auftritt [Asha, 2014; Huang, 2024]. Neuere molekularbiologische Studien konnten den Virusnachweis direkt im nekrotischen Knochen erbringen. Huang et al. wiesen mithilfe von Next-Generation-Sequencing VZV-DNA in den betroffenen Arealen nach und bestätigten so die direkte virale Beteiligung an der Pathogenese [2024]. Diese Erkenntnis stützt die Hypothese einer primär vaskulopathischen Genese mit sekundärer Knochenischämie.
Parallel dazu beschrieb Park in einer systematischen Übersichtsarbeit mit mehr als 60 publizierten Fällen, dass über 80 Prozent der Patientinnen und Patienten systemische Risikofaktoren wie Diabetes, eine HIV-Infektion, eine Tumorerkrankung oder eine medikamentöse Immunsuppression aufwiesen [2024]. Besonders gefährdet sind ältere Patienten mit eingeschränkter Immunabwehr oder vaskulären Begleiterkrankungen. In Einzelfällen kann die Erkrankung aber auch bei immunkompetenten Personen auftreten [Faure, 2021; Chatterjee, 2023].
In den publizierten Fallserien war der Unterkiefer häufiger betroffen als der Oberkiefer (Verhältnis etwa 3,5 zu 1). Der Krankheitsbeginn liegt meist zwischen der zweiten und der vierten Woche nach den Hauteffloreszenzen, kann aber auch verzögert auftreten [Mintz, 1992; Badjate, 2009]. Typisch ist ein einseitiger Verlauf entlang der betroffenen Nervenäste, auch mit spontaner Zahnexfoliation, freiliegendem Knochen und (manchmal) persistierender Neuralgie. Differenzialdiagnostisch müssen die MRONJ, die Osteoradionekrose und die bakterielle Osteomyelitis ausgeschlossen werden. Wenn diese Ursachen fehlen und eine zeitlich assoziierte Herpes-Zoster-Infektion besteht, ist die Diagnose einer HZ-assoziierten Osteonekrose naheliegend [Aghaloo, 2017].
Der Therapieansatz richtet sich nach dem Krankheitsstadium. In der akuten Zosterphase steht die antivirale Therapie mit Aciclovir oder Valaciclovir im Vordergrund, um die Virusreplikation und die Dauer der Neuralgie zu reduzieren [Gan, 2013; Nagel, 2013]. Nach dem Sistieren der akuten Entzündung kann eine chirurgische Sanierung erfolgen. Frühere Berichte haben eine ausgedehnte Resektion empfohlen [Hall, 1974], doch neuere Fallserien zeigen, dass ein reduziert-invasives Vorgehen mit gezielter Sequestrotomie und sorgfältiger lokaler Wundpflege in den meisten Fällen ausreichend ist [Kaur, 2016; Park, 2024]. Nach dem Abklingen der aktiven Virusphase ist zu erwarten, dass die lokale Vaskulitis erloschen ist und sich die Mikrozirkulation im umliegenden Knochen normalisiert hat. Unter diesen Bedingungen kann die Knochenheilung erfolgreich verlaufen.
Im beschriebenen Fall wurde nach der Sequestrotomie, die eine ausgedehnte Knochenwundfläche hinterließ, ergänzend PRF appliziert, um die Weichgewebsheilung zu fördern und zugleich auf eine plastische Deckung verzichten zu können. Der Einsatz von PRF bot dabei eine biologische Unterstützung der sekundären Schleimhautheilung und ermöglichte eine nahezu komplikationslose Wundregeneration trotz der großflächigen Exposition. Klinische Studien belegen eine beschleunigte epitheliale Regeneration und eine geringere Inzidenz von Wunddehiszenzen nach PRF-Anwendung [Temmerman, 2016]. Ein solcher Heilungsverlauf wäre bei Medikamenten-assoziierten oder Strahlen-bedingten Osteonekrosen in der Regel nicht zu erwarten, da dort (unter anderem) eine persistierende Gefäßschädigung und eine chronische Ischämie bestehen. Im Gegensatz dazu ist die Durchblutung bei der Herpes-Zoster-assoziierten Osteonekrose nach Abklingen der akuten Vaskulitis meist wiederhergestellt, was eine weitgehend physiologische Regeneration des Gewebes ermöglicht.
Die Knochenszintigrafie zeigte in diesem Fall eine deutliche lokale Mehranreicherung, wie man sie in vergleichbarer Intensität auch bei Medikamenten-assoziierten oder Strahlenbedingten Osteonekrosen beobachten kann. Während bei diesen Entitäten aufgrund der chronischen Ischämie meist ausgedehnte, teils kontinuitätunterbrechende Resektionen erforderlich sind, unterscheidet sich die Pathophysiologie der Herpes-Zoster-assoziierten Osteonekrose grundlegend. Da hier eine vorübergehende, Virus-induzierte Vaskulitis vorliegt, sollte die szintigrafische Aktivität nicht überinterpretiert, sondern ein zurückhaltendes, reduziert-invasives chirurgisches Vorgehen gewählt werden. Der beschriebene Heilungsverlauf bestätigt die Effektivität des gewählten konservativen Vorgehens.
Die Prognose der HZ-ONJ ist in der Regel gut, wenn eine adäquate antivirale Therapie erfolgt und nekrotisches Gewebe entfernt wird. Langzeitverläufe zeigen stabile Verhältnisse ohne Rezidiv [Chen, 2019; Chatterjee, 2023]. Entscheidend ist eine frühzeitige und auch kontinuierliche zahnärztliche Begleitung bei Herpes-Zoster-Infektionen des Nervus trigeminus, da dentoalveoläre Komplikationen auch Wochen nach dem initialen Hautbefall auftreten können [Huang, 2024]. Eine enge interdisziplinäre Zusammenarbeit zwischen Dermatologie, Zahnmedizin und Mund-, Kiefer- und Gesichtschirurgie ist daher unabdingbar.
Zusammenfassung
Die Herpes-Zoster-assoziierte Osteonekrose wird heute dank moderner diagnostischer Verfahren und wachsender Fallzahlen zunehmend besser verstanden. Aktuelle Untersuchungen deuten darauf hin, dass diese Komplikation häufiger vorkommt als bisher angenommen, insbesondere bei älteren oder systemisch vorerkrankten Patienten.
Die Kombination aus antiviraler Frühtherapie und schonender chirurgischer Sanierung unter Verwendung von PRF stellt eine effektive und prognostisch günstige Behandlungsoption dar. Ebenso entscheidend ist eine frühzeitige interdisziplinäre Zusammenarbeit: Bei jeder Herpes-Zoster-Manifestation im Kiefer-Gesichtsbereich sollte frühzeitig eine zahnärztliche Mitbetreuung erfolgen, um dentoalveoläre Komplikationen rechtzeitig zu erkennen und gegebenenfalls therapeutisch einzugreifen.
Dieser Fall verdeutlicht, dass nach überstandener Zoster-Reaktivierung und Wiederherstellung der lokalen Mikrozirkulation eine weitgehend physiologische Knochen- und Schleimhautheilung möglich ist, sofern das operative Vorgehen an die spezifische Pathophysiologie angepasst wird.
Literaturliste
Aghaloo TL, Tetradis S (2017). Osteonecrosis of the jaw: Pathophysiology and management. Oral Maxillofac Surg Clin North Am 29: 491–501.
Asha ML et al. (2014). Herpes zoster leading to viral osteomyelitis or neuralgia inducing cavitational osteonecrosis? Int J Sci Study 2: 125–128.
Badjate SJ et al. (2009). Ramsay-Hunt syndrome complicating osteonecrosis of edentulous maxilla and mandible. J Maxillofac Oral Surg 8: 188–191.
Chatterjee A et al. (2023). Delayed presentation of mandibular osteonecrosis following herpes zoster infection. Ann Maxillofac Surg 13: 220–223.
Chen Y-W et al. (2019). Severe mandibular osteonecrosis after herpes zoster infection. J Prosthodont Implantol 8: 29–34.
Faure E et al. (2021). Herpes zoster mandibular osteonecrosis: case report and literature review. J Stomatol Oral Maxillofac Surg 122: 360–364.
Gan EY et al. (2013). Management of herpes zoster and post-herpetic neuralgia. Am J Clin Dermatol 14: 77–89.
Gershon AA et al. (2015). Varicella zoster virus infection. Nat Rev Dis Primers 1: 15016.
Hall HD et al. (1974). Necrosis of maxilla in patient with herpes zoster. Oral Surg Oral Med Oral Pathol 37: 658–662.
Huang K et al. (2024). Infection may play an important role in the pathogenesis of alveolar osteonecrosis following facial herpes zoster. BMC Oral Health 24: 409.
Kaur R et al. (2016). Spontaneous tooth exfoliation associated with trigeminal herpes zoster. Oral Maxillofac Surg 20: 133–137.
Mintz SM, Anavi Y (1992). Necrosis of maxilla following herpes zoster. Oral Surg Oral Med Oral Pathol 73: 646–650.
Nagel MA, Gilden D (2013). The protean neurologic manifestations of varicella-zoster virus infection. Cleve Clin J Med 80: 511–518.
Park KS (2024). Herpes zoster-associated osteonecrosis of the jaws: a comprehensive review of 63 cases. Medicina 60: 1189.
Schwartz O, Kvorning SA (1982). Tooth exfoliation, osteonecrosis of the jaw and neuralgia following herpes zoster of the trigeminal nerve. Int J Oral Surg 11: 364–371.
Singh G et al. (2020). Alveolar osteonecrosis and tooth exfoliation in herpes zoster: a rare pediatric case report and review of literature. Int J Clin Pediatr Dent 13(S-1): S106–S109.
Temmerman A et al. (2016). The use of leucocyte and platelet-rich fibrin in socket management and soft tissue healing: a randomized controlled trial. J Clin Periodontol 43(11): 995–1002.
Wright WE et al. (1983). Alveolar bone necrosis following herpes zoster infection. Oral Surg Oral Med Oral Pathol 55: 149–153.