Osteomyelitis der Kiefer
Entgegen seiner Etymologie, bei der die Osteomyelitis eine Entzündung ausschließlich des Knochenmarks beschreibt (Osteon = Knochen, Muelinos = Mark), versteht man in der medizinischen Literatur unter dem Begriff der Osteomyelitis eine Entzündung des gesamten Knochens, inklusive der Kortikalis und des Periosts. Von der Osteomyelitis der Kiefer müssen sowohl die Osteoradionekrosen und die Osteochemonekrosen abgegrenzt werden, auf die in dem vorliegenden Beitrag nicht weiter eingegangen werden soll (siehe Infokästen 1 und 2).
Da der Kieferknochen über die Zähne und das Parodont mit einer Vielzahl potenziell pathogener Keime in der Mundhöhle in direktem Kontakt steht, nimmt der Kiefer im Vergleich zu den langen Röhrenknochen eine einzigartige Rolle ein. Von daher lassen sich Ätiologie und Pathogenese von Entzündungen der langen Röhrenknochen nicht direkt auf die Kieferknochen übertragen.
Seit der Einführung der Antibiotikatherapie vor etwa 50 Jahren hat sich die Behandlung der Kieferosteomyelitis grundlegend verbessert. Andererseits wird durch einen frühzeitigen Antibiotikaeinsatz die akute Phase der Entzündung oft kaschiert, ohne aber eine vollständige Elimination der Erreger zu erreichen, was zu einer Zunahme von subakuten oder chronischen Verlaufsformen führt [Bünger, 1994].
Klassifikation
Für die Kieferosteomyelitiden wurde bereits eine große Vielzahl unterschiedlicher Klassifikationen beschrieben. Diese berücksichtigen zur Einteilung unterschiedliche Aspekte wie die Ätiologie, die Pathogenese, den klinischen Verlauf, pathologisch-anatomische und/oder röntgenologische Befunde [Schelhorn et al., 1989; Marx, 1991; Mercuri, 1991; Hudson, 1993 ]. Diese Vielfalt führt teilweise zu Verwirrungen und macht einen Vergleich verschiedener Studien zudem unmöglich.
Eine empfehlenswerte Einteilung der Osteomyelitis, die sowohl die klinische Symptomatik als auch den Verlauf der Erkrankung berücksichtigt, stellt die Zürich-Klassifikation dar [Baltensperger, 2008]. Hier werden drei Haupttypen unterschieden: die akute, die sekundär-chronische und die primär-chronische Osteomyelitis (Abbildung 1). Bei der sekundär-chronischen Osteomyelitis handelt es sich um die Chronifizierung einer akuten Osteomyelitis, die sich dadurch mit einem anderen klinischen Erscheinungsbild präsentiert. Der Übergang zwischen diesen beiden Formen ist fließend und klinisch oft nicht eindeutig abgrenzbar. Daher wird in der Zürich-Klassifikation eine Infektion von mehr als vier Wochen als sekundär-chronisch bezeichnet.
Wie bereits erwähnt, wird eine akute Osteomyelitis der Kiefer selten diagnostiziert. Der Begriff „subakute Osteomyelitis“ wird in der Literatur nicht eindeutig definiert und dementsprechend unterschiedlich verwendet. Von einigen Autoren wird der Terminus „subakute Osteomyelitis“ verwendet, um eine chronische Osteomyelitis mit subakuten Beschwerden zu beschreiben, andere hingegen verstehen darunter die Übergangsphase zwischen einer akuten zu einer chronischen Osteomyelitis [Schuknecht et al., 2003].
Marx und Mercuri waren die ersten, die den Zeitraum von vier Wochen definierten, nach dem man eine akute Osteomyelitis als sekundär-chronisch bezeichnete [Marx, 1991; Mercuri, 1991]. Als Beginn der Erkrankung wird dabei die bakterielle Invasion des Markraums und des kortikalen Knochens definiert. Diese Definition wurde von vielen Autoren so übernommen [Koorbusch et al., 1992; Schuknecht et al., 1997; Eyrich et al., 1999].
Der Begriff der chronischen Osteomyelitis wird in der Literatur teilweise uneinheitlich verwendet. Oft wird die chronische Osteomyelitis der Kiefer in zwei Subkategorien unterteilt: die eitrige und die nicht-eitrige Form [Hudson, 1993]. Die chronisch-eitrige Form kann synonym zu dem Begriff sekundär-chronische Osteomyelitis verwendet werden und ist bei Weitem die häufigste Form der Osteomyelitis.
Pathogenese
In der Mundhöhle ist eine Vielzahl potenziell pathogener Keime vorhanden, die prinzipiell zu einer Infektion des Kieferknochens führen können. Warum es trotzdem relativ selten zu einer Osteomyelitis kommt, liegt an dem Gleichgewicht zwischen der Virulenz und der Anzahl der pathogenen Keime auf der einen Seite und der lokalen Immunabwehr und Gewebedurchblutung auf der anderen Seite [Baltensperger, 2008]. Kommt es nun zu einer Verschiebung dieses Gleichgewichts auf die eine oder andere Seite, dann ist eine Infektion des Knochens möglich. Dementsprechend begünstigen systemische Erkrankungen, die das Immunsystem schwächen, wie ein Diabetes mellitus, Autoimmunerkrankungen, Anämien oder Leukämien das Auftreten einer Osteomyelitis. Gleichzeitig ist eine Beeinträchtigung der lokalen Gewebedurchblutung ein kritischer Faktor für die Entstehung beziehungsweise Ausbreitung einer Osteomyelitis, da Immunzellen und Sauerstoff nicht in das Zielgebiet gelangen können. Somit sind Mikroorganismen ins-besondere Anaerobier ungehindert in der Lage, sich zu vermehren und auszubreiten.
Lokale und systemische Faktoren, die zu einer Verminderung der Gewebedurchblutung führen können, sind unter anderem Rauchen, Diabetes mellitus sowie vorbestehende Knochenerkrankungen (wie Fibröse Dysplasie, Morbus Paget, Osteopetrosis).
In den meisten Fällen betrifft eine Osteomyelitis den Unterkiefer. Dies ist der Tatsache geschuldet, dass der Oberkiefer im Vergleich zum Unterkiefer über eine bessere Gefäßversorgung verfügt und neben einer dünnen Kortikalis nur wenig Spongiosa besitzt. Innerhalb des Unterkiefers ist hauptsächlich der corpus mandibulae betroffen, gefolgt von der Symphyse, dem Kieferwinkel, dem aufsteigenden Ast und dem Kondylus [Calhoun et al., 1988].
Im Gegensatz zur Osteomyelitis der langen Röhrenknochen, bei der eine hämatogene Streuung von Mikroorganismen die häufigste Ursache darstellt, liegt bei den Osteomyelitiden des Kiefers in der Regel die Ursache in einem lokalen infektiösen Fokus, wobei hier odontogene Infektionen (pulpale oder peridontale Infektionen, infiziertes perikoronares Gewebe bei retinierten Zähnen) die größte Rolle spielen. Aber auch nicht oder inadäquatversorgte Frakturen im Kieferbereich oder chirurgische Eingriffe können Auslöser für die Entstehung einer Osteomyelitis sein.
Eine Ausnahme bildet die Säuglingsosteomyelitis. Diese tritt oft in den ersten Lebenswochen auf und betrifft in der Regel nur den Oberkiefer. Hierbei wird von den meisten Autoren ein hämatogener Infektionsweg beschrieben, wobei auch ein perinatales Trauma der lokalen Schleimhaut ursächlich gemacht wird [Nade, 1983]. Als Erreger wird hauptsächlich Staphylococcus aureus nachgewiesen [Loh et al., 1993].
Nachdem es über einen entzündlichen Fokus zu einer Invasion des Knochens mit Mikroorganismen gekommen ist, führt die lokale Immunantwort zu einer Hyperämie, zu einer erhöhten Gefäßpermeabilität und zu einer lokalen Anreicherung von Granulozyten, die proteolytische Enzyme sezernieren.
Es kommt zur Bildung von Pus, bestehend aus nekrotischem Gewebe, zerstörten Bakterien und weißen Blutkörperchen. Über diese Pus- und Ödembildung erhöht sich der intramedulläre Druck, der die lokale Blutzirkulation kompromittiert. Pus gelangt über die Haverschen Kanäle bis unter das Periost und hebt das Periost von der Kortikalis ab, was die Blutzufuhr über das Periost weiter beeinträchtigt. Kommt es zu einer Perforation des Periosts, können sich submuköse oder kutane Abszesse ausbilden und Fisteln entstehen.
Zusätzlich kann es durch den erhöhten Druck im Knochenmark des Unterkiefers zu einer direkten Kompression des Nervus alveolaris inferior mit entsprechenden Sensibilitäts-störungen kommen (Vincent-Syndrom).
Nach dem akuten Entzündungsprozess mit Beeinträchtigung der lokalen Blutzirkulation kommt es zur Nekrose des Knochens mit anschließender Sequestrierung. Dabei führt die Aktivität der Osteoklasten zu einer Separierung des toten Knochens vom vitalen Knochengewebe (Abbildung 2). Hierbei kann es zusätzlich zu einer periostalen Reaktion mit Bildung von neuem Knochen (Neo- Osteogenese) kommen. Im Rahmen der Chronifizierung einer Osteomyelitis kann sich hierbei ein neues Gleichgewicht einstellen, bei der die lokalen Abwehrmechanismen die Infektion zwar eindämmen, aber nicht komplett beseitigen können. Hier kommt es zu einer starken, diffusen Sklerosierung des Knochens mit oder ohne periostale Reaktion.
Klinik
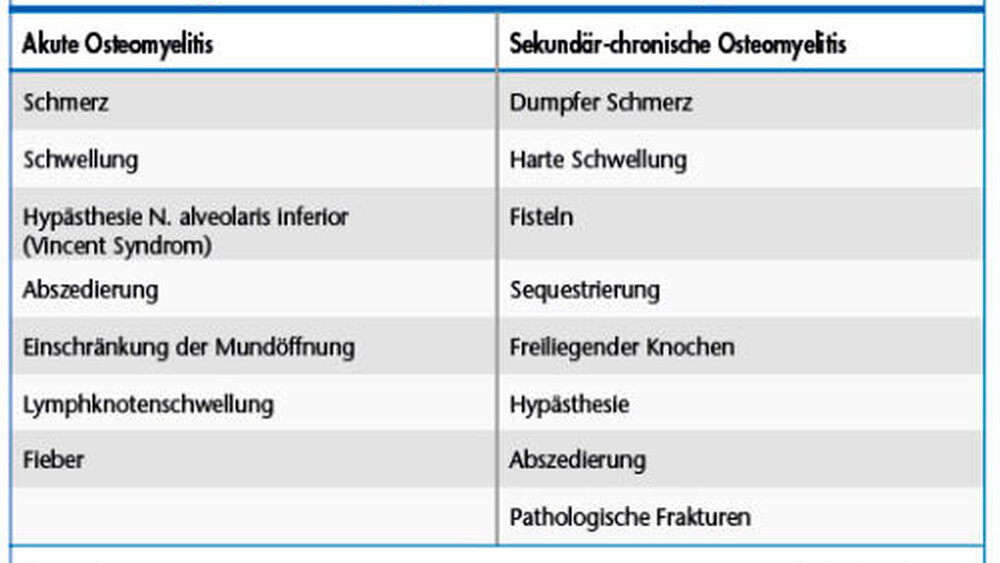
Die akute und die sekundär-chronische Osteomyelitis treten in allen Altersgruppen auf, dies mit einer relativen Häufung im dritten bis sechsten Lebensjahrzent. Männer sind dabei etwa doppelt so häufig betroffen wie Frauen [Baltensperger, 2008]. Das klinische Bild einer akuten Osteomyelitis ist von den klassischen Kardinalsymptomen einer Entzündung geprägt (Tabelle 1).
Starke Schmerzen im Kieferknochen stehen im Vordergrund, in der Regel in Kombination mit einer lokalen Schwellung oder Abszedierung, was zu einer deutlich eingeschränkten Mundöffnung führen kann. Der Patient verspürt ein starkes Krankheitsgefühl mit hohen Temperaturen von 39 bis 40°C. In der Laboranalyse können erhöhte CRP-Werte (C-reaktives Protein) und eine Leukozytose nachgewiesen werden [Baltensperger, 2008]. Insgesamt hat sich durch die Verbesserung der (zahn-)medizinischen Versorgung mit dem frühzeitigen Einsatz von Antibiotika bei dentogenen Infekten sowohl die Inzidenz als auch die Intensität des klinischen Erscheinungsbildes einer akuten Osteomyelitis deutlich reduziert, so dass es sich heutzutage meistens um sekundär-chronische Verlaufsformen handelt.
Im Fall einer sekundär-chronischen Osteomyelitis kann die klinische Symptomatik in ihrer Ausprägung und Intensität deutlich variieren (Tabelle 1). Im Vergleich zur akuten Osteomyelitis treten die Kardinalsymptome Schmerz und Schwellung weniger ausgeprägt auf. Die Schmerzqualität hat im chronischen Stadium einen eher dumpfen Charakter. Durch eine ausgeprägte periostale Reaktion kann eine harte, oft auch indolente Schwellung palpabel sein. Als klassische Zeichen einer chronischen Osteomyelitis gelten Sequestrierungen und die Ausbildung von extraoralen Fisteln, was eine eindeutige Unterscheidung zur primär-chronischen Osteomyelitis erlaubt (Abbildung 2).
Primär-chronische Osteomyelitis
Gemäß der Zürich-Klassifikation wird bei der primär chronischen Osteomyelitis zwischen drei Subtypen unterschieden einer juvenilen Form („early onset“), einer adulten Form („adult onset“) und den syndrom-assoziierten Formen (Abbildung 1).
Die primär-chronische Osteomyelitis ist eine seltene Erkrankung unbekannter Ätiologie. Charakteristisch ist das Fehlen von Pus, Fistel- oder Sequesterbildung, was die Abgrenzung von der akuten oder von der sekundär-chronischen Osteomyelitis ermöglicht [Schelhorn et al., 1989; Eyrich et al., 1999]. Gleichzeitig ist der Erkrankung kein akutes Stadium oder auslösendes Ereignis vorausgegangen. Oft wird der Begriff der „diffus-sklerosierenden Osteomyelitis“ synonym gebraucht, wobei sich dieser Terminus streng genommen nur auf das röntgenologische Erscheinungsbild bezieht, das jedoch durch unterschiedliche Entitäten verursacht werden kann [Eyrich et al., 2003].
Klinisch imponiert ein oft zyklischer Ver- lauf mit aktiven Phasen unterschiedlicher Intensität, die in der Regel von Schmerz, einer Schwellung und einer eingeschränkten Mundöffnung gekennzeichnet sind (Abbildung 3). Diese aktiven Phasen können wenige Tage bis mehrere Wochen dauern und stehen im Wechsel mit weitestgehend symptomfreien Intervallen.
Die Entstehung der primär-chronischen Osteomyelitis wird oft auf eine geringgradige Infektion zurückgeführt, obwohl sich in der Mehrzahl der intra- und extraoralen Probeentnahmen bei der mikrobiologischen Differenzierung entweder keine Bakterien oder nur die üblichen Kontaminationen nachweisen lassen [Van Merkesteyn et al., 1988].
Zusätzlich erzielt eine Vielzahl unterschied-licher Antibiotika, auch wenn über einen langen Zeitraum eingesetzt, in der Regel keine vollständige Ausheilung. Daher halten einige Autoren unter anderem eine Kieferfehlstellung oder Parafunktionen für ursächlich [van Merkesteyn et al., 1990; Groot et al., 1992]. Zum Ausschluss eines multifokalen Geschehens wird eine Skelettszintigrafie empfohlen (Abbildung 3).
Die juvenile Form („early onset“) der primär-chronischen Osteomyelitis wird von einigen Autoren als eigene Entität angesehen, und der Begriff der „juvenilen chronischen Osteomyelitis“ verwendet. Diese äußerst seltene Erkrankung tritt vor allem in der Pubertät auf und ist durch eine voluminöse Auftreibung des Unterkiefers, eine periostale Knochenanlagerung (periostitis ossificans) und eine gemischt sklerosierend-lytische Erscheinung der Spongiosa gekennzeichnet (Abbildung 4). Die klinische Symptomatik ist bei dieser Form der Osteomyelitis meist gering ausgeprägt und äußert sich in einer Schwellung der betroffenen Kieferseite. Oft wird noch der Begriff der „Garré Osteomye-litis“ synonym zur juvenilen chronischen Osteomyelitis gebraucht. Jedoch wurde von Garré ursprünglich lediglich eine spezielle Komplikation der akuten infektiösen Osteomyelitis beschrieben. Von daher sollte der Begriff „Garré Osteomyelitis“ in der Klassifikation der Osteomyelitiden nicht weiter verwendet werden [Wood et al., 1988].
In einer Vielzahl von Untersuchungen wurde ein Zusammenhang zwischen einer primär-chronischen Osteomyelitis der Kiefer und dem SAPHO-Syndrom beschrieben [Eyrich et al., 1999; Roldán et al., 2001; Fleuridas et al., 2002]. Das Akronym „SAPHO“ bezeichnet das Vorhandensein von Synovitis (Arthritis), Akne, Pustulosis (Pustolosis palmoplantaris psoriatica), Hyperostosis sowie Osteitis (sterile Osteomyelitis) und wurde 1986 durch Chamot erstmalig beschrieben [Chamot et al., 1986]. Diese chronische Erkrankung betrifft somit Gelenke, Haut und Knochen und wird als rheumatische Erkrankung behandelt.
Eine weitere systemische Erkrankung, bei der über einen Zusammenhang mit der primär-chronischen Osteomyelitis berichtet wurde, ist die chronisch rekurrierende multifokale Osteomyelitis (CRMO) [; ]. Die CRMO ist eine sterile chronische Osteomyelitis des Skelettsystems, die hauptsächlich die Metaphysen der langen Röhrenknochen betrifft und durch einen langjährigen periodischen Verlauf von Exazerbationen und Remissionen geprägt ist. In etwa fünf Prozent der Fälle wird im Rahmen einer CRMO eine Beteiligung der Mandibula beschrieben, die in diesem Fall der klinischen Symptomatik einer primär-chronischen Osteomyelitis entspricht [Schilling, 1998; Zebedin et al., 1998]. Betroffen sind hauptsächlich Kinder und Jugendliche, weshalb die CRMO auch von einigen Autoren als juvenile Variante des SAPHO-Syndroms bezeichnet wird[Vignon-Pennamen et al., 1991]. Die Behandlung erfolgt mit antiinflammatorischen (nicht-steroidalen Antiphlogistika und Kortikoiden) sowie immunmodulatorischen (TNF-alpha-Antikörper) Therapien. Bei Therapieversagen können auch Bisphosphonate eingesetzt werden.
Diagnostik
Neben der klinischen Untersuchung kommen zur Diagnostik der Kieferosteomyelitis unterschiedliche bildgebende Verfahren zum Einsatz.
Konventionelle Röntgenaufnahmen (Panoramaschichtaufnahme, Computertomografie (CT) oder digitale Volumentomografie (DVT)) dienen insbesondere dazu, das Ausmaß der Osteolyse oder auch der reaktiven Sklerosierung darzustellen. Hier muss jedoch beachtet werden, dass erst nach einer circa 30-prozentigen Reduktion des mineralisierten Knochens ein osteolytischer Prozess im Röntgenbild sichtbar wird. Gerade zur Planung eines chirurgischen Vorgehens ist jedoch heute ein schichtbildgebendes Verfahren (DVT, CT) unverzichtbar.
In frühem Stadium kann eine Magnetresonanztomografie (MRT) zur Bestätigung der Verdachtsdiagnose einer Osteomyelitis hilfreich sein. Hier zeigt sich bedingt durch das Markraumödem eine Signalintensität im T2-gewichteten Bild sowie eine Kontrastmittelanreicherung im Gewebe im T1- gewichteten Bild als Zeichen der erhöhten Gefäßpermeabilität [Schuknecht et al., 2003] (Abbildung 5).
Die Knochenszintigrafie als nuklearmedizinisches Untersuchungsverfahren zeichnet sich insbesondere durch eine sehr hohe Sensitivität aus, bleibt aber in Anbetracht der hohen Aussagekraft von CT und MRT nur für komplexe und unklare Fälle vor allem bei multifokaler Manifestation reserviert.
Therapie
• Bei der akuten Osteomyelitis steht neben der Entfernung des ursächlichen Fokus und im Fall einer Abszedierung der suffizienten Drainage vor allem die antibiotische Therapie im Vordergrund, da hier ein chirurgisches Vorgehen am Knochen noch nicht indiziert ist [Kim et al., 2001]. Bei der antiinfektiven Therapie sollte mit einem Breitspektrum- antibiotikum begonnen werden. Penicilline gelten wegen ihrer großen therapeutischen Breite als Mittel der ersten Wahl [Bode et al., 2010]. In der Regel handelt es sich bei der Osteomyelitis um eine anaerobe Misch- infektion von Keimen der oralen Flora, wobei neben den „klassischen“ Osteomyelitis-Keimen wie Staphylococcus aureus, Staphylococcus epidermidis und Actinomyces in einer aktuellen Studie der Nachweis von Streptococcus viridans führend war [Pigrau et al., 2009]. Häufig zeigen sich, wahrscheinlich als Folge einer antibiotischen Vorbehandlung, resistente Bakterien [Ang et al., 2008]. Hier wird primär Amoxicillin/ Clavulansäure oder Piperacillin/Tazobactam eingesetzt, als Mittel der zweiten Wahl Clindamycin, wobei interessanterweise eine Resistenz gegenüber Clindamycin nicht selten zu sein scheint [Pigrau et al., 2009]. Wegen des langwierigen Verlaufs ist, zumindest initial, meist eine parenterale Antibiotikatherapie indiziert, um sobald wie möglich auf ein kulturspezifisches Präparat nach mikrobiologischem Befund umzustellen. Insgesamt sollte die Antibiotikatherapie über einen längeren Zeitraum ( ein Monat) in therapeutischer Dosierung verabreicht werden.
• Das Prinzip der Therapie bei einer chronischen Osteomyelitis ist die Entfernung des infizierten und nekrotischen Knochens in Kombination mit einer antibiotischen Therapie.
Durch die Dekortikation soll der schlecht vaskularisierte und infizierte Knochen abgetragen werden, um über eine breitflächige Entfernung der Kompakta den Weichgeweben die Möglichkeit zu geben, sich an den eröffneten Markraum anzulagern. Dadurch wird zum einen der erhöhte intramedulläre Druck beseitigt und zum anderen eine erneute Gefäßeinsprossung in den Knochen erreicht. Ist der gesamte Querschnitt des Kieferknochens befallen oder liegt eine pathologische Fraktur vor, dann ist die Resektion des betroffenen Kieferabschnitts mit eventueller einzeitiger mikrochirurgischer Rekonstruktion indiziert [Kesting et al., 2008] (Abbildung 6).
• Der Stellenwert der hyperbaren Sauerstofftherapie, bei der eine Verbesserung der Gewebeoxidierung sowie ein toxischer Effekt auf Anaerobier erreicht werden sollen, wird für die Behandlung der Osteomyelitis weiterhin kontrovers diskutiert [Van Merkes-teyn et al., 1984; Jamil et al., 2000]..
• Bei chronischen Verlaufsformen sollte generell eine adäquate Schmerztherapie zur Vermeidung einer Chronifizierung der Schmerzen eingeleitet werden, weshalb unter Umständen frühzeitig ein Schmerztherapeut einbezogen werden sollte.
Zusammenfassung
Die Osteomyelitis ist trotz der hohen Verfügbarkeit von Antibiotika und einer verbesserten dentalen und medizinischen Versorgung eine relativ häufige Erkrankung im Kieferbereich. Eine Vielzahl teilweise verwirrender Klassifikationen ist in Gebrauch, die auf dem klinischen Verlauf, röntgenologischen Charakteristika oder pathogenetischen Gesichtspunkten beruhen. Aktuell bietet die Zürich-Klassifikation eine empfehlenswerte Einteilung, bei der drei Verlaufsformen unterschieden werden: Die akute Osteomyelitis, bei der es sich um eine bakterielle Infektion des Kieferknochens handelt und die bei einem Verlauf von länger als vier Wochen in die sekundär-chronische Osteomyelitis übergeht. Andererseits stellt die primär-chronische Osteomyelitis eine seltene, nicht-eitrige chronische Entzündung bislang unbekannter Ursache dar. Verlaufsformen mit einer Limitation auf den Unterkiefer wie zum Beispiel das SAPHO-Syndrom oder die chronisch-rekurrierende multifokale Osteomyelitis (CRMO) können ferner mit syste-mischen Erkrankungen assoziiert sein.
Fazit für die Praxis
Eine sinnvolle und empfehlenswerte Klassifikation unterscheidet die Osteomyelitis der Kiefer in drei Verlaufsformen, die akute, die sekundär-chronische und die primär-chronische Osteomyelitis. Bei der akuten und der sekundär-chronischen Osteomyelitis handelt es sich um eine bakterielle Infektion, die hauptsächlich von einem dentogenen Fokus ausgeht. Durch Fortschritte in der zahnmedizinischen Versorgung und den frühzeitigen Einsatz von Antibiotika wurde das Auftreten der akuten Osteomyelitis stark reduziert, so dass es sich in den meisten Fällen um die sekundär-chronische Verlaufsform handelt. Hier stehen therapeutisch die Fokussanierung, die Abtragung des infizierten, nekrotischen Knochens und die antibiotische Therapie im Vordergrund.
Zur Diagnostik sollten in der Regel schichtbildgebende Verfahren (CT, DVT, MRT) zum Einsatz kommen, die Szintigrafie bleibt Ausnahmefällen vorbehalten.
Für antiinfektive Therapie kommt in der Regel ein Breitspektrumantibiotika zum Einsatz, wobei initial oft auch eine parenterale Gabe sinnvoll ist. Der zunächst kalkulierten Therapie sollte nach Erregernachweis eine gezielte antibiotische Therapie folgen. Der Nutzen einer hyperbaren Sauerstoff- therapie bleibt weiterhin Gegenstand von Diskussionen.
PD Dr. Dr. Christian Freudlsperger
Prof. Dr. Dr. Jürgen Hoffmann
UNI-Klinikum Heidelberg, Klinik für ZMK-Heilkunde, Klinik und Poliklinik für MKG-Chirurgie
Im Neuenheimer Feld 400
69120 Heidelberg
chr.freudlsperger@med.uni-heidelberg.de
Literaturverzeichnis
Ang, J. Y. and B. I. Asmar (2008). „Multidrug-resistant viridans streptococcus (MDRVS) osteomyelitis of the mandible successfully treated with moxifloxacin.“ South Med J 101(5): 539–540.
Baltensperger, M. M. (2008). Osteomyelitis of the jaws. New York, Springer.
Bode, L. G., J. A. Kluytmans, H. F. Wertheim, D. Bogaers, C. M. Vandenbroucke-Grauls, R. Roosendaal, A. Troelstra, A. T. Box, A. Voss, I. van der Tweel, A. van Belkum, H. A. Verbrugh and M. C. Vos (2010). „Preventing surgical-site infections in nasal carriers of Staphylococcus aureus.“ N Engl J Med 362(1): 9–17.
Bünger, B. (1984). „[Primary chronic osteomyelitis in the jaw].“ ZWR 93(9): 704–707, 711–702.
Calhoun, K. H., R. D. Shapiro, C. M. Stiernberg, J. H. Calhoun and J. T. Mader (1988). „Osteomyelitis of the mandible.“ Arch Otolaryngol Head Neck Surg 114(10): 1157–1162.
Chamot, A. M., B. Vion and J. C. Gerster (1986). „Acute pseudoseptic arthritis and palmoplantar pustulosis.“ Clin Rheumatol 5(1): 118–123.
Eyrich, G. K., M. M. Baltensperger, E. Bruder and K. W. Graetz (2003). „Primary chronic osteomyelitis in childhood and adolescence: a retrospective analysis of 11 cases and review of the literature.“ J Oral Maxillofac Surg 61(5): 561–573.
Eyrich, G. K., C. Harder, H. F. Sailer, T. Langenegger, E. Bruder and B. A. Michel (1999). „Primary chronic osteomyelitis associated with synovitis, acne, pustulosis, hyperostosis and osteitis (SAPHO syndrome).“ J Oral Pathol Med 28(10): 456–464.
Fleuridas, G., N. Teysseres, J. P. Ragot, L. Chikhani and E. Favre-Dauvergne (2002). „[Diffuse sclerosing osteomyelitis of the mandible and SAPHO syndrome].“ Rev Stomatol Chir Maxillofac 103(2): 96–104.
Groot, R. H., B. W. Ongerboer de Visser, J. P. van Merkesteyn, J. D. Speelman and J. Bras (1992). „Changes in masseter inhibitory reflex responses in patients with diffuse sclerosing osteomyelitis of the mandible.“ Oral Surg Oral Med Oral Pathol 74(6): 727–732.
Hudson, J. W. (1993). „Osteomyelitis of the jaws: a 50-year perspective.“ J Oral Maxillofac Surg 51(12): 1294–1301.
Jamil, M. U., A. Eckardt and W. Franko (2000). „[Hyperbaric oxygen therapy. Clinical use in treatment of osteomyelitis, osteoradionecrosis and reconstructive surgery of the irradiated mandible].“ Mund Kiefer Gesichtschir 4(5): 320–323.
Kesting, M. R., P. Thurmüller, M. Ebsen and K. D. Wolff (2008). „Severe osteomyelitis following immediate placement of a dental implant.“ Int J Oral Maxillofac Implants 23(1): 137–142.
Kim, S. G. and H. S. Jang (2001). „Treatment of chronic osteomyelitis in Korea.“ Oral Surg Oral Med Oral Pathol Oral Radiol Endod 92(4): 394–398.
Koorbusch, G. F., P. Fotos and K. T. Goll (1992). „Retrospective assessment of osteomyelitis. Etiology, demographics, risk factors, and management in 35 cases.“ Oral Surg Oral Med Oral Pathol 74(2): 149–154.
Loh, F. C. and S. Y. Ling (1993). „Acute osteomyelitis of the maxilla in the newborn.“ J Laryngol Otol 107(7): 627–628.
Marx, R. E. (1991). „Chronic osteomyelitis of the jaws.“ Oral Maxillofac Surg Clin North Am 3(2): 367–381.
Mercuri, L. G. (1991). „Acute osteomyelitis of the jaws.“ Oral Maxillofac Surg Clin North Am 3(2): 355–365.
Nade, S. (1983). „Acute haematogenous osteomyelitis in infancy and childhood.“ J Bone Joint Surg Br 65(2): 109–119.
Pigrau, C., B. Almirante, D. Rodriguez, N. Larrosa, S. Bescos, G. Raspall and A. Pahissa (2009). „Osteomyelitis of the jaw: resistance to clindamycin in patients with prior antibiotics exposure.“ Eur J Clin Microbiol Infect Dis 28(4): 317–323.
Roldán, J. C., H. Terheyden, A. Dunsche, W. U. Kampen and J. O. Schroeder (2001). „Acne with chronic recurrent multifocal osteomyelitis involving the mandible as part of the SAPHO syndrome: case report.“ Br J Oral Maxillofac Surg 39(2): 141–144.
Schelhorn, P. and W. Zenk (1989). „[Clinics and therapy of the osteomyelitis of the lower jaw].“ Stomatol DDR 39(10): 672–676.
Schilling, F. (1998). „[Chronic recurrent multifocal osteomyelitis (CRMO)].“ Rofo 168(2): 115–127.
Schuknecht, B. and A. Valavanis (2003). „Osteomyelitis of the mandible.“ Neuroimaging Clin N Am 13(3): 605–618.
Schuknecht, B. F., F. R. Carls, A. Valavanis and H. F. Sailer (1997). „Mandibular osteomyelitis: evaluation and staging in 18 patients, using magnetic resonance imaging, computed tomography and conventional radiographs.“ J Craniomaxillofac Surg 25(1): 24–33.
Suei, Y., K. Tanimoto, A. Taguchi, T. Yamada, K. Yoshiga, T. Ishikawa and T. Wada (1995). „Possible identity of diffuse sclerosing osteomyelitis and chronic recurrent multifocal osteomyelitis. One entity or two.“ Oral Surg Oral Med Oral Pathol Oral Radiol Endod 80(4): 401–408.
Van Merkesteyn, J. P., D. J. Bakker, I. Van der Waal, G. J. Kusen, P. Egyedi, H. P. Van den Akker, K. De Man, A. K. Panders and K. E. Lekkas (1984). „Hyperbaric oxygen treatment of chronic osteomyelitis of the jaws.“ Int J Oral Surg 13(5): 386–395.
Van Merkesteyn, J. P., R. H. Groot, J. Bras and D. J. Bakker (1988). „Diffuse sclerosing osteomyelitis of the mandible: clinical radiographic and histologic findings in twenty-seven patients.“ J Oral Maxillofac Surg 46(10): 825–829.
van Merkesteyn, J. P., R. H. Groot, J. Bras, R. S. McCarroll and D. J. Bakker (1990). „Diffuse sclerosing osteomyelitis of the mandible: a new concept of its etiology.“ Oral Surg Oral Med Oral Pathol 70(4): 414–419.
Vignon-Pennamen, M. D. and D. Wallach (1991). „Cutaneous manifestations of neutrophilic disease. A study of seven cases.“ Dermatologica 183(4): 255–264.
Wood, R. E., C. J. Nortjé, F. Grotepass, S. Schmidt and A. M. Harris (1988). „Periostitis ossificans versus Garrè’s osteomyelitis. Part I. What did Garrè really say?“ Oral Surg Oral Med Oral Pathol 65(6): 773–777.
Zebedin, D., R. Fotter, P. Reittner, K. W. Preidler, C. Mache and D. H. Szolar (1998). „[Chronic recurrent multifocal osteomyelitis of the lower jaw].“ Rofo 169(5): 551–554.