Die Koronektomie – Renaissance eines alten Verfahrens?
Die operative Entfernung von Weisheitszähnen ist eine der häufigsten ambulant durchgeführten Operationen und wird in der Literatur immer wieder kontrovers diskutiert [Devine et al., 2017; AAOMS, 2013; Dodson und Susarla, 2014]. Insbesondere wenn ein erhöhtes Risiko für eine Schädigung des N. alveolaris inferior besteht, ist eine Abwägung der verschiedenen Operationstechniken von hoher Relevanz. Um die differenzialtherapeutische Entscheidungsfindung zu unterstützen, sind in der aktuellen DGZMK-Leitlinie Indikationen für die Technik der Koronektomie benannt [DGZMK, 2019].
Bei der Koronektomie wird die Zahnkrone selektiv mit dem gesamten Schmelzanteil entfernt und die Zahnwurzeln werden in situ belassen, ohne direkt oder indirekt den Nerv zu schädigen. Die Methode geriet in Deutschland etwas in Vergessenheit. Durch die aktualisierte Leitlinie und verbesserte radiologische Bildgebung, insbesondere durch die DVT, findet die Koronektomie nun wieder mehr Beachtung und stellt eine geeignete Therapieoption zum Schutz des N. alveolaris inferior bei enger Lagebeziehung zu retinierten oder impaktierten Zähnen dar [Brauer et al., 2015].
Kasuistik 1
Im Februar 2021 stellte sich eine 55-jährige Patientin nach Überweisung durch einen Oralchirurgen erstmalig in der Klinik und Poliklinik für Mund-, Kiefer- und Gesichtschirurgie der Universitätsmedizin Mainz vor. Die allgemeine Anamnese ergab Schmerzen und gelegentliche Hypästhesien beidseits im Unterkiefer, die seit etwa einem Jahr vorwiegend nach Kaubelastungen auftraten und mittels Physiotherapie behandelt wurden. Der Zahn 18 war bereits komplikationslos entfernt worden. Vier Wochen vor der Untersuchung in der Universitätsmedizin Mainz war es bei der Patientin vor allem im Bereich des retinierten Zahnes 38 zu einer akuten Schmerzexazerbation im Unterkiefer gekommen. Nach weiteren zwei Wochen war zudem erstmalig Pus in Regio 38 ausgetreten, woraufhin die Patientin von unserem Kollegen mit der Verdachtsdiagnose Dentitio difficilis Regio 38 zu uns überwiesen wurde.
Die Anamnese bei der Nichtraucherin ergab mit Ausnahme von Depressionen, die mittels Escitalopram behandelt wurden, keine weiteren Vor-/Grunderkrankungen oder Allergien. In der klinischen Untersuchung konnten eine leichte Schwellung und Druckdolenzen in Regio 38 und 48 festgestellt werden. Ein aktiver Pus-Austritt war jedoch nicht mehr zu beobachten. Der Zahn 26 reagierte etwas sensibler auf Kälte, ansonsten erwies sich der Zahnstatus unauffällig.
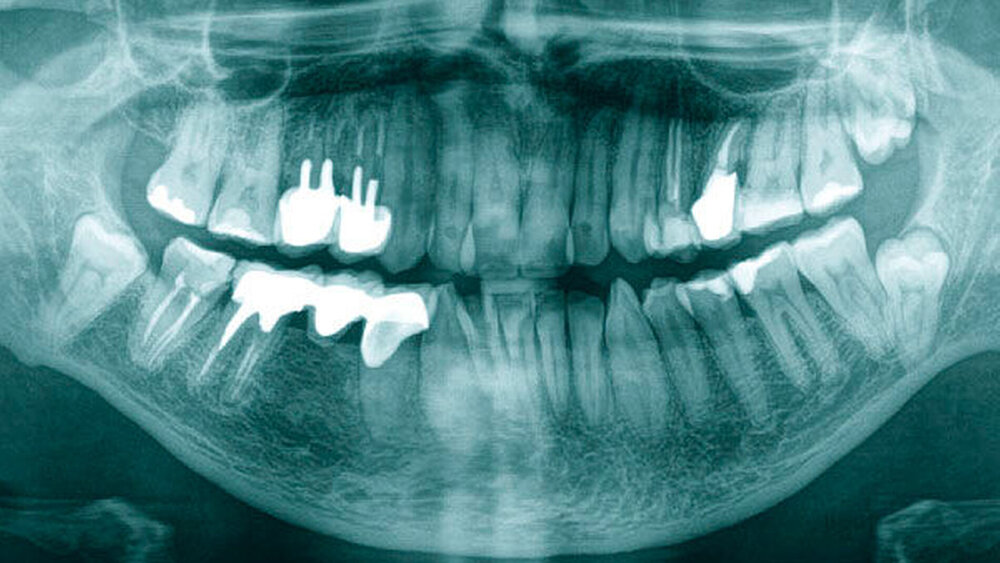
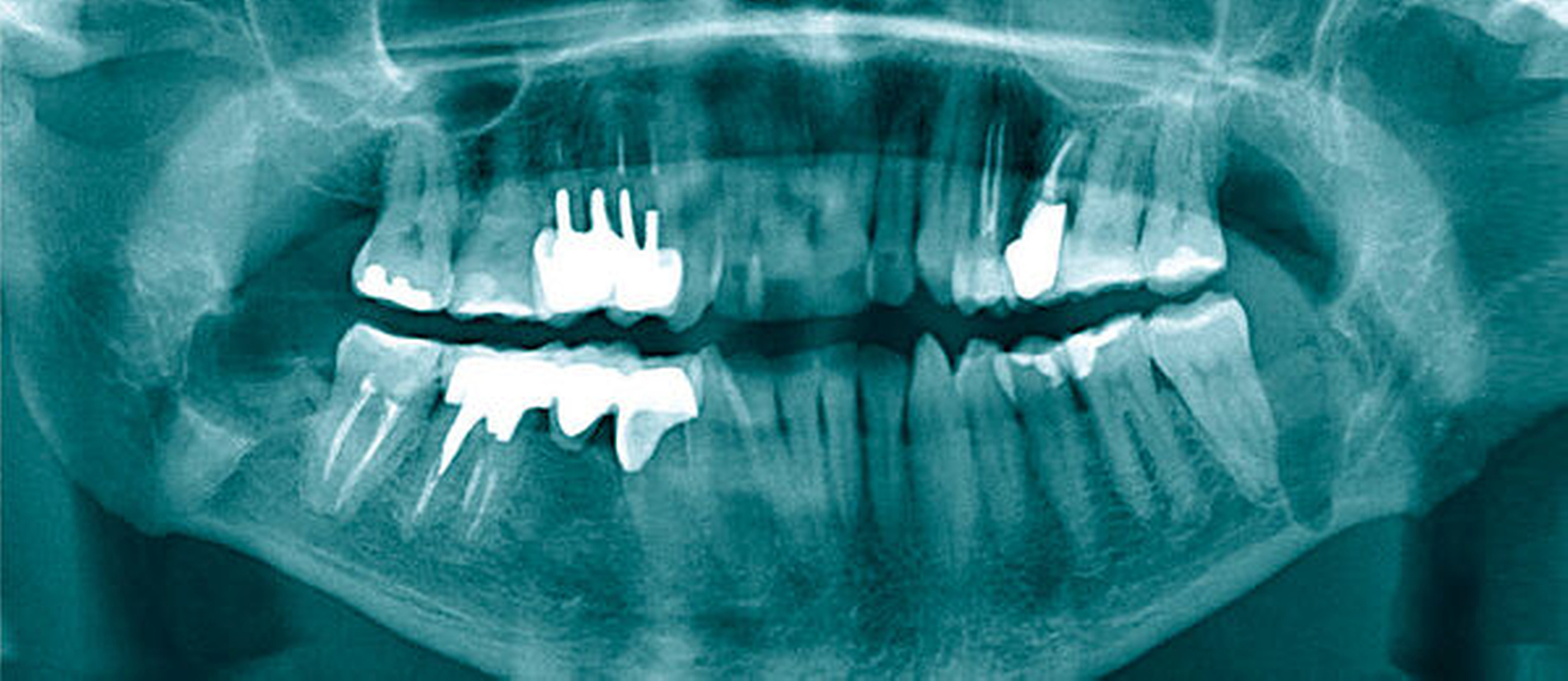
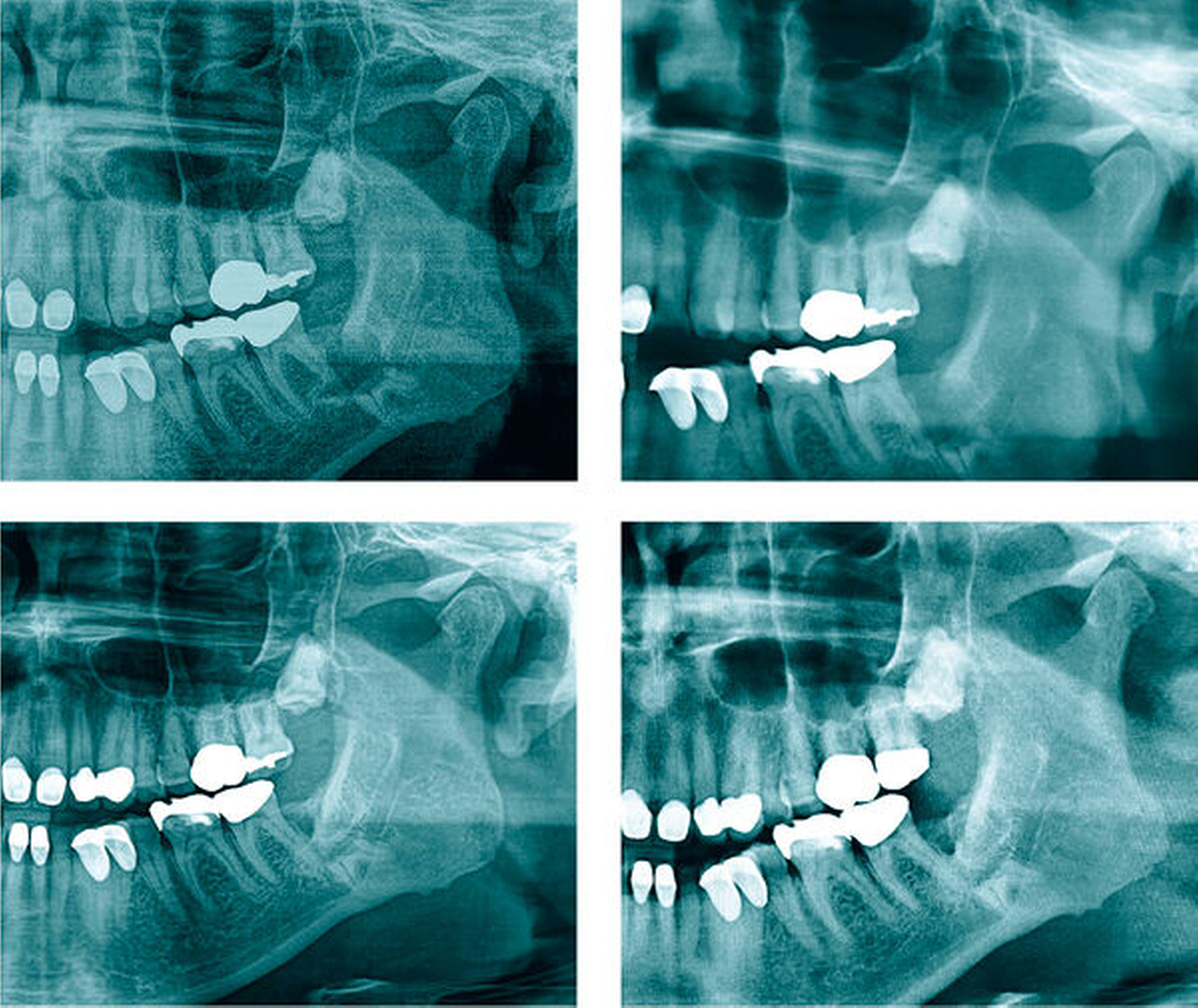
Die vom Kollegen angefertigte Panoramaschichtaufnahme (Abbildung 1) zeigte neben multiplen wurzelgefüllten Zähnen einen in Infraposition befindlichen Zahn 28, einen retinierten Zahn 38 sowie einen retinierten Zahn 48. Da die Zahnwurzeln beider Unterkiefer-Weisheitszähne sehr nah an den Unterkieferrand und in unmittelbarer Nähe zum Mandibularkanal projiziert wurden, entschieden wir uns, eine digitale Volumentomografie (DVT) anzufertigen, um die Lagebeziehung zum Nervus alveolaris inferior weiter abzuklären und die Operation planen zu können.
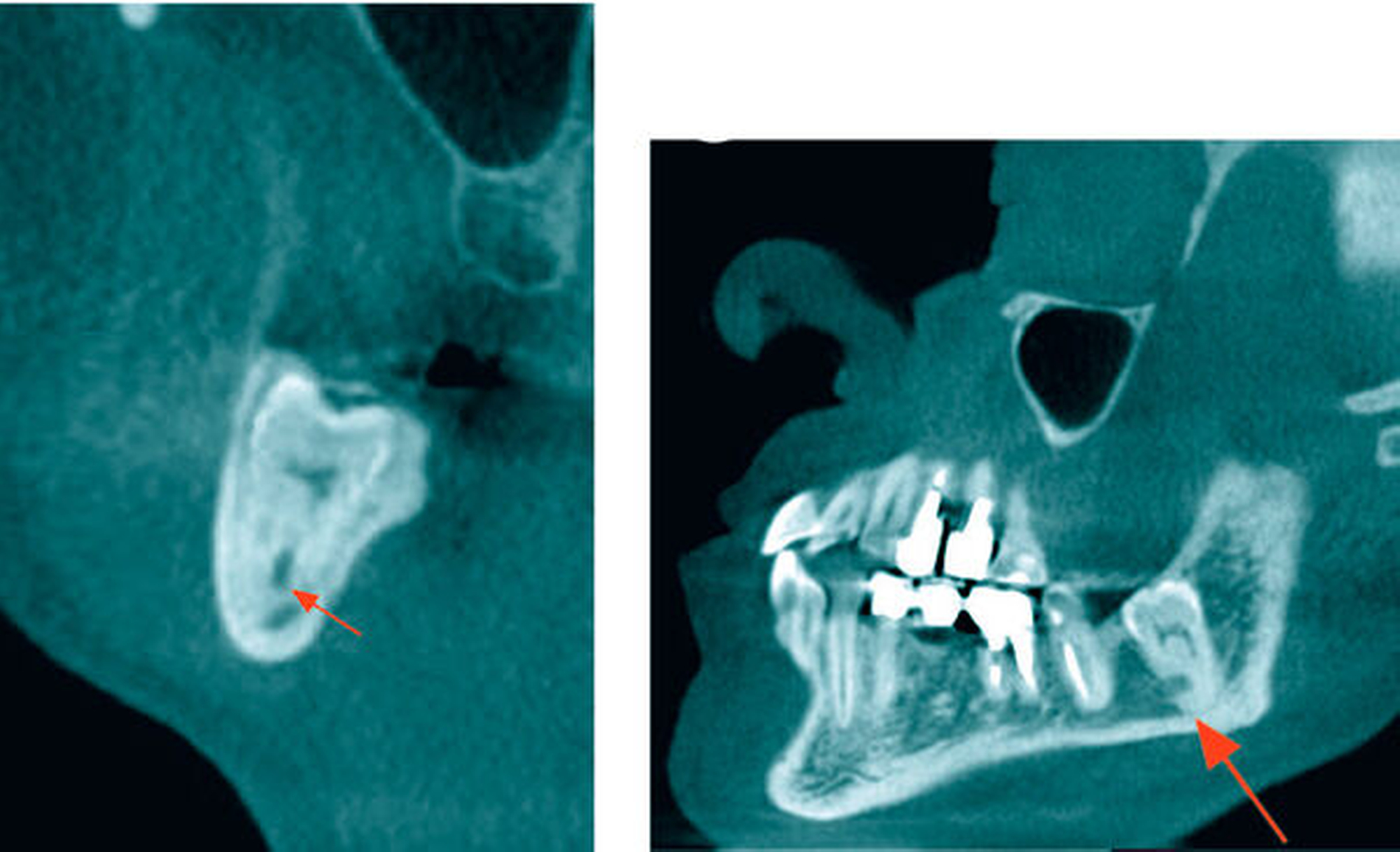
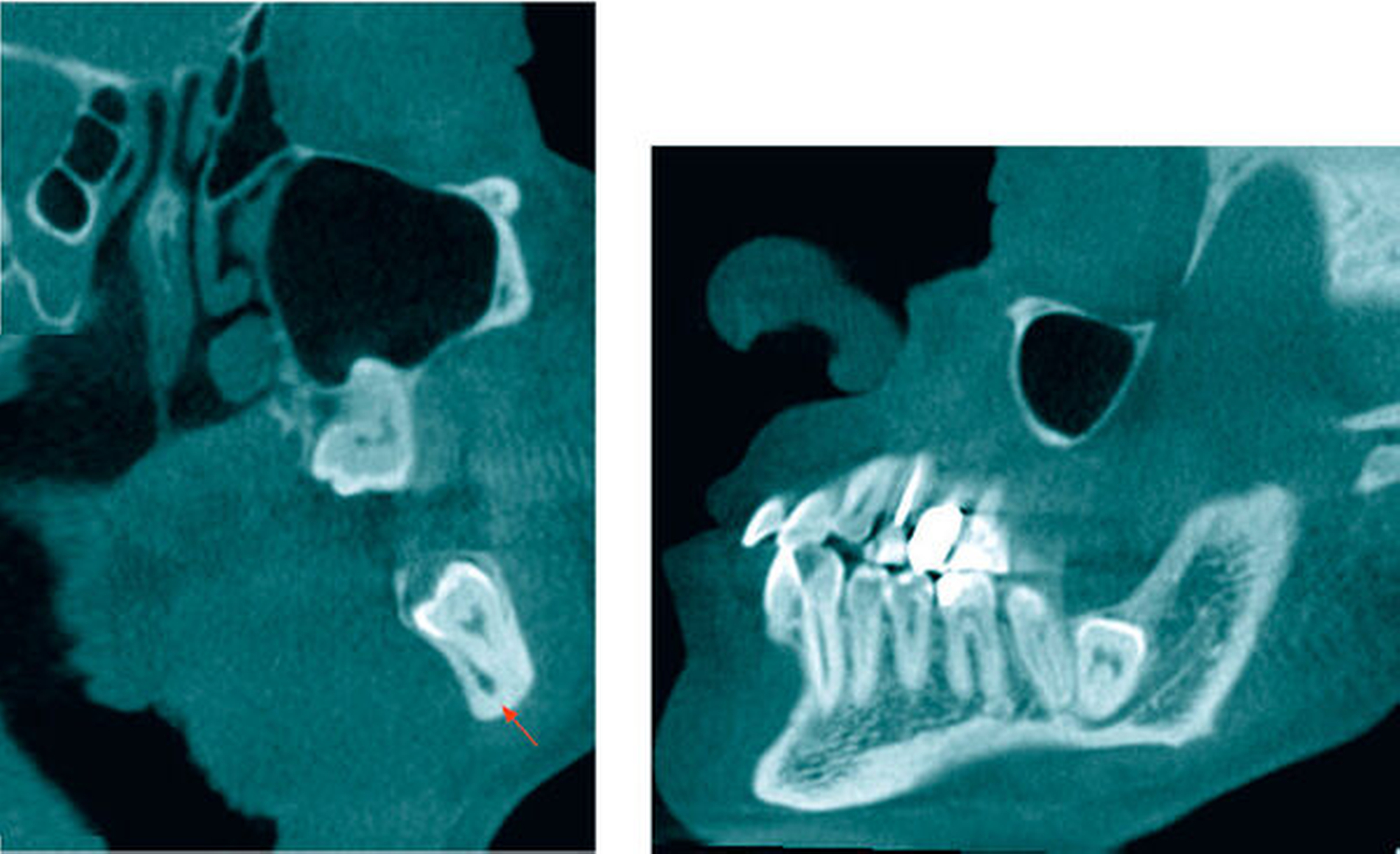
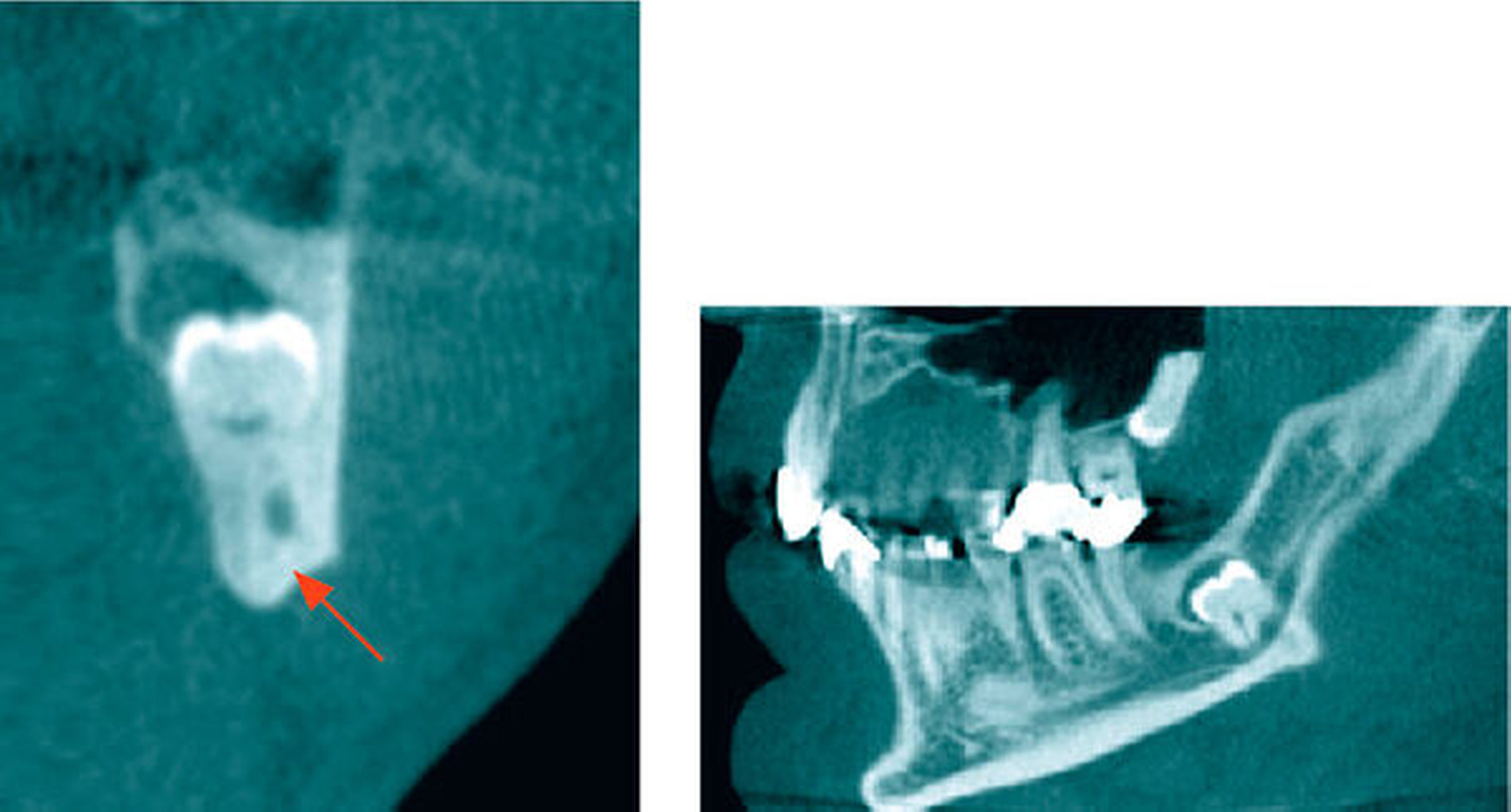
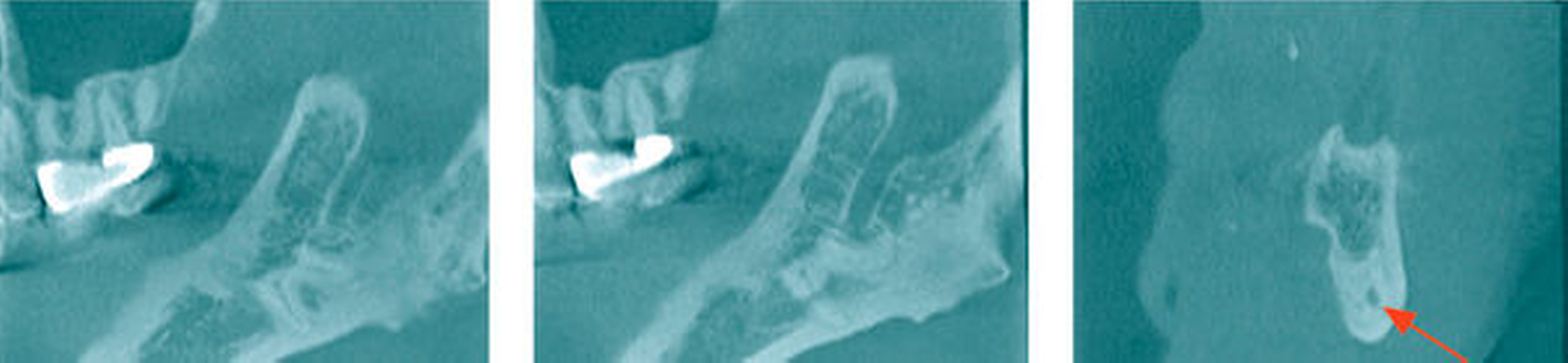
In der koronaren und der sagittalen Schicht des DVT zeigte sich deutlich die Lage beider Apices in der kaudalen Kompakta des Corpus mandibulae. Zudem wurde ein intraradikulärer Verlauf des Canalis mandibularis rechts durch die Wurzeln des 48 (Abbildung 2) erkannt. Am ebenfalls tief retinierten Zahn 38 konnte relativ zur Wurzel des Zahnes 38 ein lingualer Verlauf des Canalis mandibularis verifiziert werden (Abbildung 3).
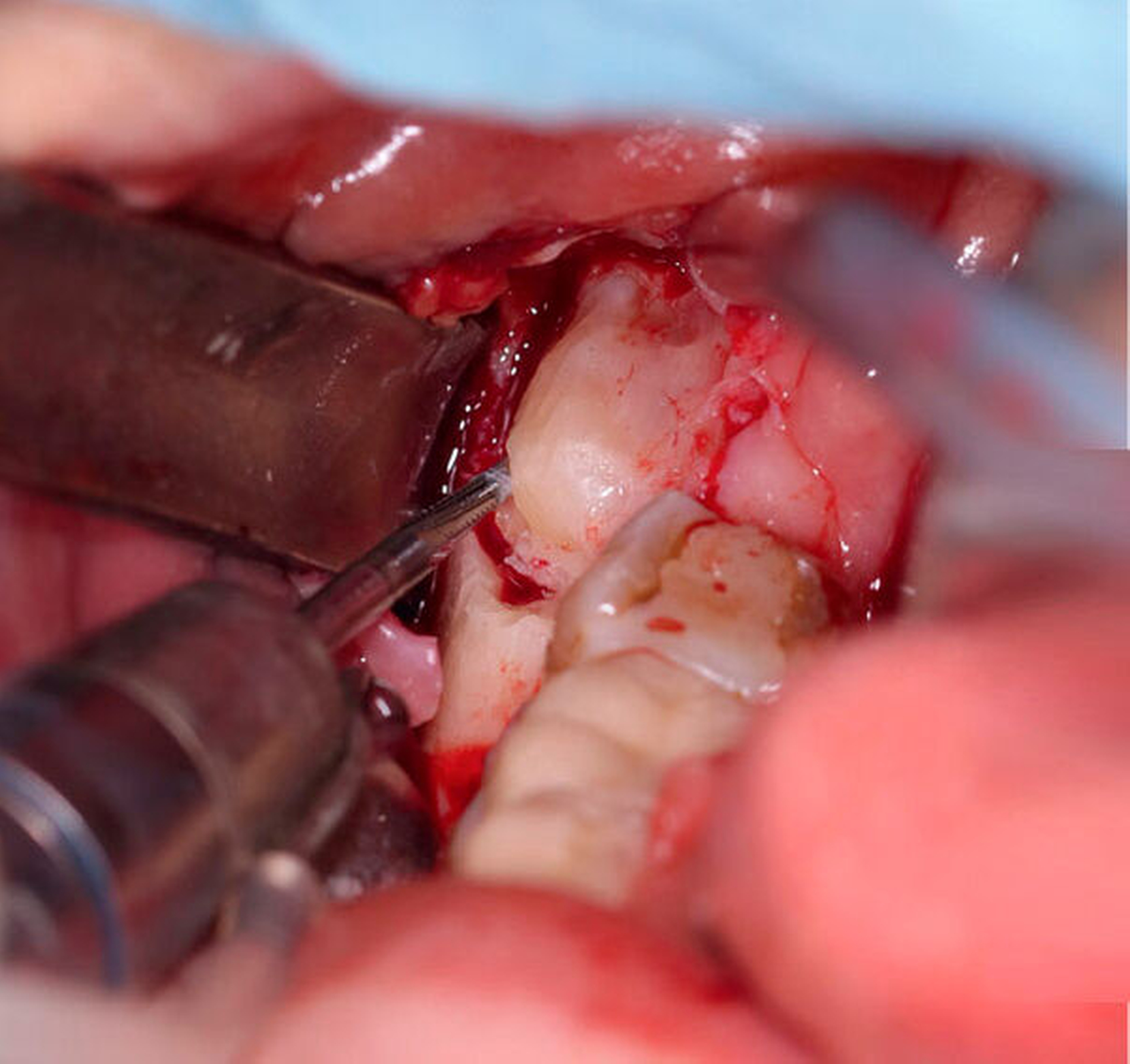
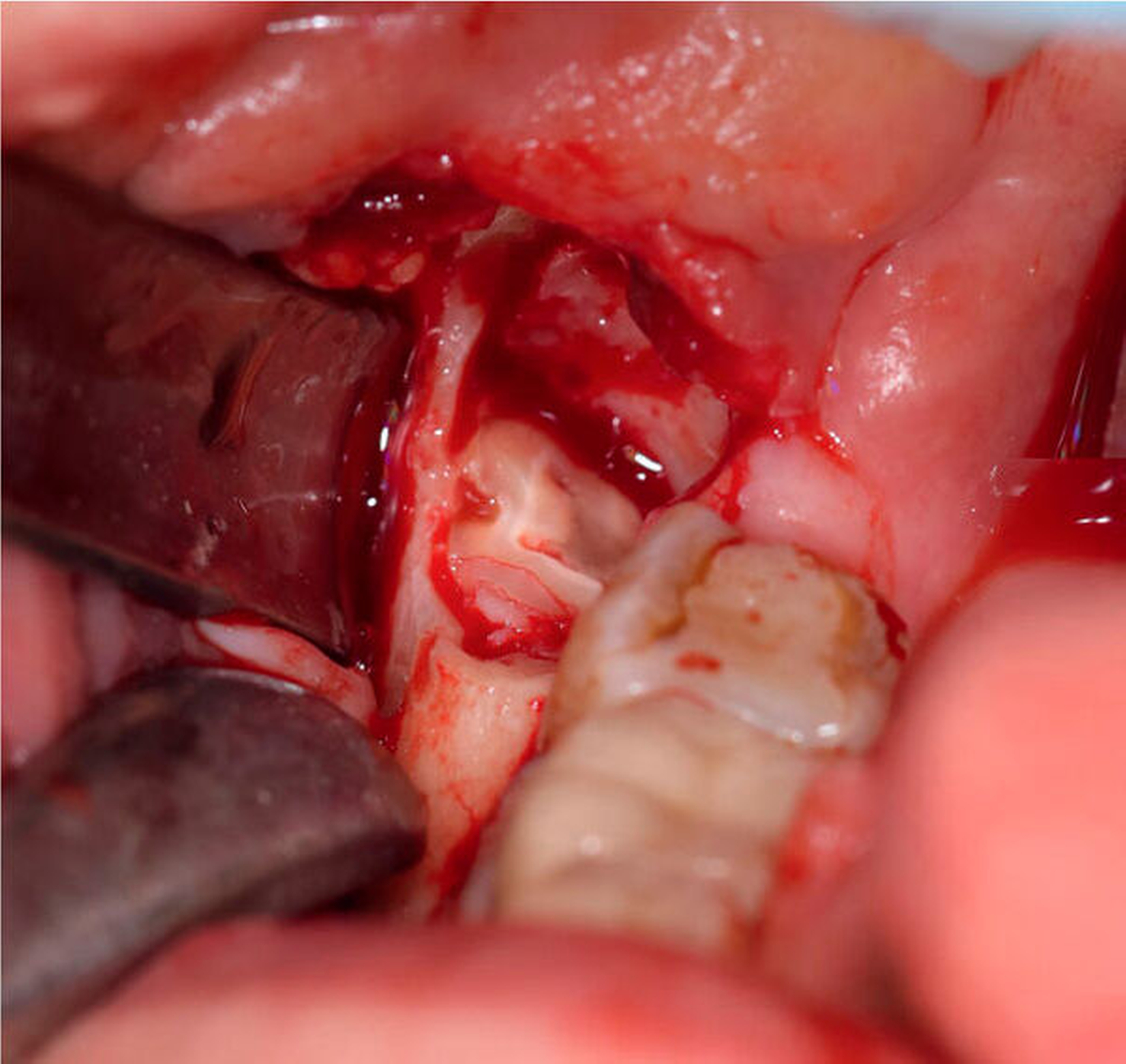
Wir entschieden uns zunächst für die klassische operative Entfernung der Zähne 28 und 38. Aufgrund des Risikos einer Nervschädigung bei der Entfernung des Zahnes 48 wurde zudem eine Koronektomie des Zahns in ambulanter Intubationsnarkose beschlossen. In Regio 48 wurde nach Schnittführung von retromolar nach distal 47 mit vestibulärer Entlastung und Bildung eines Mukoperiostlappens der Zahn 48 freigelegt (Abbildung 4). Die Zahnkrone konnte komplikationslos abgetrennt werden, woraufhin die Glättung des Wurzelblocks bei guter Sicht möglich war (Abbildung 5). Dabei wurde streng darauf geachtet, alle Schmelzanteile resektiv zu entfernen. Anschließend wurden die Wundflächen gereinigt und die Wunde durch Nähte verschlossen. Der postoperative Verlauf war unauffällig und die Patientin wurde am gleichen Tag in die ambulante Nachsorge entlassen. Zur Entzündungsprophylaxe erhielt sie Schmerzmittel. Des Weiteren wurde ihr geraten, eine starke Kaubelastung zu vermeiden.
Die Patientin stellte sich eine Woche postoperativ zur röntgenologischen und klinischen Verlaufskontrolle erneut vor. Die Schmerzen und die Schwellung waren rückläufig, die Wunden enoral heilten regelrecht und unauffällig. Im Versorgungsgebiet des N. alveolaris inferior links war eine dezente Hypästhesie zu beobachten. Eine postoperative Panoramaschichtaufnahme (Abbildung 6) zeigte eine suffiziente Koronektomie rechts ohne verbliebene Schmelzanteile sowie leere Alveolen in Regio 38 und 28. Bei der anschließenden Untersuchung nach einer weiteren Woche zeigte sich die Patientin nahezu schmerzfrei, die Hypästhesie links war rückläufig.
Kasuistik 2
Da beim oben beschriebenen Fall die Verlaufskontrollen noch ausstehen, möchten wir an dieser Stelle einen weiteren Fall präsentieren. Ein mittlerweile 64-jähriger Patient stellte sich Ende März 2021 mit Schmerzen in Regio 28 und zur Verlaufskontrolle des Zahnes 38 nach Koronektomie 2014 vor – nach einer externen Überweisung aufgrund eines komplex verlagerten 38 mit Verdacht auf eine follikuläre Zyste sowie eines hoch verlagerten Zahnes 28. Der Zahn 48 war vor etwa 15 Jahren operativ entfernt worden.
Zur Abklärung der Lagebeziehung des 38 zum N. alveolaris inferior und relativ zum Unterkieferrand sowie zur Abklärung der Verlagerung des 28 beziehungsweise des Zustands der Kieferhöhle links wurde eine DVT durchgeführt. Dabei zeigte sich, dass der Nervkanal zwischen den vestibulär und lingual in der Unterkiefer-Kortikalis endenden Wurzeln des tief vertikal verlagerten Zahnes 38 verlief. Der Zahn 28 wurde mit Kronenbeginn kranial im apikalen Wurzeldrittel des Zahnes 27 vertikal verlagert dargestellt (Abbildung 7).
Nach Abwägung der Risiken (Schädigung des N. alveolaris inferior, hoher Knochensubstanzverlust im Unterkiefer) war damals gemeinsam mit dem Patienten entschieden worden, eine Koronektomie am Zahn 38 durchzuführen. Die erste Verlaufskontrolle erfolgte im März 2015, bei der in der Panoramaschichtaufnahme eine Reossifikation nachgewiesen werden konnte (Abbildung 8). 2017 konnte röntgenologisch koronar der Radices 38 eine suffiziente Knochenneubildung festgestellt werden (Abbildung 8). Der Patient war beschwerdefrei, die Wundverhältnisse waren vollkommen reizlos und ohne Schwellung.
Aktuell wird bei ihm die operative Entfernung des Zahnes 28 geplant, der nun symptomatisch ist. Die Verlaufskontrolle nach der Koronektomie am Zahn 38 vor sieben Jahren zeigte auf der zur Planung der Entfernung von 28 angefertigten Aufnahme einen unauffälligen Befund mit deutlichem Nachweis einer Reossifikation im ehemaligen Kronenbereich (Abbildung 9). Der Patient gab an, dass er mit der Entscheidung damals zufrieden sei und er keinerlei Beschwerden in dieser Region habe.
In der aktuellen, überarbeiteten S3-Leitlinie (Stand August 2019) der Deutschen Gesellschaft für Mund-, Kiefer- und Gesichtschirurgie (DGMKG) und der Deutschen Gesellschaft für Zahn-, Mund- und Kieferheilkunde (DGZMK) zur operativen Entfernung von Weisheitszähnen stellen die Anamnese, die klinische Untersuchung und die radiologische Bildgebung zur Darstellung des Zahnstatus die zentrale Rolle in der Therapieentscheidung dar [DGZMK, 2019].
Falls die Weisheitszähne klinisch sowie röntgenologisch unauffällig sind, können sie durchaus belassen werden. Sie können kieferorthopädisch eingegliedert oder für eine prothetische Versorgung verwendet werden. Das Belassen der Weisheitszähne wird zudem empfohlen, wenn die Zähne tief impaktiert und verlagert sind. Es wird davon abgeraten die Zähne zu entfernen, falls die Operation ein zu hohes Risiko für weiterführende Komplikationen birgt [DGZMK, 2019]. Doch auch das Belassen der Zähne kann Komplikationen nach sich ziehen. Diese entwickeln sich häufiger im Alter zwischen 18 und 35 Jahren [Fernandes et al., 2010]. Dazu werden Infektionen durch Perikoronitis, die Resorption der Wurzeln des Nachbarmolaren, dessen parodontale Schädigung und die Entwicklung von Karies gezählt. Außerdem können sich dentogene Zysten, Neoplasien und Okklusionsstörungen durch Elongation oder Kippung der Nachbarzähne entwickeln [DGZMK, 2019; Pratt et al., 1998].
Die operative Entfernung der Weisheitszähne wird unter anderem bei akuten oder chronischen Infektionen, bei unklaren Gesichtsschmerzen und bei nicht restaurierfähigen Zähnen empfohlen. Allgemeine Komplikationen der Weisheitszahnentfernung können postoperative Infektionen mit Schwellung und Schmerz, die Schädigung der zweiten Molaren, mögliche Kieferfrakturen, die Eröffnung des Sinus maxillaris sowie perioperative und anästhesiologische Komplikationen sein [DGZMK, 2019; McGrath et al., 2003; Lim et al., 2012]. Bei einer sehr nahen Lage der Zahnwurzeln zum N. alveolaris inferior besteht zudem ein erhöhtes Risiko einer Nervenschädigung. So kann es bei röntgenologisch nachgewiesener enger Lagebeziehung in bis zu 20 Prozent der Fälle zu temporären und in ein bis vier Prozent zu permanenten Sensibilitätsstörungen kommen [Renton, 2012]. Das Risiko der Nervenschädigung nimmt dabei mit der Nähe der Zahnwurzel zum Mandibularkanal zu [Eyrich et al., 2011].
Besondere Risikofaktoren für die Schädigung des N. alveolaris inferior (die Rate wird im Bereich von 0,26 bis 8,4 Prozent [Leung und Cheung, 2011] angegeben) sind beispielsweise ein erhöhtes Alter (über 25 Jahre), impaktierte Weisheitszähne sowie eine Exposition des Nervs. Risikofaktoren für die Verletzung des Nervus lingualis (in 0,1 bis 22 Prozent der Fälle [Leung und Cheung, 2011]) stellen linguale Lappenplastiken, eine linguale Split-Technik und sehr tief verlagerte Weisheitszähne [Leung und Cheung, 2011; Chuang et al., 2007] dar. Patienten erfahren bei verletztem N. alveolaris inferior Parästhesien, Anästhesien oder Dysästhesien der Lippe, des Kinns oder der bukkalen Gingiva, wohingegen sie bei Schädigung des N. lingualis unter veränderter Empfindung an der Zunge mit der Gefahr einer Geschmacksstörung leiden. Bei einigen der Patienten bleiben die Sensibilitätsstörungen dauerhaft bestehen [Blondeau und Daniel, 2007; Jerjes et al., 2006], sind schwierig zu therapieren und schränken die Patienten sehr in ihrer Lebensqualität ein [Smith et al., 2013].
Wenn schonend operiert wird, geht man bei Weisheitszahnentfernungen aber dennoch von einem geringen Komplikationsrisiko aus. Die postoperative Alveolitis/Wundinfektion wird als häufigste Komplikation beschrieben [Voegelin et al., 2008]. Die Inzidenz variiert hier von Studie zu Studie stark, vom niedrigsten Wert von 0,5 Prozent bis hin zum höchsten von 68,4 Prozent [Blondeau und Daniel, 2007]. Im Durchschnitt wird sie zwischen 5 und 10 Prozent angegeben [Bui et al., 2003; Sisk et al., 1986; Blondeau und Daniel, 2007].
Neben der klassischen Weisheitzahnentfernung wird in der aktuellen Leitlinie die Koronektomie aufgegriffen. Diese Methode wurde bereits 1989 durch Knutsson et al. als Alternativtherapie zur Weisheitszahnentfernung in toto beschrieben, um dauerhafte, postoperative Sensibilitätsstörungen zu vermeiden [Wolf and Renton, 2016; Knutsson et al., 1989]. Insbesondere in Großbritannien rückte sie in den vergangenen Jahren mehr in den Fokus und wird häufig positiv bewertet [Renton et al., 2005; Renton, 2012]. Laut einer Befragung von Mitgliedern der British Association of Oral Surgeons (BAOS) wurden 2015 in 73 Prozent der Fälle Koronektomien angeboten [Devine et al., 2017].
Fazit für die Praxis
Die Koronektomie kann als geeignete Alternative zur klassischen Weisheitszahnentfernung bei enger Lagebeziehung zum N. alveolaris inferior im Unterkiefer zu dessen Schutz bewertet werden.
Die Koronektomie ist ausschließlich bei gesunden Patienten indiziert. Sie sollte die klassische Weisheitszahnentfernung nicht ersetzen, sondern für Fälle mit hohem Schädigungsrisiko vorbehalten bleiben.
Bei komplex erscheinender Lage und Lagebeziehung des zu entfernenden Zahnes zum Canalis mandibulae im OPG kann eine digitale Volumentomografie zur weiterführenden Diagnostik in Erwägung gezogen werden.
Interessant ist eine Studie von Crameri et al. [2018], die eine anonyme Befragung von 266 Oral- und Mund-Kiefer-Gesichts-Chirurgen in der Schweiz zum Thema Koronektomie durchführten. 51,6 Prozent gaben an, die Technik als unzuverlässig anzusehen. Bei einem hohen Risiko für eine Nervschädigung des N. alveolaris inferior wurden in 40,6 Prozent der Fälle Koronektomien angeboten, etwa 69 Prozent konnten sich eine Koronektomie vorstellen und 54,8 Prozent hatten bisher noch nie eine Koronektomie durchgeführt. Die Autoren nehmen an, dass die Ursache dieser eher kritischen Einstellung daher rührt, dass die Technik nicht verbreitet oder deren technische Umsetzung nicht ausreichend bekannt ist [Crameri und Kuttenberger, 2018].
Im Vergleich zur klassischen Zahnextraktion wird die Rate des postoperativen Infektionsgeschehens ähnlich hoch eingeschätzt [Leung und Cheung, 2009]. Nach einer Koronektomie kann in zehn bis zwölf Prozent der Fälle eine Alveolitis auftreten. Diese wird wie nach einer Zahnextraktion mittels Wundspülung und Wunddrainage behandelt [Renton et al., 2005; Wolf und Renton, 2016]. Die Inzidenz einer Alveolitis wie auch von Sensibilitätsstörungen wird nach einer Koronektomie jedoch geringer als nach klassischer Zahnentfernung eingeschätzt [Cervera-Espert et al., 2016].
Nach einer Koronektomie besteht hingegen das Risiko der Migration des Wurzelblocks oder dessen intraoperatives Anluxieren. Oftmals muss der Wurzelblock dann in einem Zweiteingriff entfernt werden. Um eine Migration des Wurzelblocks frühzeitig zu erkennen, sind radiologische Verlaufskontrollen notwendig [Wolf und Renton, 2016; Renton, 2012]. In den ersten zwölf Wochen ist die Tendenz zur Migration erhöht. Die Distanz beträgt nach einer Studie im Durchschnitt etwa 1,9 mm. Danach nimmt die Tendenz ab, es können aber Maximalwerte bis zu 6 mm erreicht werden [Leung und Cheung, 2009]. Laut einer aktuelleren Studie kann die Migrationstendenz bei Koronektomien aber verringert werden, wenn diese mit der sogenannten Guided-Bone-Regeneration-Technik kombiniert wird. Bei dieser Technik wird Knochenersatzmaterial auf den Wurzelblock aufgetragen. Anschließend werden das Material mit einer Kollagenmembran bedeckt und die Wunde dicht verschlossen. Die Autoren gehen davon aus, dass dabei das Risiko einer Exposition des Wurzelblocks nach mehr als drei Jahren verringert werden kann, da die Wurzelblöcke von regenerierendem Knochen bedeckt werden. Dadurch kann ein Zweiteingriff vermieden werden [Leung, 2019]. Histologische Untersuchungen verbliebener Wurzelblöcke nach Koronektomie, die in einem Zweiteingriff entfernt wurden, zeigten, dass diese keine Anzeichen einer Inflammation oder Nekrose aufwiesen. Patel et al. beschrieben in allen Wurzeln vitales Pulpengewebe und keine Hinweise auf eine periradikuläre Entzündung. Persistierende postoperative Symptome wurden auf eine Entzündung des Weichgewebes und eine Störung der Wundheilung zurückgeführt [Patel et al., 2014].
Kontraindikationen für eine Koronektomie ergeben sich bei Pulpanekrose, Karies profunda mit Pulpitis oder horizontaler Verlagerung. Zudem sollte eine Koronektomie vermieden werden, falls die Patienten immunsupprimiert sind, unter Diabetes leiden oder Bisphosphonate einnehmen [Wolf und Renton, 2016]. Die Koronektomie ist ausschließlich bei gesunden Patienten indiziert, wenn eine komplexe oder nahe Lage der Zahnwurzeln zum N. alveolaris inferior besteht. Sie sollte eine klassische Weisheitszahnentfernung nicht ersetzen [Wolf und Renton, 2016], sondern als Alternative für Fälle mit hohem Schädigungsrisiko vorbehalten bleiben [DGZMK, 2019].
Einige Autoren sind der Meinung, dass die Verfügbarkeit von dreidimensionalen Bildinformationen die Risikostratifizierung für die OP-Planung verbessern kann, wenn Risikofaktoren durch eine zweidimensionale Bildgebung nicht auszuschließen sind [Eyrich et al., 2011; Umar et al., 2013; Renton, 2012]. Die European Academy of DentoMaxilloFacial Radiology (EADMFR) verweist darauf, dass die digitale Volumentomografie nicht als Routineuntersuchung genutzt werden sollte, sondern nur für spezifische Fragestellungen, die in der zweidimensionalen Aufnahme nicht beantwortet werden können. Im Fall der Koronektomie sollte diese Untersuchung also nur dann angewendet werden, wenn die Weisheitszähne bereits erhöhte Risikofaktoren für eine Nervschädigung aufweisen [Matzen und Berkhout, 2019]. Zu diesen Faktoren zählen eine apikale Abweichung des Nervenkanals, eine Aufhellung im Wurzelbereich durch dessen Überlagerung sowie eine unterbrochene Lamina dura des Nervenkanals [Alantar et al., 1995]. Die EADMRF verglich diverse Studien und schlussfolgerte, dass die präoperative 3-D-Planung das Auftreten von postoperativen Sensibilitätsstörungen nach einer Weisheitszahnentfernung im Vergleich zur präoperativen zweidimensionalen Bildgebung nicht reduzieren kann [Matzen und Berkhout, 2019]. Auch in der aktuellen AWMF-Leitlinie wird ein DVT oder CT nur für Ausnahmefälle empfohlen [DGZMK, 2019].
Abschließend kann in Anbetracht des aktuellen Forschungsstands die Koronektomie als gute Alternative zur klassischen Weisheitszahnextraktion im Unterkiefer bei enger Lagebeziehung zum N. alveolaris inferior zu dessen Schutz bewertet werden. Um das operative Vorgehen besser planen zu können, kann bei komplex erscheinender Lage und Lagebeziehung des zu entfernenden Zahnes zum Canalis mandibulae im OPG eine digitale Volumentomografie zur weiterführenden Diagnostik in Erwägung gezogen werden [Eyrich et al., 2011].
Dr. Med. Saskia Schröger
Klinik und Poliklinik für MKG-Chirurgie der Universitätsmedizin Mainz
Augustusplatz 3, 55131 Mainz
saskia.schroeger@unimedizin-mainz.de
Prof. Dr. Med. Dent. Ralf Schulze
Sektionsleiter zahnärztliche Radiologie Klinik und Poliklinik für MKG-Chirurgie der Universitätsmedizin Mainz
Augustusplatz 3, 55131 Mainz
Univ.-Porf. Dr. Dr. Peer W. Kämmerer, MA, FEBOMFS
Leitender Oberarzt und stellvertretender Klinikdirektor Klinik und Poliklinik für Mund-, Kiefer- und Gesichtschirurgie, Plastische Operationen, Universitätsmedizin Mainz
Augustusplatz 2, 55131 Mainz
peer.kaemmerer@unimedizin-mainz.de
Literaturliste
DGZMK, P. D. D. M. K. August 2019. S3-Leitlinie „operative Entfernung von Weisheitszähnen“ Langversion).
AAOMS 2013. Evidence based third molar surgery. White paper.
Alantar, A., Roisin-Chausson, M. H., Commissionat, Y., Aaron, C., Barda, L., Debien, J., Ecuyer, J. & Hassin, M. 1995. Retention of third molar roots to prevent damage to the inferior alveolar nerve. Oral Surg Oral Med Oral Pathol Oral Radiol Endod, 80, 126.
Blondeau, F. & Daniel, N. G. 2007. Extraction of impacted mandibular third molars: postoperative complications and their risk factors. J Can Dent Assoc, 73, 325.
Brauer, H., Green, R., Arnold, J., Wilson, D. & Pynn, B. 2015. Koronektomie (intentionelle chirurgische Teilentfernung unterer Weisheitszähne) – Ein Update. ZWR - Das Deutsche Zahnärzteblatt, 124, 458-461.
Bui, C. H., Seldin, E. B. & Dodson, T. B. 2003. Types, frequencies, and risk factors for complications after third molar extraction. J Oral Maxillofac Surg, 61, 1379-89.
Cervera-Espert, J., Pérez-Martínez, S., Cervera-Ballester, J., Peñarrocha-Oltra, D. & Peñarrocha-Diago, M. 2016. Coronectomy of impacted mandibular third molars: A meta-analysis and systematic review of the literature. Med Oral Patol Oral Cir Bucal, 21, e505-13.
Chuang, S. K., Perrott, D. H., Susarla, S. M. & Dodson, T. B. 2007. Age as a risk factor for third molar surgery complications. J Oral Maxillofac Surg, 65, 1685-92.
Crameri, M. & Kuttenberger, J. J. 2018. Application and evaluation of coronectomy in Switzerland. Swiss Dent J, 128, 582-586.
Devine, M., Gerrard, G. & Renton, T. 2017. Current practice in mandibular third molar surgery. A national survey of British Association of Oral Surgeons membership. Oral Surgery, 10, 11-19.
Dodson, T. B. & Susarla, S. M. 2014. Impacted wisdom teeth. BMJ Clin Evid, 2014.
Eyrich, G., Seifert, B., Matthews, F., Matthiessen, U., Heusser, C. K., Kruse, A. L., Obwegeser, J. A. & Lübbers, H. T. 2011. 3-Dimensional imaging for lower third molars: is there an implication for surgical removal? J Oral Maxillofac Surg, 69, 1867-72.
Fernandes, M. J., Ogden, G. R., Pitts, N. B., Ogston, S. A. & Ruta, D. A. 2010. Actuarial life-table analysis of lower impacted wisdom teeth in general dental practice. Community Dent Oral Epidemiol, 38, 58-67.
Jerjes, W., Swinson, B., Moles, D. R., El-Maaytah, M., Banu, B., Upile, T., Kumar, M., Al Khawalde, M., Vourvachis, M., Hadi, H., Kumar, S. & Hopper, C. 2006. Permanent sensory nerve impairment following third molar surgery: a prospective study. Oral Surg Oral Med Oral Pathol Oral Radiol Endod, 102, e1-7.
Knutsson, K., Lysell, L. & Rohlin, M. 1989. Postoperative status after partial removal of the mandibular third molar. Swed Dent J, 13, 15-22.
Leung, Y. Y. 2019. Guided bone regeneration to reduce root migration after coronectomy of lower third molar: a randomized clinical trial. Clin Oral Investig, 23, 1595-1604.
Leung, Y. Y. & Cheung, L. K. 2009. Safety of coronectomy versus excision of wisdom teeth: a randomized controlled trial. Oral Surg Oral Med Oral Pathol Oral Radiol Endod, 108, 821-7.
Leung, Y. Y. & Cheung, L. K. 2011. Risk factors of neurosensory deficits in lower third molar surgery: an literature review of prospective studies. Int J Oral Maxillofac Surg, 40, 1-10.
Lim, A. A., Wong, C. W. & Allen, J. C., Jr. 2012. Maxillary third molar: patterns of impaction and their relation to oroantral perforation. J Oral Maxillofac Surg, 70, 1035-9.
Matzen, L. H. & Berkhout, E. 2019. Cone beam CT imaging of the mandibular third molar: a position paper prepared by the European Academy of DentoMaxilloFacial Radiology (EADMFR). Dentomaxillofac Radiol, 48, 20190039.
McGrath, C., Comfort, M. B., Lo, E. C. & Luo, Y. 2003. Changes in life quality following third molar surgery--the immediate postoperative period. Br Dent J, 194, 265-8; discussion 261.
Patel, V., Sproat, C., Kwok, J., Beneng, K., Thavaraj, S. & McGurk, M. 2014. Histological evaluation of mandibular third molar roots retrieved after coronectomy. Br J Oral Maxillofac Surg, 52, 415-9.
Pratt, C. A., Hekmat, M., Barnard, J. D. & Zaki, G. A. 1998. Indications for third molar surgery. J R Coll Surg Edinb, 43, 105-8.
Renton, T. 2012. Notes on coronectomy. Br Dent J, 212, 323-6.
Renton, T., Hankins, M., Sproate, C. & McGurk, M. 2005. A randomised controlled clinical trial to compare the incidence of injury to the inferior alveolar nerve as a result of coronectomy and removal of mandibular third molars. Br J Oral Maxillofac Surg, 43, 7-12.
Sisk, A. L., Hammer, W. B., Shelton, D. W. & Joy, E. D., Jr. 1986. Complications following removal of impacted third molars: the role of the experience of the surgeon. J Oral Maxillofac Surg, 44, 855-9.
Smith, J. G., Elias, L. A., Yilmaz, Z., Barker, S., Shah, K., Shah, S. & Renton, T. 2013. The psychosocial and affective burden of posttraumatic neuropathy following injuries to the trigeminal nerve. J Orofac Pain, 27, 293-303.
Umar, G., Obisesan, O., Bryant, C. & Rood, J. P. 2013. Elimination of permanent injuries to the inferior alveolar nerve following surgical intervention of the „high risk“ third molar. Br J Oral Maxillofac Surg, 51, 353-7.
Voegelin, T. C., Suter, V. G. & Bornstein, M. M. 2008. [Complications during and after surgical removal of mandibular third molars. Impact of patient related and anatomical factors]. Schweiz Monatsschr Zahnmed, 118, 192-8.
Wolf, D. & Renton, T. 2016. Die Koronektomie als Alternativtherapie Swiss Dent J, 126, 1147-1159.