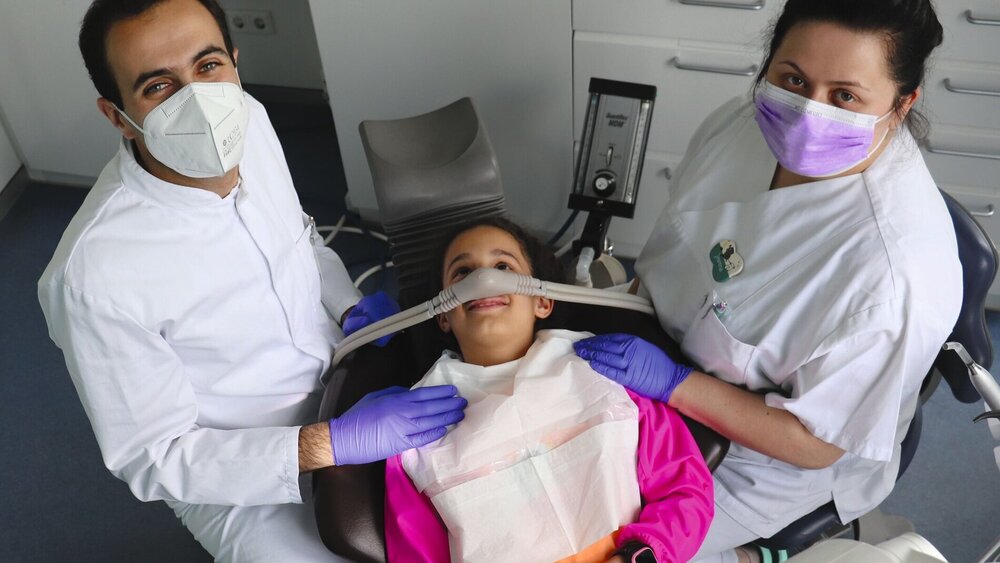
Lachgassedierung – eine Alternative zur zahnärztlichen Narkose bei Kindern
Die zahnärztliche Behandlung von ängstlichen Kindern ist äußerst anspruchsvoll. Insgesamt 10 bis 30 Prozent der Kinder und Erwachsenen haben eine Form von Angst vor Zahnbehandlungen und „Angst vor dem Zahnarzt“ kann zu nicht kooperativem Verhalten bei Kindern führen [Council of European Dentists, 2014; Hennequin et al., 2012]. Kinder mit großer Zahnarztangst haben ein etwa doppelt so hohes Risiko für unbehandelte kariöse Defekte im Vergleich zu Kindern mit geringer Angst [Murthy et al., 2014].
Mithilfe der Lachgassedierung gelingt es häufig, diese Angst zu reduzieren und so günstigere Behandlungsbedingungen zu schaffen. Dies kann auch helfen, eine langfristig positive Einstellung zum Zahnarztbesuch zu entwickeln. Lachgassedierungen können mitunter sogar eine Alternative zur Narkose darstellen. Gerade bei überschaubarem Behandlungsbedarf ist deswegen bei potenziell kooperativen Kindern ab circa fünf Jahren, aber auch bei Erwachsenen, die Abwägung einer Lachgassedierung im Vergleich zur Narkose zwingend geboten [Hallonsten et al., 2003]. Die Sedierung mit Lachgas ist seit vielen Jahrzehnten in der Zahnmedizin etabliert und in den Empfehlungen der Europäischen Akademie für Kinderzahnheilkunde detailliert beschrieben [Hallonsten et al., 2003].
Wirkung
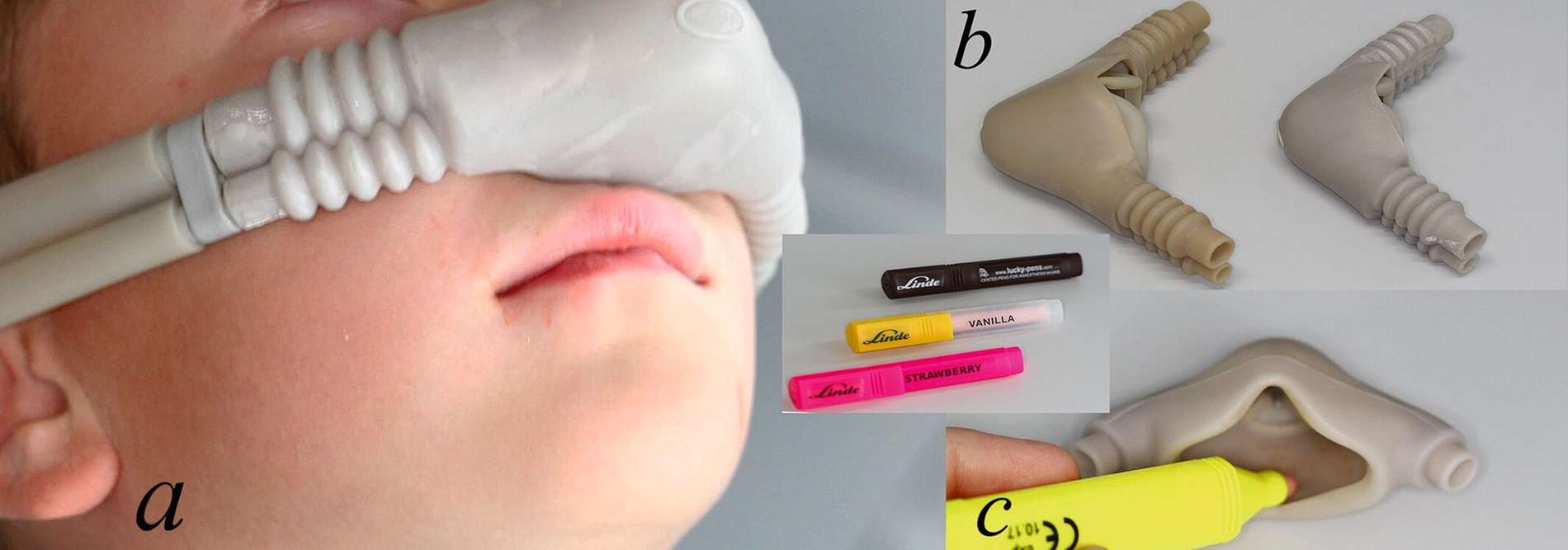
Lachgas hat eine gute sedierende und mittlere schmerzlindernde Wirkung, das heißt für invasive Zahnbehandlungen ist in der Regel zusätzlich eine Lokalanästhesie erforderlich [Zier et al., 2010]. Der sedierte Patient fühlt sich meist ruhig, teilweise aber auch fröhlich bei seelischer und körperlicher Entspannung. Die Fähigkeit des Patienten zur verbalen und nonverbalen Kommunikation bleibt in der Regel bei subanästhetischen Konzentrationen (≤ 50 Prozent Lachgas) erhalten (Abbildung 1a), das heißt der Patient bleibt ansprechbar. Die Atmung wird ruhig und tief, der Würgereiz verschwindet meist fast völlig. Die Schmerzwahrnehmung und -reaktion sind vermindert und die Erinnerungsfähigkeit wird reduziert. Die Lachgassedierung ersetzt aber nicht die Techniken der Verhaltensformung wie „Tell-Show-Do“, eine Desensibilisierung oder hypnotische Sprachmuster. Insbesondere durch Kombination von Lachgassedierung und verhaltensführenden Maßnahmen ist eine deutlich verbesserte Kooperation der Patienten zu erzielen.
Da das Lachgas eine geringe Löslichkeit in Blut und Fett hat, sind Wirkungseintritt und Wirkungsaustritt sehr rasch innerhalb weniger Minuten zu beobachten [Tobias, 2013; Wang et al., 2002]. Die Lachgassedierung kann bei Kindern, Jugendlichen und Erwachsenen für die üblichen Zahnbehandlungen, aber auch gut für kleine chirurgische Eingriffe eingesetzt werden. Der Patient muss jedoch behandlungswillig sein, das heißt, die Nasenmaske muss toleriert werden und das Lachgas-Sauerstoff-Gemisch darüber eingeatmet werden. Zudem eignet sich Lachgas bei Patienten mit starkem Würgereiz, der dann meist völlig verschwindet. Bislang wurden keine schwerwiegenden unerwünschten Ereignisse bei der Lachgassedierung in der Zahnheilkunde registriert [Hennequin et al., 2012]. Bei richtlinientreuer Anwendung (AAPD, EAPD) unter entsprechenden Rahmenbedingungen wie der Nutzung eines titrierbaren Systems, der fachkundigen Anwendung und dem Einsatz eines Absaugsystems beziehungsweise der Raumbelüftung wird Lachgas für Anwender und Patienten als sicher beschrieben [American Academy of Pediatric Dentistry, 2022; Tobias, 2013; Hallonsten et al., 2003].
Technik und Durchführung
In der Zahnarztpraxis sollte ein titrierbares System verwendet werden, bei dem das Sauerstoff-Stickoxydul-Gemisch in seiner Konzentration eingestellt werden kann, (Abbildung 2a). Der N2O-Anteil kann in der Regel null bis 50 Prozent des Atemgemischs betragen. Zu Beginn der Sedierung sollte zunächst reiner Sauerstoff (100 Prozent) über die Nasenmaske eingeatmet werden. Dann kann die Lachgaskonzentration schrittweise bis auf 30 bis 50 Prozent hochtitriert werden, um die gewünschte Sedierungstiefe zu erreichen. Bei den meisten Patienten reicht eine Lachgaskonzentration von 30 bis 40 Prozent aus. Am Ende der Behandlung und vor dem Entfernen der Nasenmaske sollte noch für drei bis fünf Minuten reiner Sauerstoff verabreicht werden [American Academy of Pediatric Dentistry, 2022; Höhne et al., 2021].
Die Anschlüsse für Sauerstoff-Stickoxydul müssen verwechslungssicher sein und ein eingebautes Druckreduziersystem mit Druckanzeige enthalten. Es muss ein Anschluss für eine Notfallsauerstoffmaske vorhanden sein. Bei einer Unterbrechung des Sauerstoffflusses muss der Lachgasfluss automatisch unterbrochen werden und es muss eine ausreichend große Sauerstoffreserve zur Verfügung stehen, um Patienten ausreichend lange beatmen zu können. Die Praxis sollte mit folgenden Elementenausgerüstet sein [American Academy of Pediatric Dentistry, 2022; Hallonsten et al., 2003]:
Nasenmasken in verschiedenen Größen (Abbildung 1b)
Lachgasmischer als individualisierbares, das heißt titrierbares System (Abbildung 2a)
Mietflaschen oder zentrale Anlage (Abbildungen 2b und 2c)
Eventuell externe Absaugung für ausgeatmete Luft mit Sekretabsaugung (Abbildung 3a)
Raumabsaugung beziehungsweise -entlüftung im Bodenbereich (Abbildung 3b)
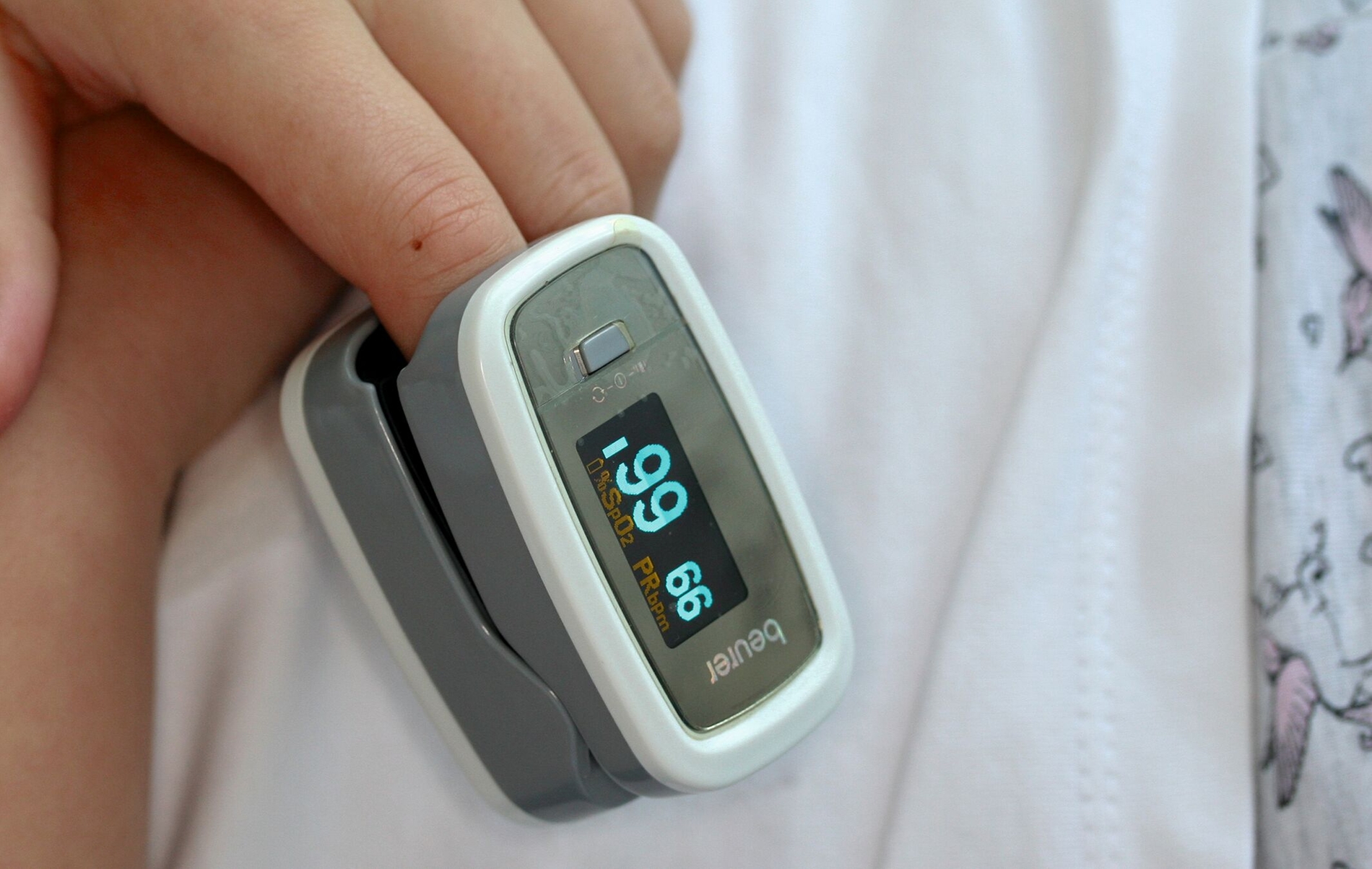
Pulsoximeter (Abbildung 4)
Notfallkoffer
Eine schriftliche Patienten- beziehungsweise Elternaufklärung inklusive Einwilligung mit ausreichenden Informationen unter anderem zu Wirkung, Risiken und Kosten ist zwingend durchzuführen. Die Anwendung von Duftstiften (Abbildung 1c) kann vor allem bei kleinen Kindern die Akzeptanz der Nasenmaske erhöhen.
Eine Dokumentation der Herzfrequenz, der Sauerstoffsättigung im Blut (zum Beispiel mit einem Pulsoximeter), der Länge des Eingriffs, der maximalen Dosierung und der Dauer der Behandlung in der Patientenakte ist empfehlenswert [American Academy of Pediatric Dentistry, 2022; Höhne et al., 2021].

Evidenz in der Zahnmedizin
Lachgassedierung stellt eine einfach durchführbare und zugleich sichere Technik für die Behandlung von ängstlichen Patienten, Patienten mit Würgereiz und mäßig kooperativen Kindern dar. International gilt die Lachgassedierung als erfolgreiche Behandlungsalternative für die Narkose bei der zahnärztlichen Behandlung der Kinder [Galeotti et al., 2016; Hennequin et al., 2012; Collado et al., 2007; Foley, 2005; Bryan, 2002].
In Deutschland wird die Lachgassedierung für Zahnbehandlungen von Anästhesisten und Zahnärzten befürwortet [Höhne et al., 2021]: Seit 2013 existiert die gemeinsame Stellungnahme des wissenschaftlichen Arbeitskreises Kinderanästhesie der Deutschen Gesellschaft für Anästhesiologie und lntensivmedizin e.V. (DGAI) und des Interdisziplinären Arbeitskreises Zahnärztliche Anästhesie von DGAI, Berufsverband Deutscher Anästhesisten e.V. (BDA), Deutscher Gesellschaft für Kinderzahnheilkunde (DGKiZ) und Deutscher Gesellschaft für Zahn-, Mund- und Kieferheilkunde (DGZMK) für den Einsatz von Lachgas zur minimalen Sedierung von Kindern in der Zahnheilkunde [Philippi-Höhne et al., 2013]. Trotzdem sind bislang nach unserer Kenntnis zur Nutzung und zu den Erfolgsraten von Lachgassedierung in der Kinderzahnheilkunde in Deutschland noch keine Daten publiziert worden.
Das Ziel einer von der DGZMK unterstützten und an der Abteilung für Präventive Zahnmedizin und Kinderzahnheilkunde in Greifswald durchgeführten Studie ist daher, die Erfolgsraten der kinderzahnärztlichen Behandlung unter Lachgassedierung und die mögliche Ersetzung einer zahnärztlichen Sanierung unter Vollnarkose durch Lachgassedierung in Kombination mit Verhaltensmanagementtechniken bei Kindern zu untersuchen, die aufgrund des hohen zahnärztlichen Behandlungsbedarfs und der mangelnden Kooperation bei zahnärztlichen Behandlungen in eine spezialisierte Praxis für Kinderzahnheilkunde überwiesen wurden.
Da aktuell eine Zahnbehandlung in Lachgassedierung von Patienten privat getragen werden muss und die Verbreitung der Lachgassedierung in Deutschland noch in den Kinderschuhen steckt, erfolgt wahrscheinlich häufiger eine Behandlung unter Vollnarkose, die im GKV-System erstattet wird. Diese Kinder sind dadurch höheren Risiken ausgesetzt und die Krankenversicherungen tragen vermutlich höhere Kosten als bei einer Sedierung mit Lachgas.
Der Anteil von Kindern, bei denen Narkose für Zahnbehandlungen durchgeführt wurde, wird deutschlandweit als signifikant eingeschätzt, da bereits jedes siebte 3-jährige Kind beziehungsweise jedes zweite 6- bis 7-jährige Kind Milchzahnkaries aufweist und dann im Schnitt vier Zähne betroffen sind. Zudem ist der Sanierungsgrad in den Altersgruppen mit knapp 25 Prozent bei 3-Jährigen und circa 50 Prozent bei 6- bis 7-Jährigen sehr gering. Daher hat jede mögliche Reduktion von Narkosen, aber auch die Erhöhung des Sanierungsgrades durch die Lachgassedierung eine sehr hohe Relevanz [Schmoeckel et al., 2021].
Die Ergebnisse der in der Abteilung für Präventive Zahnmedizin und Kinderzahnheilkunde in Greifswald durchgeführten Studie zeigen, dass die zahnärztliche Behandlung von ängstlichen beziehungsweise prä-kooperativen Kindern in 92,7 Prozent der Lachgassitzungen erfolgreich durchgeführt werden konnte. Mit dem Alter der Kinder und der Erfahrung des Zahnarztes stiegen die Erfolgsquoten [Mourad et al., 2022a]. Etwa 80 Prozent der Kinder mit „Narkoseüberweisung“ könnten ohne Narkose, insbesondere durch die Lachgassedierung behandelt werden [Mourad et al., 2022b]. Dies zeigt das enorme Potenzial der Narkosealternative, das im klinischen Alltag stärker genutzt werden sollte! Lachgassedierungen eignen sich auch zur besseren Versorgung von Kindern mit akuten Schmerzen, die sonst zum Teil eine stationäre Einweisung bedingen, da die Lachgassedierung nicht den hohen organisatorischen Erfordernissen einer Narkosebehandlung unterliegt und tagtäglich in der Zahnarztpraxis angeboten werden kann. Für Deutschland ergibt sich eine beträchtliche Anzahl an Kindern, für die eine Zahnbehandlung in Narkose vermeidbar wäre.
Was den Erfolg der Lachgassedierung beeinflusst
Ziel: Evaluation der Erfolgsraten und möglicher Einflussfaktoren der Lachgassedierung bei zahnärztlichen Behandlungen in einer spezialisierten Kinderzahnarztpraxis
Material und Methoden: Die Patientenakten aller Kinder, die zwischen 2012 und 2017 in einer spezialisierten Klinik für Kinderzahnheilkunde unter Lachgassedierung behandelt wurden, wurden retrospektiv auf Parameter wie Alter des Kindes, Erfahrung der Zahnärzte, Behandlungsverfahren sowie Erfolg oder Misserfolg der Sedierung und der Behandlung analysiert.
Ergebnisse: 480 präkooperative und/oder ängstliche Patienten im Alter von 3 bis 17 Jahren (Mittelwert 6,7 ± 2,7; 54,6 Prozent männlich) wurden in 803 Lachgassitzungen behandelt. Die meisten Kinder waren zwischen sechs und zwölf Jahre alt (n = 271, 56,5 Prozent). Die Gesamterfolgsrate lag bei 92,7 Prozent für alle Lachgassitzungen (95 Prozent CI, bereinigt um Mehrfachsitzungen: 91 bis 94 Prozent). Mit zunehmendem Patientenalter stieg die Erfolgsquote signifikant (P = 0,041). Über die Jahre der Anwendung lässt sich ein deutlicher Lerneffekt, also steigende Erfolgsquoten, abbilden.
Schlussfolgerung: Angesichts der hohen Gesamterfolgsrate von über 90 Prozent kann die Lachgassedierung als eine hocheffektive Behandlungsoption für die Durchführung von Zahnbehandlungen bei präkooperativen und/oder ängstlichen Kindern und Jugendlichen sein. Mit dem Alter der Kinder und der Erfahrung des Zahnarztes stiegen die Erfolgsquoten.
Mourad, MS, Santamaria, RM, Splieth, CH, Schwahn, C, Midani, R, Schmoeckel, J. (2022): Impact of operators' experience and patients' age on the success of nitrous oxide sedation for dental treatment in children. in: Eur J Paediatr Dent, 23, 3, S. 183–88.
Neben der ethischen Verpflichtung, eine risikoarme und sichere Therapie anzubieten, zeichnet sich ab, dass auch aus gesundheitsökonomischen Gründen die Kosten einer Lachgassedierung zur Vermeidung von Narkosebehandlungen vom Kostenträger übernommen werden sollten. Die erhöhte Erkrankungsprävalenz, insbesondere von Karies und Folgeerkrankungen bei Individuen mit niedrigem sozio-ökonomischem Status, resultiert darin, dass unter Umständen die bezahlte Narkose der gegebenenfalls schneller verfügbaren, risikoärmeren, aber privat zu bezahlenden Lachgassedierung vorgezogen wird [Freeman und Carson, 2003]. Dies gilt auch, wenn im Einzelfall – nach Erfahrung der Autoren – die Patienten/Eltern manchmal die Kosten für eine einzelne Lachgassedierung im Nachhinein erstattet bekommen, wenn die Rechnung mit einer Bestätigung eingereicht wird, dass die Behandlung sonst in Narkose hätte durchgeführt werden müssen.
Potenzial der Lachgassedierung in der Kinderzahnheilkunde zur Reduktion zahnärztlicher Vollnarkosen
Ziel: Untersuchung zur möglichen Reduktion einer zahnärztlichen Sanierung unter Vollnarkose durch Lachgassedierung in Kombination mit Verhaltensmanagementtechniken bei Patienten unter zwölf Jahren, die aufgrund des hohen zahnärztlichen Behandlungsbedarfs und der mangelnden Kooperation bei zahnärztlichen Behandlungen in eine spezialisierte Praxis für Kinderzahnheilkunde überwiesen wurden.
Material und Methode: Retrospektive Analyse der digitalen Patientenakten aller Kinder, die zwischen 2012 und 2017 in einer spezialisierten Kinderzahnklinik mit Lachgassedierung behandelt wurden. Die Reduktion des Bedarfs an zahnärztlicher Vollnarkose wurde in Abhängigkeit von der Erfolgsrate der Lachgassedierung auf Patientenebene und in Bezug auf mehrere damit zusammenhängende Faktoren wie Alter, Grund der Überweisung und Behandlungsbedarf gemessen.
Ergebnisse: In 406 zahnärztlichen Behandlungssitzungen wurde Lachgas bei 228 präkooperativen und/oder ängstlichen Patienten im Alter von drei bis zwölf Jahren (Mittelwert 6,4 ± 1,7; 43,4 Prozent weiblich) eingesetzt. In 91,9 Prozent der Lachgas-Sitzungen konnte die geplante zahnärztliche Behandlung erfolgreich durchgeführt werden. Eine vollständige orale Rehabilitation war bei 84 Prozent der Patienten mit Lachgassedierung ohne Narkose möglich. Was das Alter betrifft, so war die Erfolgswahrscheinlichkeit der Narkose-Reduktion zwar bei Vorschulkindern geringer als bei Schulkindern (77,8 Prozent / 87,9 Prozent), aber immer noch erstaunlich hoch.
Schlussfolgerung: Ein hoher Anteil ängstlicher oder präkooperativer Kinder mit hohem zahnärztlichem Behandlungsbedarf kann ohne Vollnarkose behandelt werden, wenn ein umfassendes Konzept der Kariesbehandlung mit dem Einsatz von Lachgassedierung und Verhaltensmanagementtechniken kombiniert wird. Die Lachgassedierung sollte daher als Option für die zahnärztliche Behandlung von semi-kooperativen Kindern mit hohem zahnärztlichem Behandlungsbedarf in Betracht gezogen werden, bevor eine Entscheidung für eine Zahnbehandlung unter Narkose getroffen wird.
Mourad, MS, Splieth, CH, Al Masri, A, Schmoeckel, J. (2022): Potential for nitrous oxide sedation in pedodontics practice to reduce the need for dental general anesthesia. in: Quintessence Int, 53, 7, S. 598–606.
Fazit
Zahnmedizinische Behandlungen bedürfen einer strikten Indikationsstellung des Behandlers und nicht des Patienten oder der Eltern, der Überweiser oder des Anästhesisten, da der Behandler mit seiner Approbation haftet. Vor einer Narkose für eine Zahnbehandlung sollten daher Alternativen wie die Verhaltensformung, Hypnose und auch die Lachgassedierung geprüft werden. Auch die Reduktion der Kariesaktivität und eine Inaktivierung von kariösen Läsionen erleichtern die Therapie. Die genannten Techniken sind häufig so erfolgreich, dass durch ihre adäquate Nutzung die Zahl der Narkosen für Zahnbehandlungen bei Kindern in Deutschland stark reduziert werden kann, ohne eine zahnärztlich geringere Versorgungsqualität in Kauf nehmen zu müssen.
<bibliography>
American Academy of Pediatric Dentistry (2022): Use of Nitrous Oxide for Pediatric Dental Patients. in: The Reference Manual of Pediatric Dentistry. Chicago, Ill., 353-358.
Bryan, R.A.E. (2002): The success of inhalation sedation for comprehensive dental care within the Community Dental Service. in: Int J Paediatr Dent, 12, 6, S. 410–14.
Collado, V., Nicolas, E., Faulks, D., Hennequin, M. (2007): A review of the safety of 50% nitrous oxide/oxygen in conscious sedation. in: Expert Opin Drug Saf, 6, 5, S. 559–71.
Council of European Dentists (2014): Anwendung der inhalativen Lachgassedierung in der Zahnmedizin. in: Stomatologie, 111, 4-5, S. 188–90.
Foley, J. (2005): A prospective study of the use of nitrous oxide inhalation sedation for dental treatment in anxious children. in: Eur J Paediatr Dent, 6, 3, S. 121–28.
Freeman, R., Carson, P. (2003): Relative analgesia and general dental practitioners: attitudes and intentions to provide conscious sedation for paediatric dental extractions. in: Int J Paediatr Dent, 13, 5, S. 320–26.
Galeotti, A., Garret Bernardin, A., D'Antò, V., Ferrazzano, G.F., Gentile, T., Viarani, V., Cassabgi, G., Cantile, T. (2016): Inhalation Conscious Sedation with Nitrous Oxide and Oxygen as Alternative to General Anesthesia in Precooperative, Fearful, and Disabled Pediatric Dental Patients: A Large Survey on 688 Working Sessions. in: Biomed Res Int, 2016.
Hallonsten, A.-L., Jensen B, Raadal, M., Veerkamp, J., Hosey, M., Poulsen S (2003): EAPD Guidelines on Sedation in Paediatric Dentistry.
Hennequin, M., Collado, V., Faulks, D., Koscielny, S., Onody, P., Nicolas, E. (2012): A clinical trial of efficacy and safety of inhalation sedation with a 50% nitrous oxide/oxygen premix (Kalinox™) in general practice. in: Clin Oral Investig, 16, 2, S. 633–42.
Höhne, C., Daubländer, M., Becke, K., Splieth, C.H., Beck, G. (2021): Empfehlung Einsatz von Lachgas zur minimalen Sedierung von Kindern in der Zahnheilkunde, Gemeinsame wissenschaftliche Mitteilung des Wissenschaftlichen Arbeitskreises Kinderanästhesie der DGAI und des Interdisziplinären Arbeitskreises Zahnärztliche Anästhesie von DGAI, BDA, DGKiZ und DGZMK.
Mourad, M.S., Santamaria, R.M., Splieth, C.H., Schwahn, C., Midani, R., Schmoeckel, J. (2022a): Impact of operators' experience and patients' age on the success of nitrous oxide sedation for dental treatment in children. in: Eur J Paediatr Dent, 23, 3, S. 183–88.
Mourad, M.S., Splieth, C.H., Al Masri, A., Schmoeckel, J. (2022b): Potential for nitrous oxide sedation in pedodontics practice to reduce the need for dental general anesthesia. in: Quintessence Int, 53, 7, S. 598–606.
Murthy, A.K., Pramila, M., Ranganath, S. (2014): Prevalence of clinical consequences of untreated dental caries and its relation to dental fear among 12-15-year-old schoolchildren in Bangalore city, India. in: Eur Arch Paediatr Dent, 15, 1, S. 45–49.
Philippi-Höhne, C., Daubländer, M., Becke, K., Reinhold, P., Splieth, C.H., Beck, G. (2013): Gemeinsame Stellungnahme: Einsatz von Lachgas zur minimalen Sedierung von Kindern in der Zahnheilkunde. in: Anästhesiologie & Intensivmedizin, 54, S. 323–26.
Schmoeckel, J., Santamaría, R.M., Basner, R., Schankath, E., Splieth, C.H. (2021): Mundgesundheitstrends im Kindesalter: Ergebnisse aus den epidemiologischen Begleituntersuchungen zur Gruppenprophylaxe in Deutschland. in: Bundesgesundheitsblatt Gesundheitsforschung Gesundheitsschutz, 64, 7, S. 772–81.
Tobias, J.D. (2013): Applications of nitrous oxide for procedural sedation in the pediatric population. in: Pediatr Emerg Care, 29, 2, S. 245–65.
Wang, C.Y., Chiu, C.L., Har, K.O., Chan, C., Rahman, Z.A.A. (2002): A comparative study of sevoflurane sedation with nitrous oxide sedation for dental surgery. in: Int J Oral Maxillofac Surg, 31, 5, S. 506–10.
Zier, J.L., Tarrago, R., Liu, M. (2010): Level of sedation with nitrous oxide for pediatric medical procedures. in: Anesth Analg, 110, 5, S. 1399–405.
</bibliography>