Patientenspezifische biokeramische Implantate zur Augmentation der Le-Fort-I-Zone
Ein 35-jähriger Patient stellte sich mit einem obstruktiven Schlafapnoesyndrom (OSAS) in der Ambulanz der Klinik für Mund-, Kiefer- und Gesichtschirurgie der Charité vor. Bei ihm war 2018 ein schweres OSAS diagnostiziert worden (Apnoe-Hypopnoe-Index [AHI] von 60/h). Er klagte über eine ausgeprägte Tagesschläfrigkeit und Konzentrationsschwierigkeiten, die sich negativ auf sein Berufs- und Privatleben auswirkten. Bei Intoleranz gegenüber einer CPAP-Maske stellte sich der Patient mit dem Wunsch einer definitiven, kausalen Therapie vor.
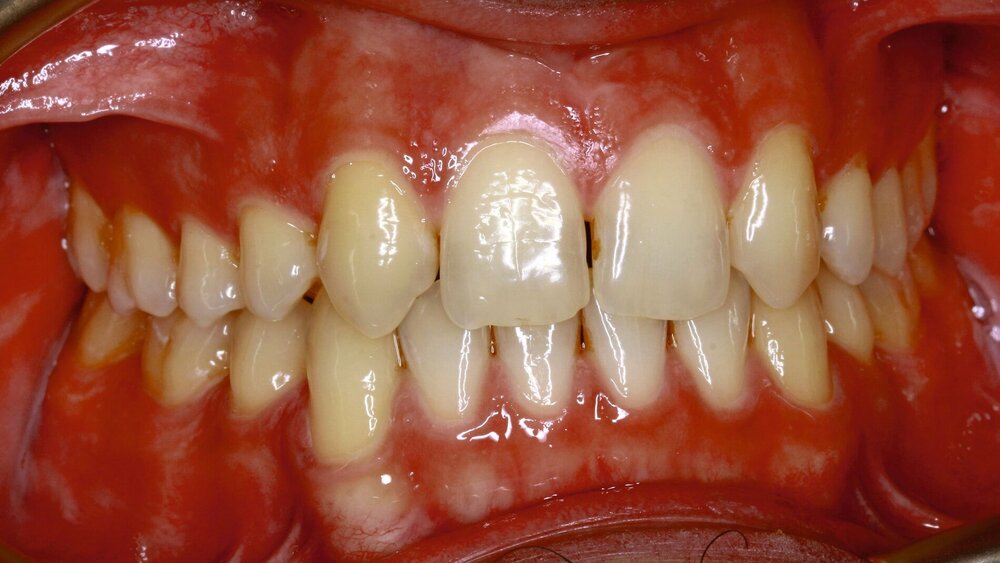
Im klinischen Befund zeigten sich eine Klasse-III-Verzahnung mit retralem Zwangsbiss sowie das Fehlen der Zähne 12, 22, 34 und 44 (Abbildung 1). Es wurde eine vollständig virtuelle Planung der Rotation-Advancement-Operation durchgeführt, bei der Ober- und Unterkiefer um 10 mm nach vorne verlagert wurden, um die pharyngealen Atemwege zu erweitern.
Planung und chirurgisches Vorgehen
Mithilfe einer computergestützten Simulation wurden die dreidimensionale Bewegung sowie die finale skelettale Position der Maxilla und der Mandibula festgelegt – mit dem Ziel einer skelettalen Klasse-I-Okklusion. Für den präzisen operativen Transfer wurden ein CAD/CAM-„Surgical Guide“ und patientenspezifische 3D-gedruckte Titanplatten gefertigt.
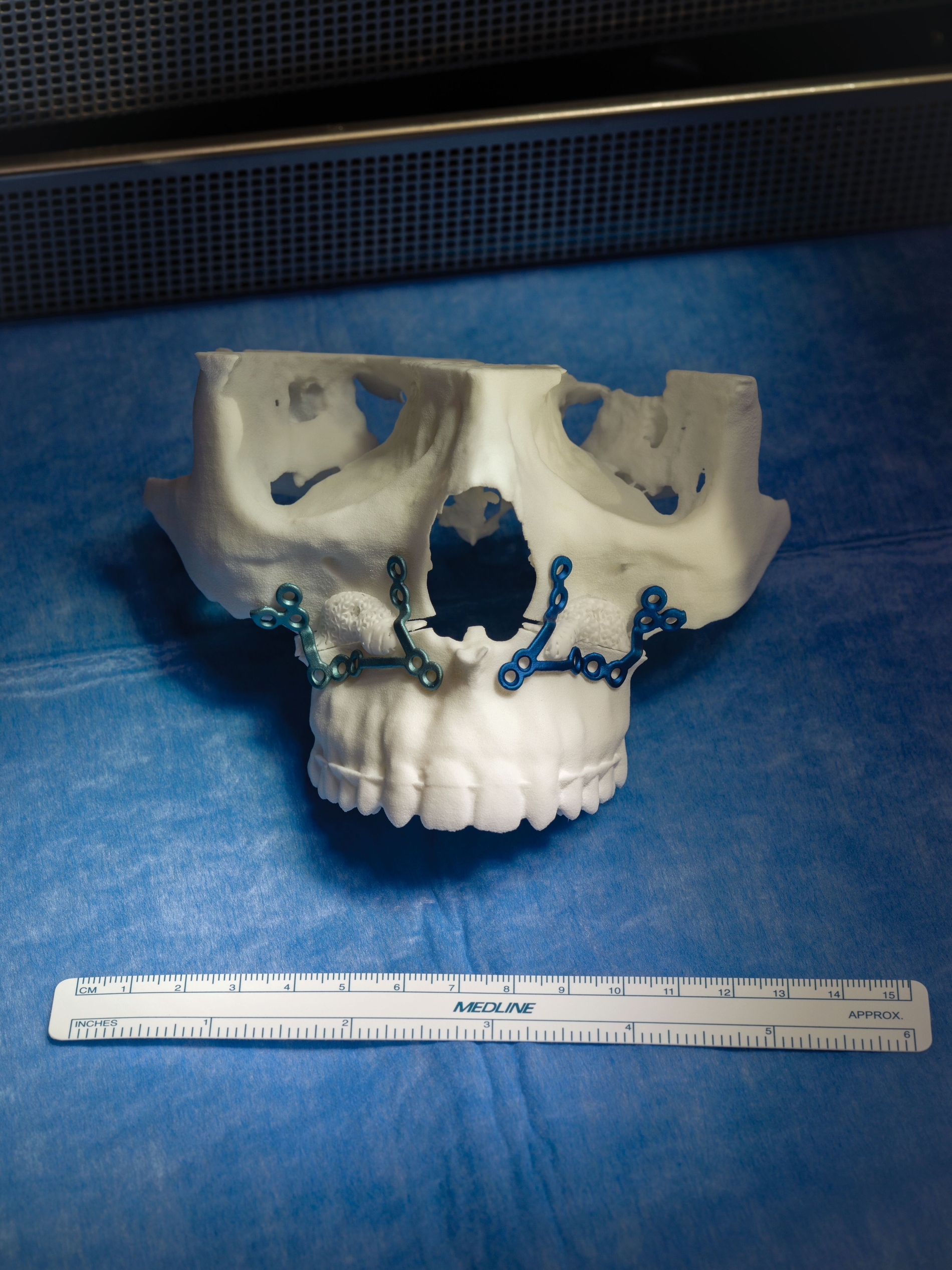
Die biokeramischen Implantate wurde von der Firma Cerhum (Lüttich, Belgien) hergestellt (Abbildungen 2 und 3). Das Unternehmen ist seit 2015 auf die Herstellung von 3D-gedruckten, patientenspezifischen Implantaten aus Hydroxylapatit für verschiedene Einsatzzwecke spezialisiert.
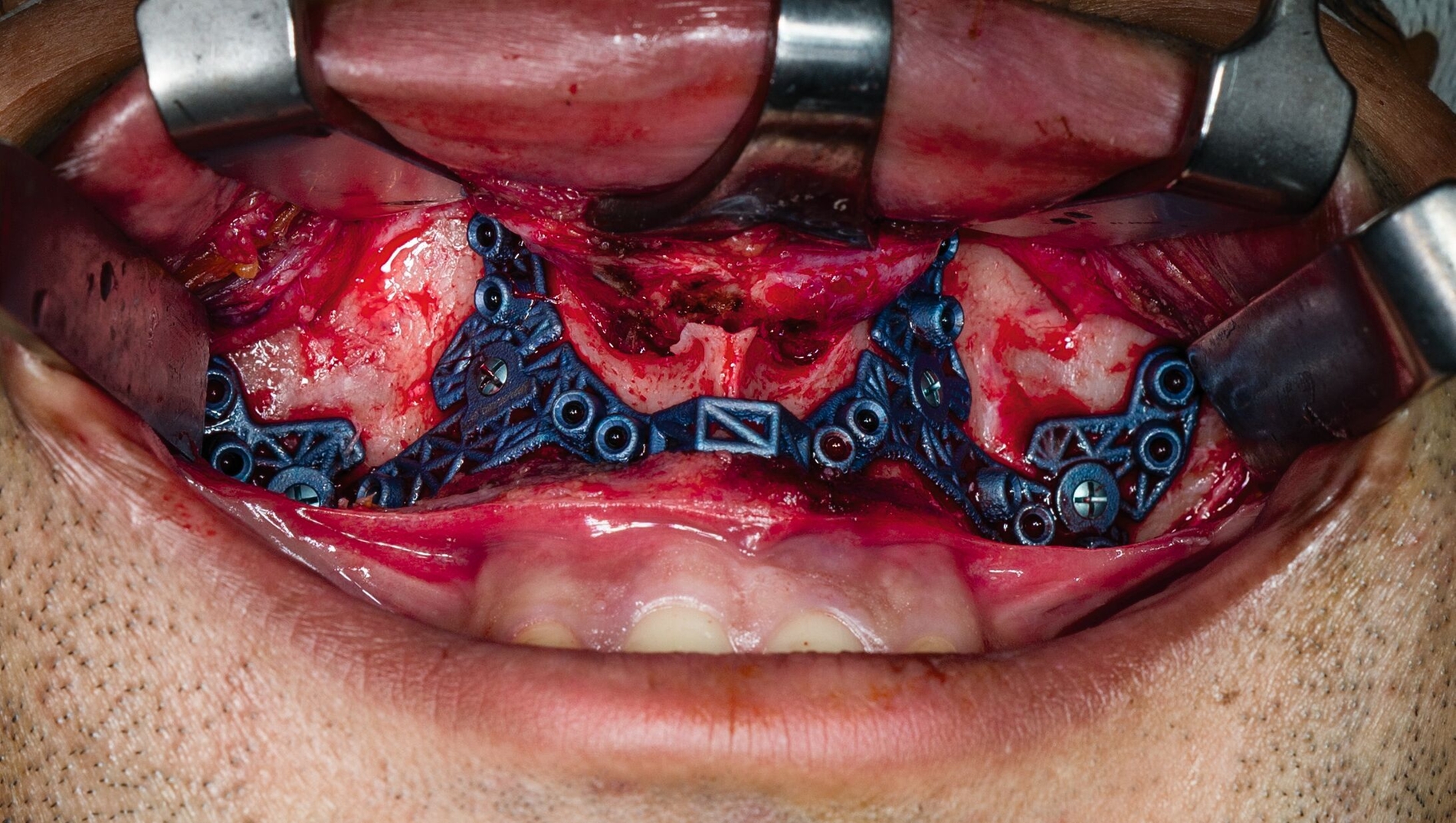
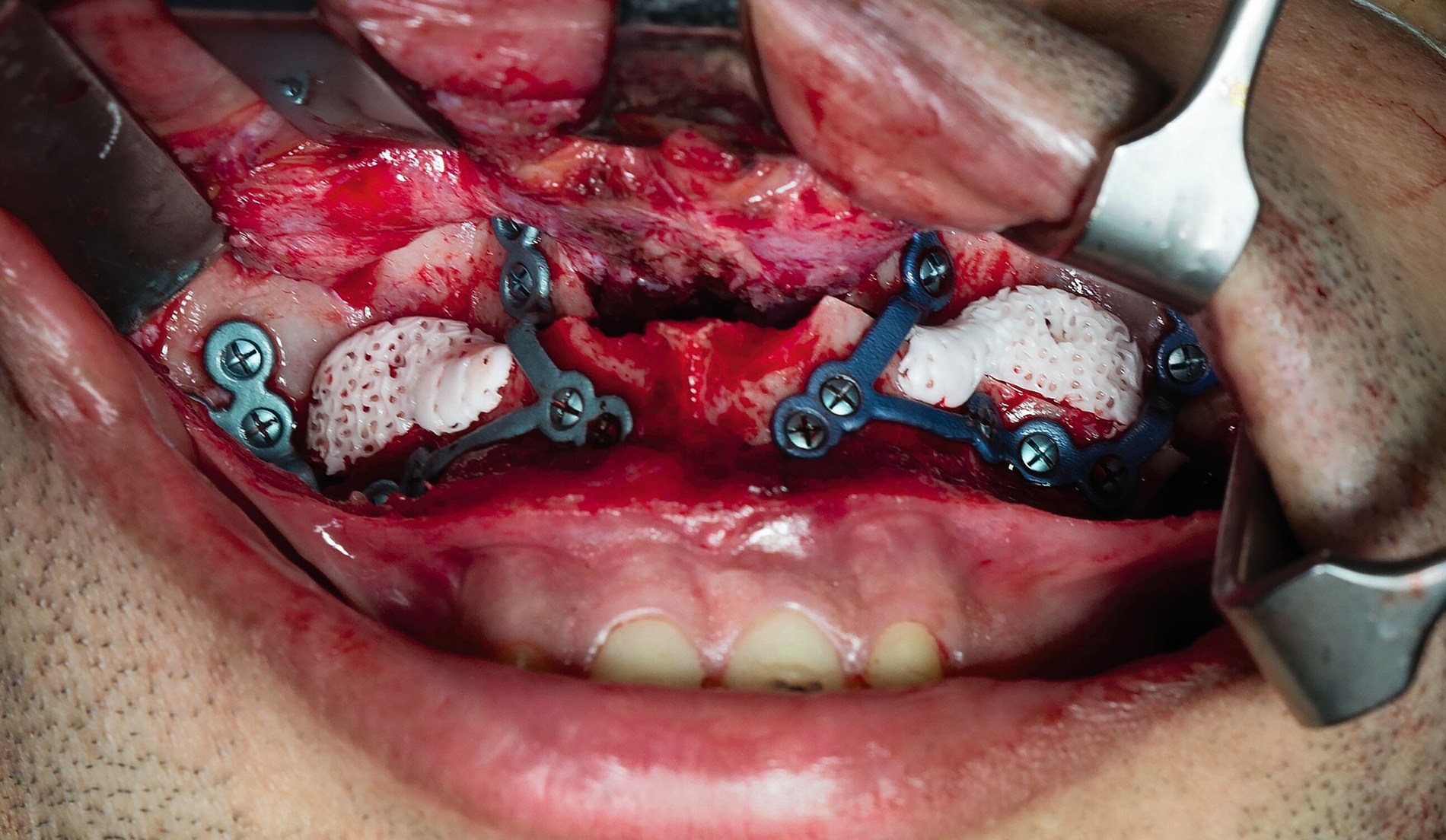
Der Eingriff erfolgte unter Vollnarkose mit nasotrachealer Intubation. Der Surgical Guide (Abbildung 4) wurde mit vier Schrauben fixiert, die Löcher für die patientenspezifische Platte wurden vorgebohrt und die Osteotomielinien in der Le-Fort-I-Ebene mit einer piezoelektrischen Säge markiert. Nach Entfernung des Guides wurden die horizontale Le-Fort-I-Osteotomie vervollständigt, die Maxilla mobilisiert und in der gewünschten Position mittels der patientenspezifischen Osteosyntheseplatte fixiert. Zur Augmentation der Le-Fort-I-Zone wurde das biokeramische Implantat inseriert und mit einer Schraube an der fazialen Kieferhöhlenwand fixiert (Abbildung 5). Im Unterkiefer wurde eine bilaterale sagittale Spaltungsosteotomie (BSSO) nach Hunsuck/Epker durchgeführt. Der zahntragende Anteil der Mandibula wurde mithilfe eines Finalsplints in der geplanten Position eingestellt und mittels konventioneller Miniplatten im Bereich der Linea obliqua fixiert.
Der Patient blieb drei Nächte stationär zur Überwachung und erhielt eine intravenöse Antibiotikaprophylaxe. Nach der Entlassung folgten wöchentliche ambulante Verlaufskontrollen. Der postoperative Verlauf war regelrecht, so dass er nach drei Wochen aus der Nachsorge entlassen wurde.
Diskussion
Die zentrale Frage lautet, ob der Einsatz von Hydroxylapatit-Implantaten auf der Le-Fort-I-Ebene zu einer beschleunigten Ossifikation führen kann. Patientenspezifische Implantate (PSIs) aus Hydroxylapatit (HA) fördern dank ihrer integrierten Mikrostruktur mit vielen miteinander verbundenen Poren die Osteogenese und das fibrovaskuläre Einwachsen [Van Hede et al., 2022]. Die Affinität von Hydroxylapatit zu osteogenetischen und antiresorptiven Molekülen und Wachstumsfaktoren trägt wesentlich zur Osseointegration bei [Ferraz et al., 2023]. Radiologisch nachweisbare Zeichen der Osseointegration erfordern eine Beobachtungszeit von sechs bis zwölf Monaten [Systermans et al., 2024]. Im Vergleich zu Implantaten aus PEEK oder Titan zeigen PSIs aus HA zudem eine höhere Infektionsresistenz. Dies könnte auf das schnelle vaskuläre Einwachsen ins Implantat zurückzuführen sein, das eine verbesserte Immunantwort ermöglicht [Bouakaz et al., 2023].
Ein potenzieller Nachteil von HA-Implantaten ist ihre anfänglich geringe mechanische Festigkeit, die der Druckfestigkeit der Spongiosa entspricht [Doi et al., 2016]. Dadurch sind sie perioperativ anfälliger für Frakturen während der Insertion und der Fixierung [Systermans et al., 2024]. Die mechanische Stabilität nimmt jedoch im Verlauf des Osseointegrationsprozesses zu und erreicht schließlich die Druckfestigkeit des natürlichen Knochens.
Ein weiterer Vorteil von HA-basierten PSIs ist ihre poröse Struktur, die während eines Eingriffs eine einfache Formanpassung ermöglicht, was insbesondere im Vergleich zu Titanimplantaten einen großen Vorteil darstellt [Van Hede et al., 2022]. Zudem führt die Verwendung von PSIs aus HA zu einer signifikanten Verkürzung der Operationszeit im Vergleich zur autologen Knochentransplantation [Hou et al., 2022], und die Entnahmemorbidität entfällt.
Fazit
Patientenspezifische Hydroxylapatit-Implantate (PSIs) sind eine vielversprechende Innovation in der kraniomaxillofazialen Chirurgie. Sie fördern dank ihrer porösen Mikrostruktur die Osteogenese und Osseointegration, zeigen eine hohe Biokompatibilität und vermeiden Entnahmemorbiditäten. Ihre anfänglich geringe Stabilität erfordert jedoch eine vorsichtige Handhabung. Diese ersten Einblicke sollen den Grundstein für weiterführende Studien zur Validierung dieser Technik legen.
Literaturliste
Bouakaz, I.; Drouet, C.; Grossin, D.; Cobraiville, E.; Nolens, G. Hydroxyapatite 3D-Printed Scaffolds with Gyroid-Triply Periodic Minimal Surface (TPMS) Porous Structure: Fabrication and an in Vivo Pilot Study in Sheep. Acta Biomater.( 2023), 170, 580–595. doi.org/10.1016/J.ACTBIO.2023.08.041.
Doi, K.; Kubo, T.; Makihara, Y.; Oue, H.; Morita, K.; Oki, Y.; Kajihara, S.; Tsuga, K. Osseointegration Aspects of Placed Implant in Bone Reconstruction with Newly Developed Block-Type Interconnected Porous Calcium Hydroxyapatite. J. Appl. Oral. Sci. (2016), 24, 325–331. doi.org/10.1590/1678-775720150597.
Ebker T. et al. Comprehensive virtual orthognathic planning concept in surgery-first patients. British Journal of Oral and Maxillofacial Surgery (2022), doi.org/10.1016/j.bjoms.2022.04.008.
Ferraz, M.P. Bone Grafts in Dental Medicine: An Overview of Autografts, Allografts and Synthetic Materials. Materials (2023), 16, 4117. doi.org/10.3390/MA16114117.
Hou, X.; Zhang, L.; Zhou, Z.; Luo, X.; Wang, T.; Zhao, X.; Lu, B.; Chen, F.; Zheng, L. Calcium Phosphate-Based Biomaterials for Bone Repair. J. Funct. Biomater.( 2022), 13, 187. doi.org/10.3390/JFB13040187.
Kanno, T.; Sukegawa, S.; Karino, M.; Furuki, Y. Navigation-Assisted Orbital Trauma Reconstruction Using a Bioactive Osteocon-ductive/Bioresorbable u-HA/PLLA System. J. Maxillofac. Oral. Surg. (2019), 18, 329–338. doi.org/10.1007/S12663-019-01207-Y.
Systermans, S.; Cobraiville, E.; Camby, S.; Meyer, C.; Louvrier, A.; Lie, S.A.; Schouman, T.; Siciliano, S.; Beckers, O.; Poulet, V.; et al. An Innovative 3D Hydroxyapatite Patient-Specific Implant for Maxillofacial Bone Reconstruction: A Case Series of 13 Patients. J. Cranio‐Maxillofac. Surg. (2024), 52, 420–431. doi.org/10.1016/J.JCMS.2024.02.026.
Van Hede, D.; Liang, B.; Anania, S.; Barzegari, M.; Verlée, B.; Nolens, G.; Pirson, J.; Geris, L.; Lambert, F. 3D-Printed Synthetic Hydroxyapatite Scaffold With In Silico Optimized Macrostructure Enhances Bone Formation In Vivo. Adv. Funct. Mater. (2022), 32, 2105002. doi.org/10.1002/ADFM.202105002.