Therapie der LKGF – Zahnärztliche Aspekte im Fokus
LKGF zählen weltweit zu den häufigsten angeborenen Fehlbildungen. In Deutschland scheint die Frequenz mit näherungsweise 1:500 betroffenen Neugeborenen besonders hoch zu sein [Mossey/Modell, 2012].
Die Entwicklung von Gesicht und Mundhöhle stellt einen höchst komplexen Prozess in der frühen Embryonalentwicklung dar. Die sensible Phase für die Entwicklung von Lippe und Alveolarkamm ist zeitlich etwa in der sechsten Woche der menschlichen Embryogenese verortet, die von Hart- und Weichgaumen etwas später in der achten bis zehnten Woche post conceptionem [Hammond/Dixon, 2022].
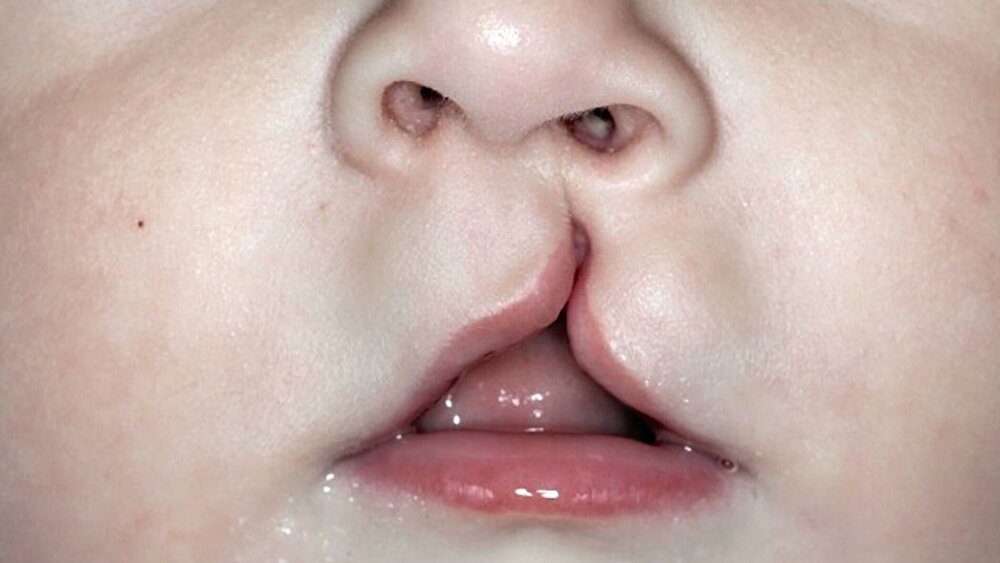
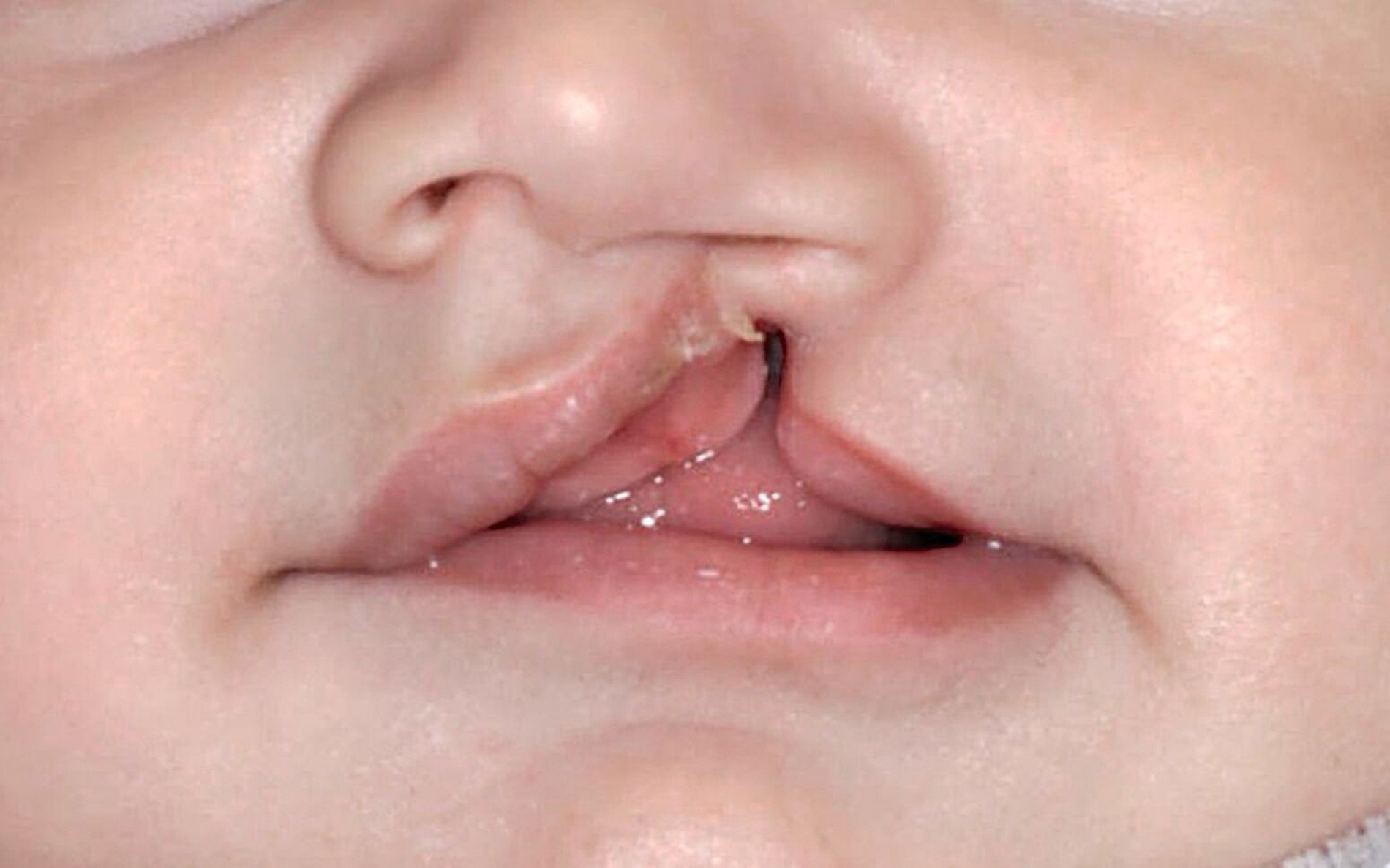
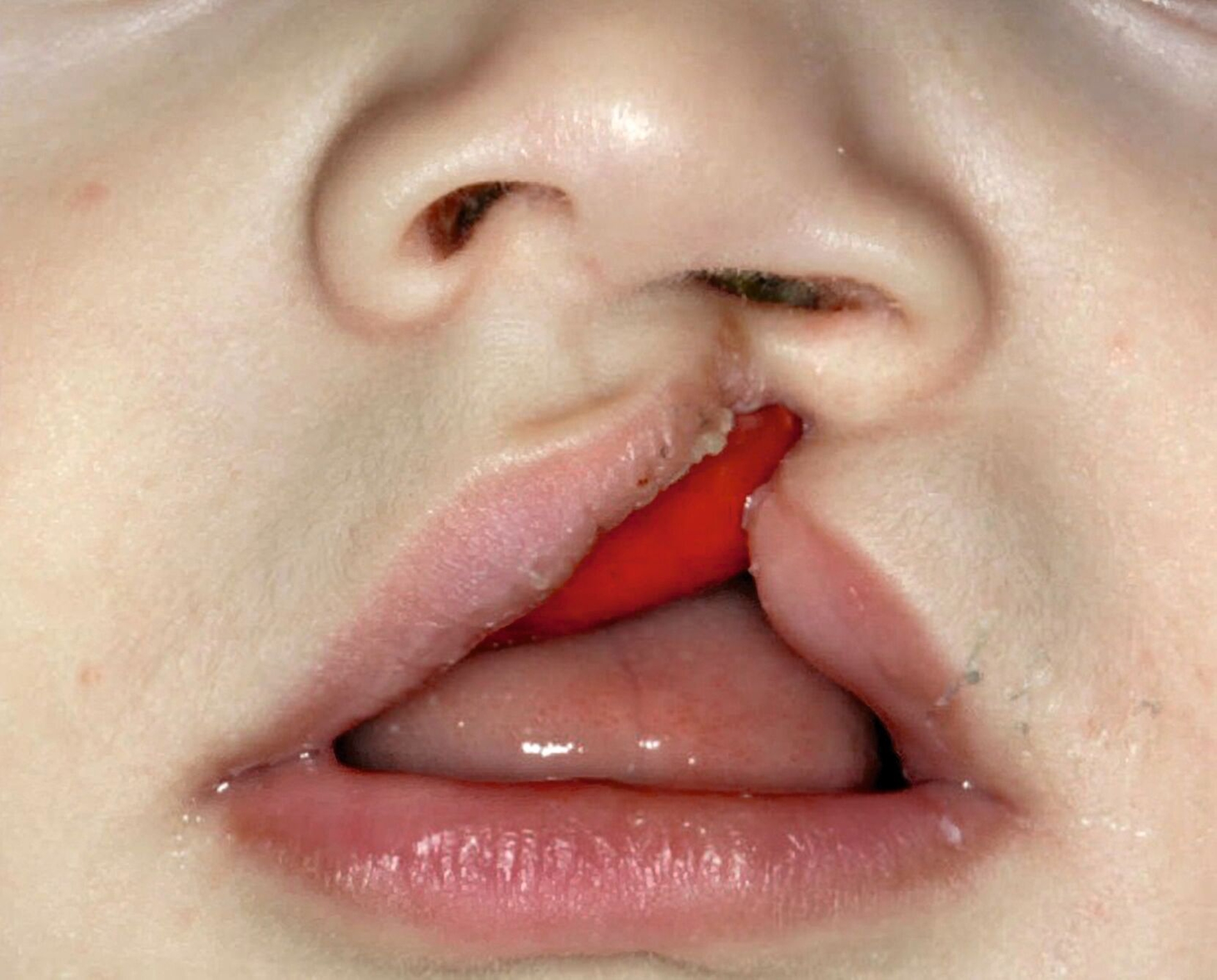
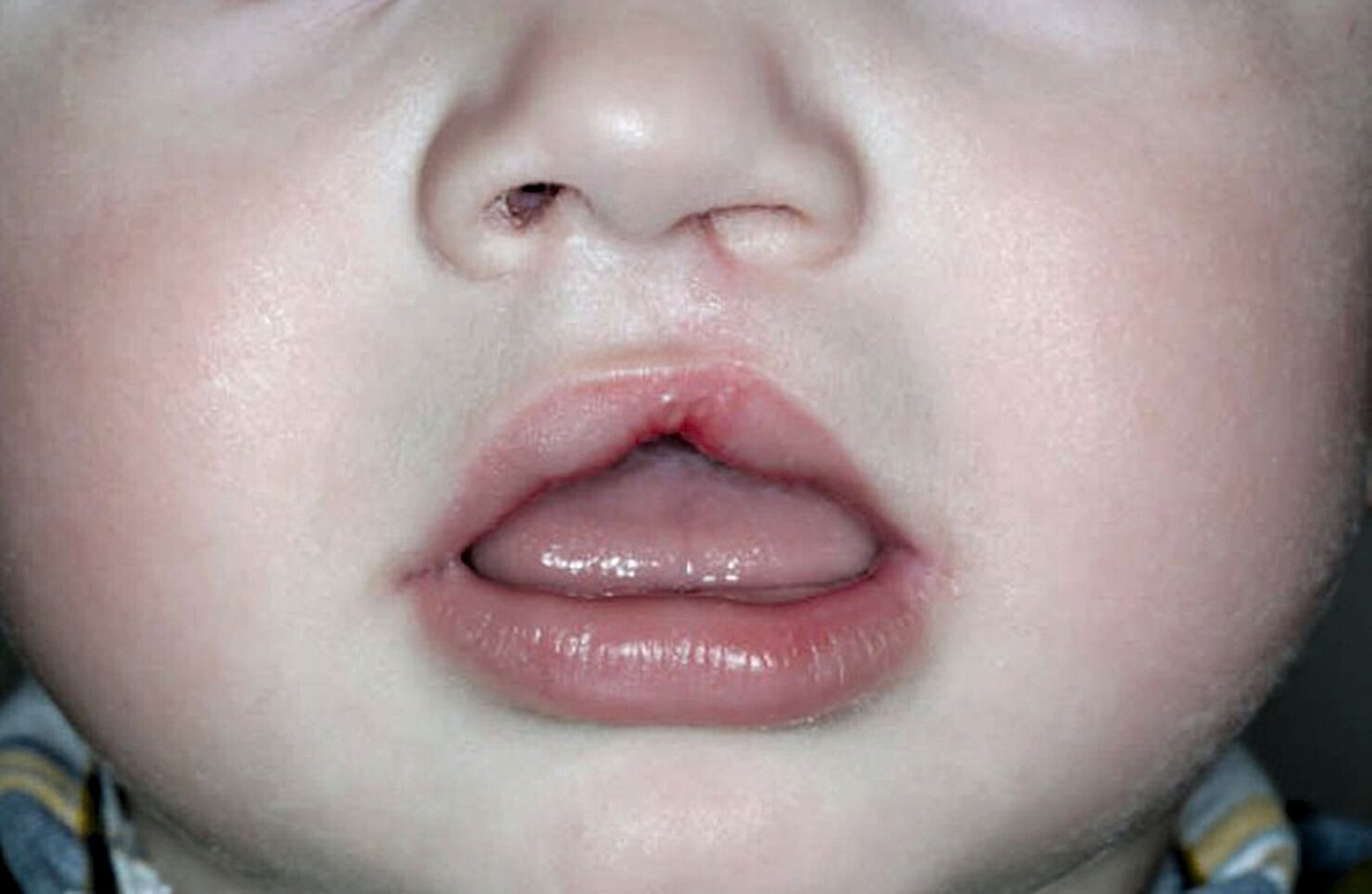
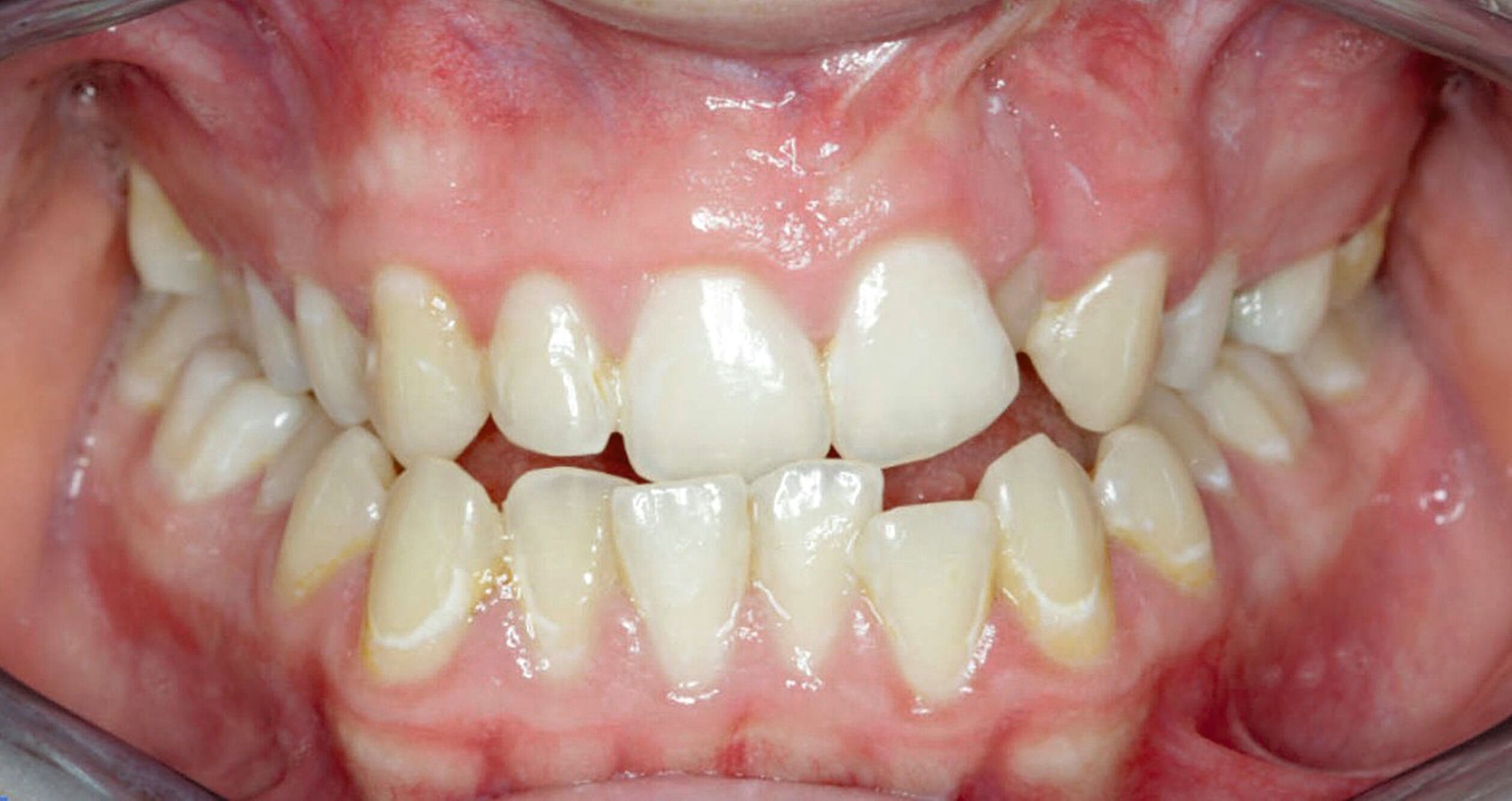
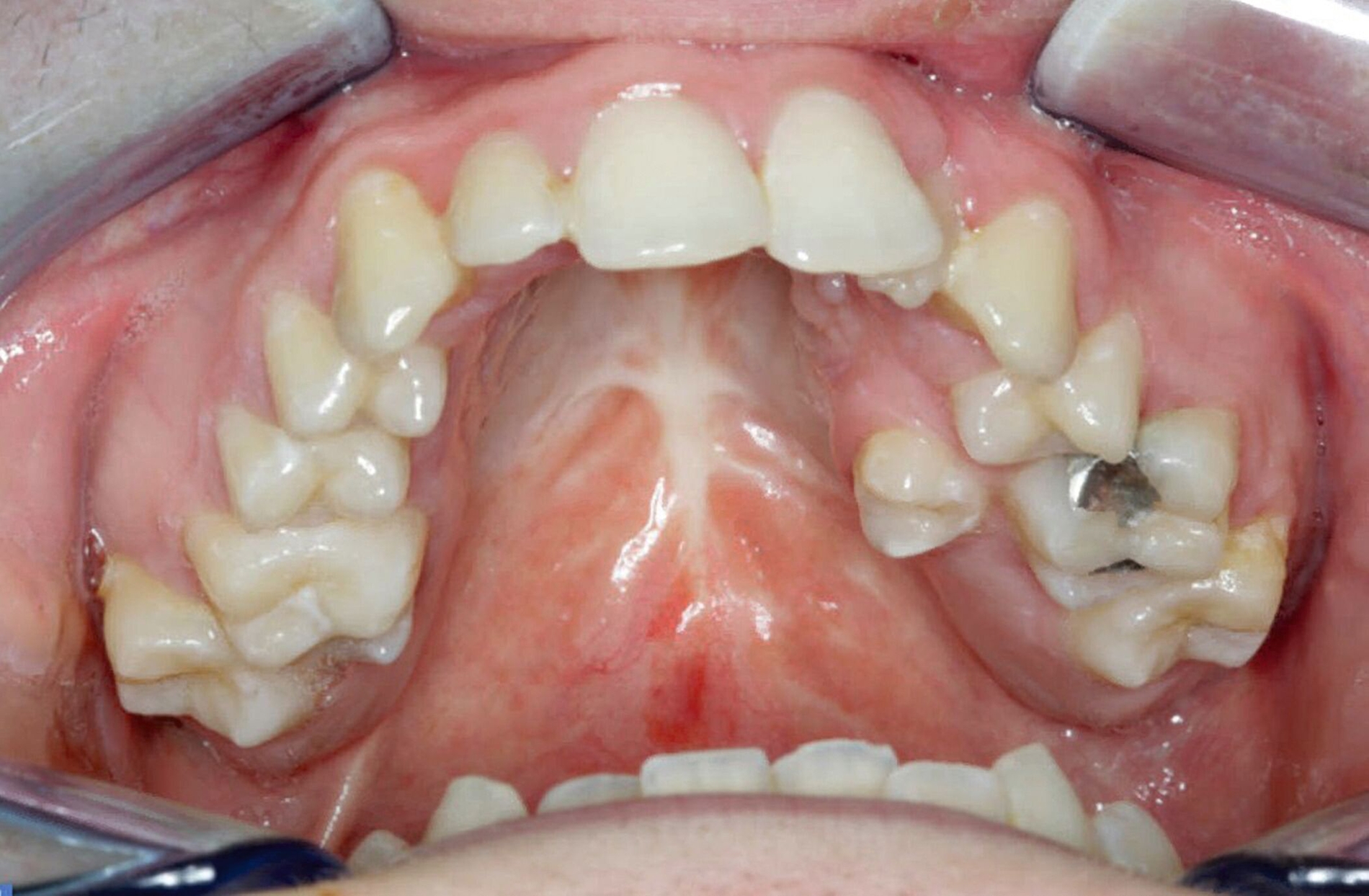
Störungen der involvierten Gen-Interaktionen sowie Umwelteinflüsse können in dieser Phase eine physiologische Fusion der Nasen- und Oberkieferwülste verhindern und zu uni- oder bilateralen Fehlbildungen unterschiedlicher Ausprägung führen. Dabei können nur einzelne anatomische Untereinheiten betroffen sein (siehe Abbildung 1, isolierte Lippen- oder Lippen-Kieferfehlbildungen, isolierte Hart-/Weichgaumenfehlbildungen). Der Ausprägungsgrad variiert von Mikroformen (zum Beispiel Lippenkerbe, Uvula bifida) bis hin zur vollständigen Unterbrechung aller anatomischen Strukturen mit Fehlbildung der äußeren und/oder inneren Nase.
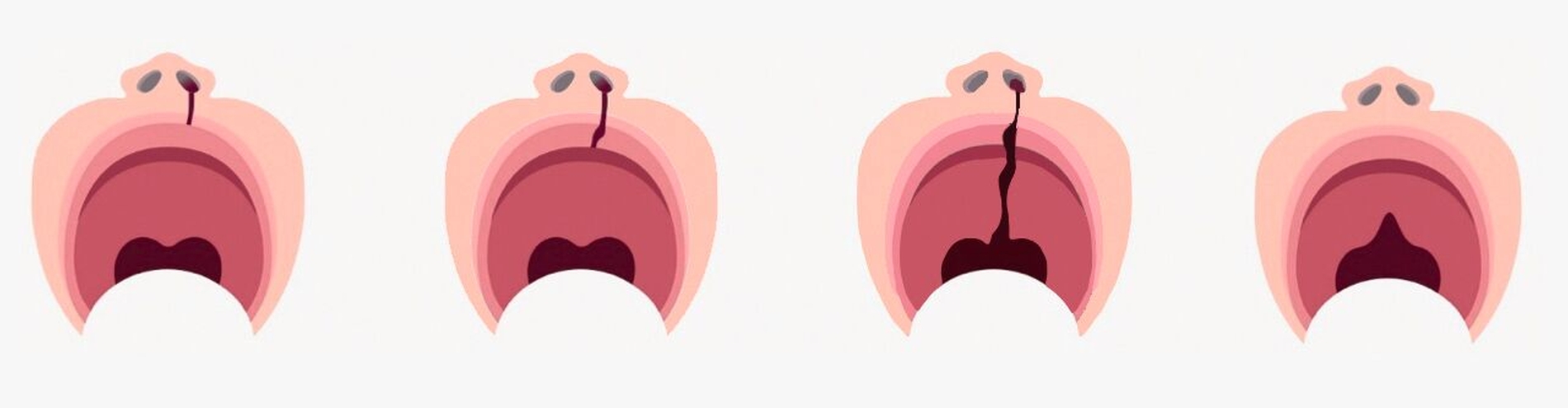
Die individuelle Krankheitslast wird primär von der Ausprägung der Fehlbildung, Komorbiditäten und Komplikationen beeinflusst. Eine langfristige, multidisziplinäre, auf den Patienten abgestimmte Therapie ist jedoch die Voraussetzung für eine vollständige Rehabilitation, adäquate Lebensqualität und gesellschaftliche Integration der Betroffenen. Eine gute zahnärztliche Versorgung ist dabei lebenslang von besonderer Bedeutung.
Bei Fehlbildungsformen, die den Hartgaumen involvieren, wird zumeist bereits in den ersten Lebenstagen eine sogenannte Mund-Nasen-Trennplatte durch die Kieferorthopädie eingegliedert. Durch das gestörte Wachstumsmuster der Maxilla ist bei den meisten Patienten eine kieferorthopädische Mitbetreuung über den gesamten Zeitraum der Gebissentwicklung hinweg sinnvoll. Mit dem Durchbruch des Milchgebisses sollten zudem engmaschige kinderzahnärztliche Kontrollen eingeleitet werden. Häufig auftretende Nichtanlagen und Zahnmissbildungen stellen auch bei jugendlichen und erwachsenen Patienten eine besondere Herausforderung in Bezug auf die prothetische Versorgung dar.
Ziel der neuen Leitlinie ist, durch Standardisierung der Behandlungskonzepte auf Basis des aktuellen Forschungsstandes Langzeit-Outcome und Lebensqualität von Patienten mit LKGF zu verbessern. Speziell auf die zahnärztlichen Aspekte der Therapie soll im Folgenden näher eingegangen werden.
Methodik der S3-Leitlinie
Unter Federführung der DGMKG und der DGZMK erstellten und bearbeiteten Mandatsträger von 40 Fachgesellschaften, Organisationen und Patientenorganisationen 42 Schlüsselfragen. Die standardisierte und dokumentierte Bewertung der Evidenz diente als Basis für die Formulierung von Empfehlungen und Statements sowie für die Konsensfindung. Zusätzlich gehen klinische, versorgungspraktische und ethische Werturteile der Leitliniengruppe in die Formulierung ein.
Prinzipiell wird unterschieden zwischen evidenzbasierten Empfehlungen (EbE), bei denen die vorliegende Evidenz den Empfehlungsgrad leitet, und konsensbasierten Empfehlungen (Expertenkonsens, EK). Die Methodik folgt dem Regelwerk der Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften [AWMF, 2023]. Über alle Themenbereiche hinweg fällt eine insgesamt niedrige Qualität der wissenschaftlichen Evidenz aus Studien auf. Dies schließt auch die zahnmedizinischen Teilbereiche mit ein.
Insgesamt wurden 74 Empfehlungen und 20 Statements verabschiedet (66 evidenz- und 28 konsensbasiert), die die Pränataldiagnostik und humangenetische Diagnostik, Ernährung, Kieferorthopädische Therapie und Kieferspaltosteoplastik, Operative Rekonstruktion, HNO und Pädaudiologie, Sprachtherapie/Logopädie, Anästhesiologische Aspekte, Zahnärztliche Therapie sowie Psychosoziale Unterstützung/Organisation der Therapie abdecken.
Chirurgische Rekonstruktion und KFO-Therapie
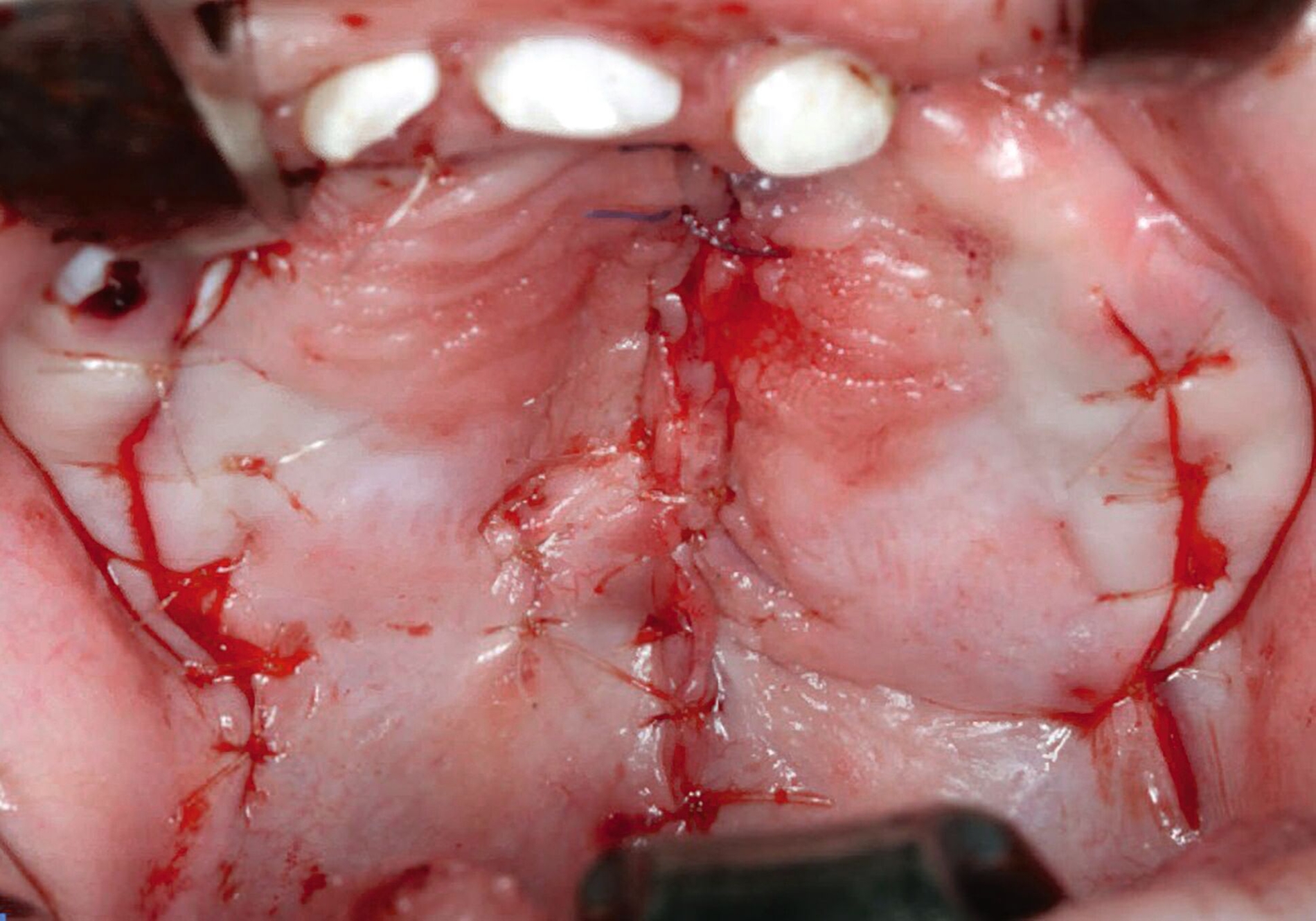
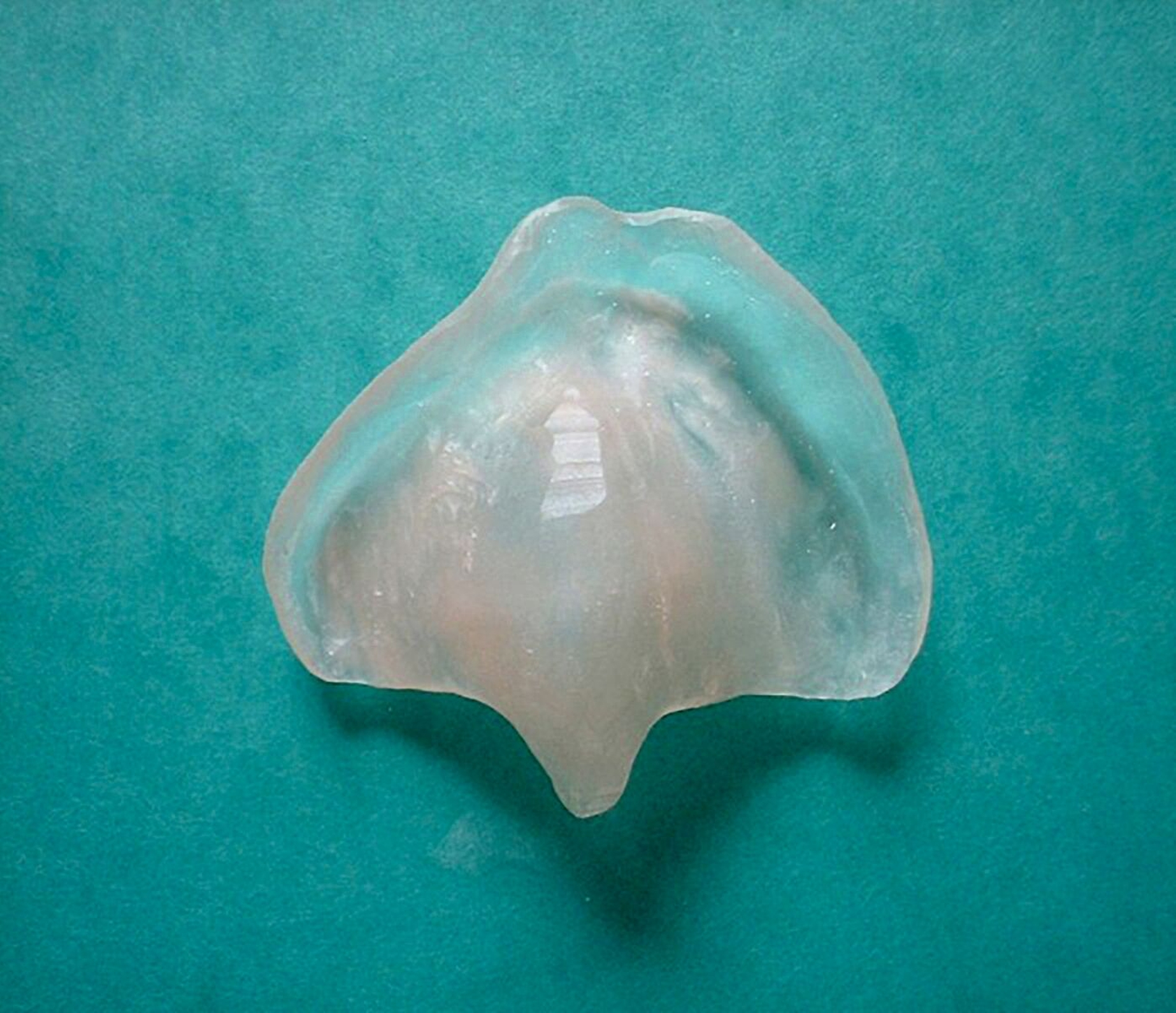
Chirurgische und kieferorthopädische Therapie sollten zur bestmöglichen Rehabilitation der orofazialen Funktionalität und Ästhetik in allen Entwicklungsphasen eng aufeinander abgestimmt sein. Die chirurgische Rekonstruktion von Oberlippe, Naseneingang, Nasenboden, Hart- und Weichgaumen erfolgt möglichst im ersten Lebensjahr (Abbildung 2). Die vorhergehende kieferorthopädische Therapie mittels Mund-Nasen-Trennplatte (Abbildungen 2, 3) zielt darauf ab, die Zungenruhelage zu korrigieren und somit bei durchgehenden Fehlbildungsformen das weitere Auseinanderdrängen der Segmente zu verhindern.
Eine Annäherung der Kiefersegmente erleichtert durch die verminderte Spaltbreite und eine geringere Mittellinienabweichung eine anatomisch möglichst korrekte, spannungsfreie chirurgische Rekonstruktion. Die prächirurgische passive kieferorthopädische Therapie (im Sinne einer Mund-Nasen-Trennplatte) wird daher in der Leitlinie konsensbasiert empfohlen (EK ↑).
Bei Beteiligung der Lippe wird teils die Ergänzung der Trennplatte durch zusätzliche Elemente zur Ausformung der Nase (Naso-Alveoläres-Molding, NAM-Therapie) propagiert. Die Effektivität von Nasoalveolar Molding (NAM)-Apparaturen konnte in zwei umfangreichen systematischen Übersichtsarbeiten 2011 und 2012 [Papadopoulos et al., 2012; Uzel/Alparslan, 2011] sowie auch in einer Auswertung des Instituts für Qualität und Wirtschaftlichkeit im Gesundheitswesen (IQWiG) [Hagen et al., 2019] nicht nachgewiesen werden.
Eine verbesserte nasolabiale Form und Ästhetik durch NAM-Therapie bis zum vierten Lebensjahr wird durch aktuelle Studienergebnisse nahegelegt [Padovano et al., 2022], die Anwendung dieser Therapieform kann nach Abwägung individueller Patientenfaktoren erfolgen (EbE ↑).
Die vorhandene Literatur zu verschiedenen Operationstechniken, -zeitpunkten und der Reihenfolge der Eingriffe ist begrenzt, eindeutige Schlussfolgerungen sind in den meisten Fällen nicht möglich. Auf Basis der vorhandenen Evidenz kann dementsprechend keine eindeutige Empfehlung für oder gegen einzelne operative Techniken zur Rekonstruktion von Oberlippe, Nase und Gaumen gegeben werden.
Grundsätzlich wird eine Rekonstruktion frühestens ab dem dritten Lebensmonat empfohlen (EbE ↔), diese kann auch bei durchgehenden Fehlbildungsformen ein- oder mehrzeitig erfolgen (EbE ↔). Zum Zeitpunkt der Rekonstruktion von Oberlippe und Nase sollte eine primäre Septorhinoplastik erfolgen [Zelko et al., 2023; Di Chiaro et al., 2022]. Im Bereich des Hartgaumens wird eine zweischichtige Rekonstruktion unter Bildung eines oralen und eines nasalen Blattes empfohlen (EK ↑). Unabhängig von der angewendeten Technik zur Gaumenrekonstruktion muss die besondere Bedeutung der sorgfältigen Rekonstruktion der velaren Muskelschlinge betont werden.
Die regelmäßige Kontrolle des Oberkieferwachstums durch Kieferorthopädie und Mund-Kiefer-Gesichtschirurgie sollte während der weiteren Entwicklung Standard sein. Bei ausgeprägter maxillärer Wachstumshemmung des Patienten wird bereits in der ersten Dentition eine Frühbehandlung eingeleitet. Zumeist beginnt die weitere kieferorthopädische Therapie jedoch in der frühen zweiten Wechselgebissperiode und begleitet besonders die perioperative Phase der sekundären Kieferspaltosteoplastik.
Laut Leitlinie sollte bei Patienten mit LKGF, transversaler Enge und maxillärer Retrognathie bevorzugt eine Therapie nach Alternate Rapid Maxillary Expansion and Constriction (Alt-RAMEC)-Protokoll mit maxillärer Protraktion [Liou/Tsai, 2005] eingesetzt werden (EbE ↑). Die Protraktion mittels Gesichtsmaske oder Oberkieferprotraktionsfedern kann dabei simultan zur oder erst nach Abschluss der forcierten transversalen Nachentwicklung der Maxilla mittels zahngetragener oder knöchern fixierter Expander erfolgen.
Hier zeigen sich signifikant größere vorteilhafte Veränderungen von skelettalen, dentoalveolären und weichgewebigen Parametern im Vergleich zur konventionellen Behandlung mit Expansion und anschließender Protraktion [Sami et al., 2023] und der Therapie ausschließlich mit Gesichtsmaske [Dogan/Seckin, 2020].
Bei Patienten mit LKGF mit Beteiligung des Kieferkamms sollte die kieferorthopädische Ausformung und transversale Weitung vor einer geplanten Kieferspaltosteoplastik des Oberkiefers erfolgen (EbE ↑). Diese sollte mindestens sechs Monate vor der geplanten Kieferspaltosteoplastik begonnen werden (EK ↑) und kann mittels festsitzender oder herausnehmbarer Apparaturen vorgenommen werden (EK ↑).
Die Kieferspaltosteoplastik sollte dann erfolgen, wenn absehbar ist, dass der eingebrachte Knochen in den folgenden sechs bis 18 Monaten dental belastet wird (EK ↑). Normalerweise ist das der Fall, wenn spaltrandnahe permanente Zähne durchbrechen oder kieferorthopädisch in den Spaltbereich bewegt werden sollen. Die Transplantation von autologem Knochen vom Beckenkamm in den Kieferspaltbereich muss im Vergleich zu alternativen Knochenersatzmaterialien weiterhin als Goldstandard betrachtet werden und sollte bis zum Vorliegen aussagekräftiger Ergebnisse von Studien hoher methodischer Qualität bevorzugt eingesetzt werden (EK ↑).
Im Regelfall erstreckt sich die kieferorthopädische Therapie über das Wechselgebiss hinaus bis in die permanente Dentition. Bei ausgeprägten Dysgnathien wird nach Wachstumsabschluss gegebenenfalls eine kombinierte kieferorthopädisch-kieferchirurgische Therapie erforderlich.
Versorgung durch die Kinderzahnheilkunde
Negative Auswirkungen einer LKGF auf die mundgesundheitsbezogene Lebensqualität von Kindern und Erwachsenen wurden wiederholt belegt [Queiroz Herkrath et al., 2015]. Die Prävalenz von Nichtanlagen, Mikro- und Makrodontien, Doppelanlagen und Schmelzhypoplasien ist in dieser Patientengruppe deutlich erhöht [Azevedo et al., 2025; Marzouk et al., 2021]. Zudem scheint aber auch die Kariesprävalenz sowohl im Milch- als auch im bleibenden Gebiss signifikant höher als in Kontrollgruppen ohne orale Fehlbildung [Antonarakis et al., 2013].
Verschiedene kausale Faktoren könnten hierbei eine Rolle spielen. Einerseits erschweren die reduzierte Flexibilität des operierten Mundvorhofs und vermehrte Engstände (durch überzählige Zähne und ein geringeres Platzangebot bei einer hypoplastischen Maxilla) womöglich die Mundhygiene. Andererseits könnten impaktierte Nahrungsreste in palatinalen Nischen oder Restlöchern als Substrat kariogener Bakterien das Kariesrisiko erhöhen [Cheng et al., 2007]. Zähne mit Schmelzhypoplasien sind zudem per se kariesanfälliger.
Ein weiterer möglicher Einflussfaktor sind kieferorthopädische Apparaturen. Die frühzeitige Eingliederung von Mund-Nasen-Trennplatten aus Acryl könnte die frühe Kolonisierung der Mundhöhle mit Streptococcus mutans und Laktobazillen bedingen [van Loveren et al., 1998] und so eine erhöhte Kariesprävalenz bereits im Milchgebiss verursachen [Bokhout et al., 1996a; Bokhout et al., 1996b]. Im Wechsel- und permanenten Gebiss ist die meist komplexere und langwierigere kieferorthopädische Therapie ein zusätzlicher Risikofaktor.
Eine engmaschige zahnärztliche Betreuung und spezifische Mundhygieneinstruktionen sind daher essenziell. Der Zahnerhalt ist entscheidend für die Oberkieferentwicklung, weshalb die Vorsorge mit Durchbruch des Milchgebisses sorgfältig durchgeführt werden soll. Im Kindesalter hält die Leitliniengruppe im Regelfall dennoch über die reguläre halbjährliche Untersuchung hinausgehende zahnärztliche Kontrollen nicht für erforderlich. Ziel ist es, durch regelmäßige interdisziplinäre Kontrollen, unter anderem durch Mund-Kiefer-Gesichtschirurgen, Zahnärzte und Fachzahnärzte für Kieferorthopädie, die Mund- und Zahngesundheit betreffende Probleme frühzeitig zu identifizieren.
Therapie bei Nichtanlagen
Lückenöffnung versus Lückenschluss
Besonders häufig sind die lateralen Inzisivi im Spaltbereich nicht angelegt. Bewährte Therapiemöglichkeiten sind einerseits der kieferorthopädische Lückenschluss, andererseits die Lückenöffnung mit anschließender konventioneller oder implantatprothetischer Versorgung. Beide Varianten können zu ästhetisch ansprechenden und funktionell hochwertigen Ergebnissen führen [Alqahtani, 2021].
Bei Vorliegen einer LKGF sind jedoch zusätzlich einige Besonderheiten in Betracht zu ziehen. Vorteil des kieferorthopädischen Lückenschlusses ist die Langlebigkeit des therapeutischen Ergebnisses und der Abschluss der Behandlung im frühen Jugendalter bei einer Patientengruppe, die in vielen Bereichen einen hohen therapeutischen Bedarf zeigt. Außerdem wird durch die frühe Mesialbewegung des Eckzahns in den unbezahnten Bereich eine normale gingivale und alveoläre Konfiguration erzeugt und der Knochen im Spaltbereich nach Kieferspaltosteoplastik erhalten.
Andererseits wurde die Mesialisierung des Eckzahns als unabhängiger Prädiktor für einen SNA-Winkel kleiner 78° sowie für die Indikation zur Umstellungsosteomie nach Wachstumsabschluss identifiziert [Lee et al., 2014]. Lückenschluss und Lückenöffnung sind somit valide Alternativen; die individuelle Anatomie, die Ausprägung der maxillären Retrognathie, der Zahnstatus des Patienten sowie der Patientenwunsch sollten laut Leitlinie in die Entscheidung mit einfließen (EbE ↔/↑).
Prothetische Versorgung
Auch nach Abschluss der chirurgischen und kieferorthopädischen Therapie besteht bei Patienten mit LKGF häufig eine komplexe Ausgangssituation für eine prothetische Versorgung im rekonstruierten Spaltbereich.
Eine Lücke im Spaltbereich durch Nichtanlagen oder Zahnverlust sollte bei erwachsenen Patienten mit LKGF mittels festsitzender prothetischer Versorgung geschlossen werden (EbE ↑). Implantatprothetische Versorgungen im rekonstruierten Kieferspaltbereich haben eine gute Survivalrate (93 Prozent nach einer durchschnittlichen Nachbeobachtungszeit von 60,5 Monaten) und erzielen eine hohe Patientenzufriedenheit [Sales et al., 2019]. Die Implantation sollte vier bis sechs Monate nach einer eventuellen Knochentransplantation erfolgen (EbE ↑).
Ist bei erwachsenen Patienten mit LKGF eine implantatprothetische Versorgung nicht gewünscht oder möglich, sollten bevorzugt minimalinvasive einflügelige Adhäsivbrücken zum Lückenschluss verwendet werden (EK ↑). Einflügelige Adhäsivbrücken haben dabei im Vergleich zu zweiflügeligen Adhäsivbrücken eine signifikant höhere Überlebensrate und können schon im frühen Wechselgebiss verwendet werden, da hierbei die permanenten Zähne nicht oder nur minimal abgeschliffen werden müssen und aufgrund einer fehlenden Verblockung auch keine Wachstumshemmung verursacht wird. Sie zeigen zum Ersatz von nichtangelegten Schneidezähnen mit 98,5 Prozent eine sehr gute 10-Jahres-Überlebensrate in einem Kollektiv ohne LKGF [Kern et al., 2017].
Die herausnehmbare prothetische Versorgung scheint hingegen zu einer signifikant geringeren mundgesundheitsbezogenen Lebensqualität zu führen [Papi et al., 2015]. Sie kann als Interimslösung vor Abschluss des Wachstums oder der chirurgischen Behandlung eingesetzt werden. Weitere Indikationen können sich bei ausgeprägten Weichgewebedefiziten, multiplen oronasalen Fisteln oder ausdrücklichem Patientenwunsch ergeben (EbE ↔).
Weitere beteiligte Fachdisziplinen
Die Therapie von Patienten mit LKGF ist vom ersten Lebenstag an in hohem Maße interdisziplinär. Neben den bereits erwähnten Disziplinen sind Pädiatrie, Neonatologie und Anästhesiologie bei der primären stationären und perioperativen Versorgung sowie der Therapie von eventuellen Begleiterkrankungen führend. Zur Therapie von Störungen der Nahrungsaufnahme sollte den Eltern eine pränatale Beratung sowie postnatale Betreuung durch speziell geschultes Personal, beispielsweise aus den Hebammenwissenschaften (Still-/Laktationsberatung) angeboten werden (EbE ↑).
Die Fehlbildung beeinflusst neben den oberen Atemwegen außerdem zumeist das Mittelohr. Besonders bei Patienten mit den Gaumen betreffenden Fehlbildungen ist die physiologische Belüftung des Mittelohrs beeinträchtigt, wodurch es zu Paukenergüssen, chronischen Otitiden und einer Beeinträchtigung der Sprachentwicklung kommen kann. Die Hals-Nasen-Ohrenheilkunde und insbesondere die Teilbereiche der Pädaudiologie und Phoniatrie sind daher im multidisziplinären Behandlungsteam unverzichtbar.
Essenziell sind außerdem Diagnostik und Therapie durch Experten der Logopädie/Sprachtherapie, da die orofazialen Veränderungen Störungen der Sprechfunktion und teils sekundär des Spracherwerbs nach sich ziehen können. Ein regelmäßiges Screening auf psychosoziale Probleme und erhöhte psychische Belastung sollte im Bedarfsfall die Mitbetreuung und frühzeitige Interventionen durch einen klinischen Psychologen im Rahmen der multidisziplinären Behandlung ermöglichen.
Fazit
Die umfängliche Rehabilitation und Optimierung der mundgesundheitsbezogenen Lebensqualität von Patienten mit LKGF ist in allen Entwicklungsphasen auf zahnärztliche Expertise angewiesen. Anhand der Empfehlungen der neu erstellten Leitlinie sollen Therapiestandards auf Basis der aktuell vorhandenen Evidenz etabliert werden. Die in vielen Teilbereichen niedrige Qualität der Evidenz unterstreicht allerdings auch die Bedeutung einer einheitlichen, langfristigen Datenerhebung und den Bedarf an zukünftigen qualitativ hochwertigen klinischen Studien.
Förderung: Die Erstellung der Leitlinie wurde mit Mitteln des Innovationsausschusses beim Gemeinsamen Bundesausschuss unter dem Förderkennzeichen 01VSF21008 gefördert.
Eine Kurzfassung dieser Leitlinie mit Fokus auf die humanmedizinischen Aspekte der Versorgung wurde vom Deutschen Ärzteblatt zur Veröffentlichung akzeptiert.
Literaturliste
Antonarakis, G.S., Palaska, P.-K., Herzog, G. (2013): Caries prevalence in non-syndromic patients with cleft lip and/or palate: a meta-analysis. in: Caries Res, 47, 5, S. 406–13.
AWMF (2023): AWMF-Regelwerk „Leitlinien“. www.awmf.org/regelwerk/ (06.05.2025).
Azevedo SG, de Oliveira LQR, Martelli-Júnior H, Coletta RD, Machado RA. Tooth Anomalies in Patients With Nonsyndromic Orofacial Cleft: A Systematic Review and Meta-Analysis. Oral Dis. 2025 Jan 6. doi: 10.1111/odi.15226. Epub ahead of print. PMID: 39760181.
Bokhout, B., Hofman, F.X., van Limbeek, J., Kramer, G.J., Prahl-Andersen, B. (1996a): Increased caries prevalence in 2.5-year-old children with cleft lip and/or palate. in: Eur J Oral Sci, 104, 5-6, S. 518–22.
Bokhout, B., van Loveren, C., Hofman, F.X., Buijs, J.F., van Limbeek, J., Prahl-Andersen, B. (1996b): Prevalence of Streptococcus mutans and lactobacilli in 18-month-old children with cleft lip and/or palate. in: Cleft Palate Craniofac J, 33, 5, S. 424–28.
Cheng, L.L., Moor, S.L., Ho, C.T.C. (2007): Predisposing factors to dental caries in children with cleft lip and palate: a review and strategies for early prevention. in: Cleft Palate Craniofac J, 44, 1, S. 67–72.
DGMKG, D. (2025): Therapie der Lippen-Kiefer-Gaumenfehlbildungen, Langfassung. Version 1. www.awmf.org/leitlinien/detail/ll/007-038.html (28.01.2025).
Di Chiaro, B., Santiago, G., Santiago, C., Zelko, I., Choudhary, A., Purnell, C.A. (2022): A Systematic Review of Primary Rhinoplasty in Patients With Bilateral Cleft Lip. in: J Craniofac Surg, 33, 8, S. 2406–10.
Dogan, E., Seckin, O. (2020): Maxilläre Protraktion bei Patienten mit einseitiger Lippen-Kiefer-Gaumenspalte : Evaluierung von Weich- und Hartgeweben mit dem Alt-RAMEC-Protokoll. in: J Orofac Orthop, 81, 3, S. 209–19.
Hagen, A., Gorenoi, V., Tavassol, F., Krauth, C., Mertz, M., Kahrass, H., Strech, D., Beck, S., Seidel, G. (2019): HT17-01: Lippen-Kiefer-Gaumenspalte: Führt die Anwendung der Nasoalveolar-Molding-Methode vor einer Operation zu besseren Ergebnissen? [HTA-Report].
Hammond, N.L., Dixon, M.J. (2022): Revisiting the embryogenesis of lip and palate development. in: Oral Dis, 28, 5, S. 1306–26.
Kern, M., Passia, N., Sasse, M., Yazigi, C. (2017): Ten-year outcome of zirconia ceramic cantilever resin-bonded fixed dental prostheses and the influence of the reasons for missing incisors. in: J Dent, 65, S. 51–55.
Liou, E.J.-W., Tsai, W.-C. (2005): A new protocol for maxillary protraction in cleft patients: repetitive weekly protocol of alternate rapid maxillary expansions and constrictions. in: Cleft Palate Craniofac J, 42, 2, S. 121–27.
Marzouk, T., Alves, I.L., Wong, C.L., DeLucia, L., McKinney, C.M., Pendleton, C., Howe, B.J., Marazita, M.L., Peter, T.K., Kopycka-Kedzierawski, D.T., Morrison, C.S., Malmstrom, H., Wang, H., Shope, E.T. (2021): Association between Dental Anomalies and Orofacial Clefts: A Meta-analysis. in: JDR Clin Trans Res, 6, 4, S. 368–81.
Mossey, P.A., Modell, B. (2012): Epidemiology of oral clefts 2012: an international perspective. in: Front Oral Biol, 16, S. 1–18.
Padovano, W.M., Skolnick, G.B., Naidoo, S.D., Snyder-Warwick, A.K., Patel, K.B. (2022): Long-Term Effects of Nasoalveolar Molding in Patients With Unilateral Cleft Lip and Palate: A Systematic Review and Meta-Analysis. in: Cleft Palate Craniofac J, 59, 4, S. 462–74.
Papadopoulos, M.A., Koumpridou, E.N., Vakalis, M.L., Papageorgiou, S.N. (2012): Effectiveness of pre-surgical infant orthopedic treatment for cleft lip and palate patients: a systematic review and meta-analysis. in: Orthod Craniofac Res, 15, 4, S. 207–36.
Papi, P., Giardino, R., Sassano, P., Amodeo, G., Pompa, G., Cascone, P. (2015): Oral health related quality of life in cleft lip and palate patients rehabilitated with conventional prostheses or dental implants. in: J Int Soc Prev Community Dent, 5, 6, S. 482–87.
Queiroz Herkrath, Ana Paula Corrêa de, Herkrath, F.J., Rebelo, M.A.B., Vettore, M.V. (2015): Measurement of health-related and oral health-related quality of life among individuals with nonsyndromic orofacial clefts: a systematic review and meta-analysis. in: Cleft Palate Craniofac J, 52, 2, S. 157–72.
Sales, P.H.H., Oliveira-Neto, O.B., Torres, T.S., Lima, F.J.C. de (2019): Effectiveness of dental implants placed in bone graft area of cleft Patients. in: Int J Oral Maxillofac Surg, 48, 8, S. 1109–14.
Sami, Q.-U.-A., Ali, B., Farooqui, W.A. (2023): Effects of Alt-RAMEC protocol with facemask therapy in cleft lip palate patients in a sample of Pakistani population. in: BMC Oral Health, 23, 1, S. 401.
Uzel, A., Alparslan, Z.N. (2011): Long-term effects of presurgical infant orthopedics in patients with cleft lip and palate: a systematic review. in: Cleft Palate Craniofac J, 48, 5, S. 587–95.
van Loveren, C., Buijs, J.F., Bokhout, B., Prahl-Andersen, B., Cate, J.M. ten (1998): Incidence of mutans streptococci and lactobacilli in oral cleft children wearing acrylic plates from shortly after birth. in: Oral Microbiol Immunol, 13, 5, S. 286–91.
Zelko, I., Zielinski, E., Santiago, C.N., Alkureishi, L.W.T., Purnell, C.A. (2023): Primary Cleft Rhinoplasty: A Systematic Review of Results, Growth Restriction, and Avoiding Secondary Rhinoplasty. in: Plast Reconstr Surg, 151, 3, 452e-462e.