Regeneration des Knochens – präimplantologische Augmentationstechniken
Die Insertion dentaler Implantate ist eine etablierte Methode zur funktionellen und ästhetischen Rehabilitation des teilbezahnten oder zahnlosen Gebisses. Um eine Exposition der Implantatoberfläche aufgrund einer zu geringen Dicke der buccalen Knochenlamelle im Verlauf zu vermeiden, können augmentative Maßnahmen zur Optimierung der Knochenquantität vor oder während der Implantatinsertion durchgeführt werden [Monje et al., 2019; Yoda et al., 2017].
Hierbei gilt es, die medizinischen Einflussfaktoren, die eine erhöhte Komplikationsrate beziehungsweise eine geringe Knochenneubildungsrate zur Folge haben können, in Erwägung zu ziehen und gemeinsam mit dem Patienten eine Risiko-Nutzen-Abwägung durchzuführen. Eine Reihe von Studien konnte zeigen, dass insbesondere Rauchen, anamnestische Parodontopathien und ein schlecht eingestellter Diabetes mellitus mit einer verringerten Erfolgsrate einhergehen können [Wagner et al., 2022; Sakkas et al., 2018]. Ferner gilt es, weitere Risikofaktoren wie den Zustand nach einer Bestrahlung im Kopf-Hals-Bereich oder die Einnahme von Antiresorptiva, Serotonin-Wiederaufnahmeinhibitoren (SSRI) und Protonenpumpeninhibitoren (PPI) zu eruieren, da auch diese Umstände/Medikamente sich negativ auf das Augmentationsergebnis auswirken können [Carr et al., 2019; Shugaa-Addin et al., 2016; Schiegnitz et al., 2022; Stavropoulos et al., 2018; Chrcanovic et al., 2017a, 2017b].
Erfolgen die knochenaufbauenden Maßnahmen während der Implantatinsertion, entspricht dies einem einzeitigen Vorgehen. Gering ausgeprägte Konturaugmentationen, Dehiszenzdefekte, aber auch Fenestrationen stellen hierbei mögliche Indikationen eines einzeitigen Vorgehens dar [Troeltzsch et al., 2016].
Bei fortgeschrittener Resorption, die bei der Einbringung des Implantats mit einer langstreckigen beziehungsweise mehrwandigen Exposition der Implantatoberfläche oder ohne sichere Primärstabilität einhergeht, ist ein zweizeitiges Vorgehen angezeigt. Die Augmentation ist hierbei erforderlich, um sowohl angemessen dimensionierte Implantate einzubringen als auch um passende Bedingungen für eine ästhetische und funktionelle Implantatprothetik zu schaffen. Die Einbringung des Implantats erfolgt hierbei in einem separaten Eingriff nach Konsolidierung des Augmentats.
Defektklassifikation
Die präimplantologische Rekonstruktion kann in unterschiedlichen klinischen Defektkonfigurationen erforderlich sein und den Chirurgen mit unterschiedlichen Herausforderungen konfrontieren. In diesem Zusammenhang lässt sich der vorliegende Defekt anhand der Klassifikation von Terheyden et al. beschreiben, die das charakteristische Resorptionsverhalten des Alveolarkamms nach Zahnextraktion berücksichtigt [Terheyden, 2010]. Die Defekttypen sind danach in vier Viertel unterteilt, die den Umfang des bestehenden Knochenverlusts in Beziehung zur Position des künftigen Implantats setzen. Eine initiale Resorption des kresto/vestibulären Alveolarfortsatzes (1/4-Defekt, weniger als 50 Prozent der vorgesehenen Implantatlänge) ist hierbei gefolgt von einer anhaltenden buccalen Resorption (2/4-Defekt, mehr als 50 Prozent der vorgesehenen Implantatlänge), bevor der Alveolarkamm durch Resorption der oralen Anteile partiell (3/4-Defekt) und schließlich total (4/4-Defekt) verloren geht. Das Modell lässt sich auf Einzelzahnlücken, ausgedehnte Lücken, Freiendsituationen und auch einen zahnlosen Kiefer anwenden.
Darüber hinaus kann die Klassifikation eines Defekts beziehungsweise das Ausmaß einer Augmentation dahingehend bewertet werden, ob der geplante Eingriff sich innerhalb der „knöchernen Hülle“ („bony envelope“) oder bis außerhalb der knöchernen Kontur erstreckt. Besteht die Indikation zur Augmentation außerhalb des „bony envelope“, wird in der Regel ein zweizeitiges Vorgehen empfohlen.
Der Kontinuitätsdefekt, der die Folge eines Traumas oder der Resektion eines Tumors sein kann, nimmt eine Sonderstellung ein und wird häufig zweizeitig, das heißt nach Rekonstruktion mit einem mikrovaskulären Transplantat (mikrovaskuläres Fibula-, Beckenkamm- oder Scapulatransplantat), implantologisch versorgt.
Autologe Knochenentnahme bei ausgeprägten Augmentationen
Aufgrund seiner osteoinduktiven, osteokonduktiven und genetischen Eigenschaften besitzt der autologe Knochen im Vergleich zu Knochenersatzmaterialien ein höheres regeneratives Potenzial, so dass dessen Anwendung bei ausgeprägten Augmentationsvolumina einen hohen Stellenwert besitzt und als biologischer Goldstandard anerkannt ist [Bauer und Muschler, 2000].
Je nach Defektgröße können hierbei intraorale (bis 5 mm) oder extraorale Spenderregionen (mehr als 5 mm) gewählt werden. Beliebte enorale Entnahmeregionen sind der horizontale beziehungsweise der aufsteigende Unterkieferast oder die Mentalregion [Sittitavornwong und Gutta, 2010]. Die Knochenmenge, die im Rahmen einer Implantatbohrung oder bei mit Knochenschabern gewonnenen Knochenspänen anfällt, ist gering und spielt daher in der präimplantologischen Chirurgie eine eher untergeordnete Rolle. Die Entnahme von enoralem autologem Knochen kann unter Lokalanästhesie erfolgen, wohingegen die extraorale Knochenentnahme in der Regel in Intubationsnarkose erfolgt.
Patientenfall
Nach Resektion der krestalen Anteile des Unterkiefers im Sinne einer Kastenresektion zusammen mit Anteilen des anterioren Mundbodens und der Zunge aufgrund eines Plattenepithelkarzinoms stellte sich der 65-jährige Patient nach Abschluss einer adjuvanten Brachytherapie in einem guten Allgemein- und Ernährungszustand mit dem Wunsch nach einer implantatprothetischen Versorgung des anterioren Unterkiefers von Regio 34–45 vor. Der klinische und der radiologische Befund zeigten eine dehiszenzfreie Situation, ohne Anhalt für eine Osteoradionekrose bei suffizienter weichgewebiger Deckung des knöchernen Defekts durch ein fasziokutanes Radialis-Transplantat (Abbildungen 1 und 2).
Abb. 1: Postoperative Panoramaschichtaufnahme bei Zustand nach Kastenresektion aufgrund eines Plattenepithelkarzinoms im Bereich des anterioren Unterkiefers von Regio 34–45 | UK Erlangen
Abb. 2: Dehiszenzfreie enorale Situation bei Zustand nach Defektdeckung mittels fasziokutanem Radialis-Transplantat | Tobias Möst
Obwohl die Restknochenhöhe die Insertion dentaler Implantate erlaubt hätte, wäre die funktionelle und ästhetische implantatprothetische Rehabilitation aufgrund einer starken kaudalen Position der Implantate erschwert gewesen, so dass bei guter weichgewebiger Situation die Entscheidung für eine Auflagerungsosteoplastik mit mehreren kortikospongiösen Blöcken aus dem Becken fiel (Abbildungen 3 und 4).
Abb. 3: Intraoperative Aufnahme nach Durchführung einer Auflagerungsosteoplastik mittels autologen Knochenblöcken aus dem Becken | Tobias Möst
Abb. 4: Postoperative Panoramaschichtaufnahme bei Zustand nach Blockaugmentation des anterioren Unterkiefers | UK Erlangen
Nach einer Einheilzeit von circa vier Monaten erfolgten die Ausdünnung des Transplantats, die Insertion von vier dentalen enossalen Implantaten sowie die Durchführung einer Vestibulumplastik zur Optimierung des weichgewebigen Lagers (Abbildung 5).
Abb. 5: Postoperative Panoramaschichtaufnahme bei Zustand nach Implantatinsertion im Bereich des anterioren Unterkiefers | UK Erlangen
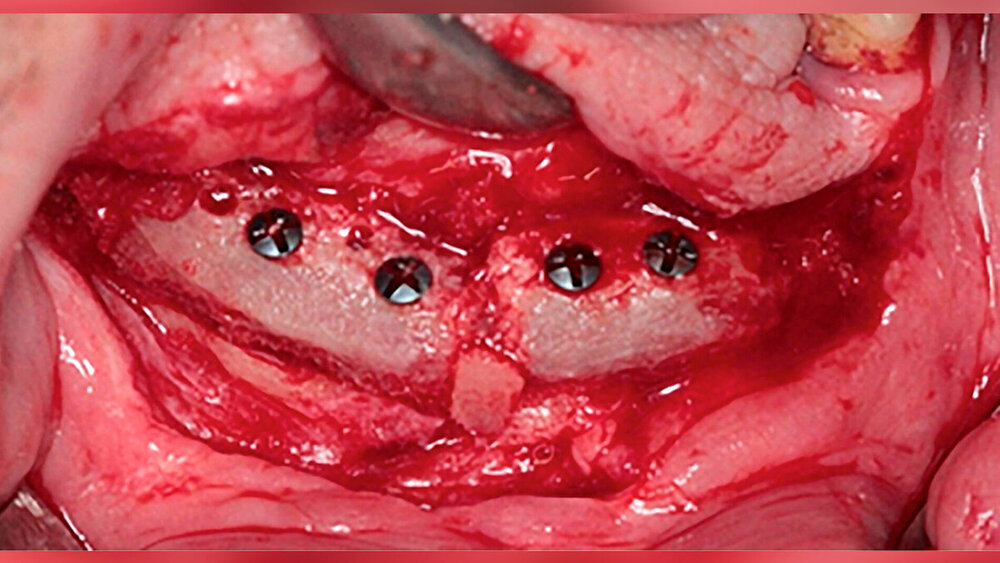
Nach einer Einheilzeit von circa vier Monaten folgte die Freilegung der Implantate und die Eingliederung des festsitzenden Zahnersatzes (Abbildungen 6 und 7).
Abb. 6: Enorale Aufnahme mehrere Wochen nach Freilegung vor Insertion des definitiven Zahnersatzes | Tobias Möst
Abb. 7: Enorale Aufnahme nach Eingliederung des finalen Zahnersatzes | Tobias Möst
Im Fall einer Knochenentnahme aus dem Ramus mandibulae kann mittels marginaler Schnittführung mit dorsaler Entlastung in Richtung des aufsteigenden Unterkieferastes der retromolare Knochen dargestellt werden. Die möglichst parallelen Osteotomien auf der lateralen Ramusseite legen die Länge und die Höhe des Transplantats fest und umfassen lediglich die kortikale Schicht. Eine dritte Osteotomie in der sagittalen Ebene verbindet die parallel verlaufenden Osteotomien entsprechend der vorliegenden Kortikalisbreite. Nach Schwächung der vestibulären Kortikalis können der Block entnommen, das Defektareal mit einem Kollagenvlies gefüllt und der Wundverschluss durchgeführt werden.
Zur Entnahme von Knochen aus der Kinnregion kann eine horizontale Inzision tief im Vestibulum unter Durchtrennung der Musculi mentales gewählt werden. Unter Schonung des Nervus mentalis folgt die Darstellung des Unterkieferknochens und die Hebung des Knochens mittels Trepanbohrer unter Einhaltung eines Sicherheitsabstands zu den Wurzelspitzen der unteren Frontzähne und der Foramina mentalia. Eine Perforation der lingualen Kortikalis gilt es zu vermeiden. Nach Entnahme des Knochenblocks kann die Defektfüllung mit einem Kollagenvlies erfolgen, bevor ein spannungsfreier und speicheldichter Wundverschluss folgt.
Sollten allerdings größere Mengen an autologem Knochen benötigt werden, ist eine extraorale Knochenentnahme zum Beispiel die Entnahme eines Beckenkammtransplantats in Vollnarkose angezeigt [Troeltzsch et al., 2016]. Die Knochenblockentnahme aus dem Beckenkamm wird hierbei häufig als Goldstandard angegeben [Sakkas et al., 2017]. Im Fall eines Kontinuitätsdefekts ist eine mikrovaskuläre Rekonstruktion zum Beispiel mit einem Fibula-, Scapula- oder Beckenkammtransplantat angezeigt. Die Auswahl der entsprechenden Entnahmestelle richtet sich nach der Ausdehnung des Befunds, nach den anatomischen Gegebenheiten der Spenderregion (Gefäßversorgung des Unterschenkels bei Fibulatransplantat) und gegebenenfalls der Notwendigkeit einer Hautinsel.
Gesteuerte Knochenregeneration (GBR-Technik)
Das Grundprinzip der gesteuerten Knochenregeneration (guided bone regeneration – GBR) stellt die Anwendung eines partikulären Materials in Kombination mit einer Barriere dar. Barrieren dienen der effektiven Abschirmung von Weichgewebe, um langsam migrierenden osteogenen Zellen das Einwachsen in den Defekt beziehungsweise auf das angewendete Knochenersatzmaterial zu ermöglichen. Darüber hinaus dienen Barrieren dazu, das Defektvolumen zu wahren, was insbesondere für Augmentationen großer Knochenvolumina essenziell ist. Als mögliche Barrieren können Membranen (resorbierbar / nicht resorbierbar), Gitter oder Knochenschalen dienen, deren Anwendung wiederum vom Augmentationsvolumen abhängt.
Kollagenbasierte, PTFE- oder PLA-/PGA-Membranen können erfolgreich für geringe vertikale oder horizontale Defekte bis 3 mm angewendet werden, wobei kollagenbasierte und PTFE-Membranen die besten Ergebnisse zeigten [Troeltzsch et al., 2016; Merli et al., 2014]. Formstabile Varianten der Barriere, zum Beispiel in Form von titanverstärkten Membranen [Mendoza-Azpur et al., 2018] oder Titangittern, können für vertikale und horizontale Alveolarkammdefekte größer 3 mm angewendet werden [Sagheb et al., 2017]. Durch 3-D-Bildgebung individualisiert hergestellte Titangitter können den intraoperativen Aufwand der Gitteradaptation und damit die OP-Dauer reduzieren [Sagheb et al., 2017]. Die Notwendigkeit eines Zweiteingriffs zur Entfernung einer nicht-resorbierbaren Membran / eines Gitters und die Gefahr der Exposition und der Notwendigkeit einer Entfernung bei ausbleibender Sekundärgranulation des infizierten Materials werden als potenzielle Nachteile aufgeführt [Hartmann et al., 2019]. Zur Verbesserung der Dehiszenzrate wird der kombinierte Einsatz von resorbierbaren Kollagenmembranen und von PRF diskutiert [Lorenz et al., 2018].
Auflagerungsosteoplastik
Ist eine Implantation aufgrund eines horizontalen Defizits (2/4-Defekt) beziehungsweise aufgrund eines vertikalen und/oder kombiniert vertikalen und horizontalen Defizits (3/4-Defekt oder 4/4-Defekt) mit einem knöchernen Defizit von mehr als 3 mm nicht möglich, kann eine Auflagerungsosteoplastik eingesetzt werden.
Aufgrund des regenerativen Potenzials von autologem Knochen wird die Verwendung von autologen Blöcken bevorzugt. Mit intraoral entnommenen Blöcken können Defekte bis zu 5 mm bewältigt werden, wohingegen bei größeren Defekten die Verwendung extraoral entnommener Blöcke empfohlen wird [Troeltzsch et al., 2016]. Klinische Studien zeigen, dass die Applikation allogener Blöcke bei geringem knöchernem Bedarf ebenfalls eingesetzt werden kann [Kloss et al., 2018; Blume et al., 2017; Motamedian et al., 2016].
Bei einer geplanten horizontalen Blockaugmentation erfolgen eine krestale Schnittführung bis zu den angrenzenden Zähnen, die Präparation eines Mukoperiostlappens und die Darstellung des knöchernen Augmentatlagers. Um eine Gefäßeinsprossung und damit eine von basal beginnende Regeneration zu ermöglichen, wird die kortikale Oberfläche des Empfängerknochens mit einem Rosenbohrer bis in den Markraum perforiert. Der Knochenblock wird an den Defekt angepasst und mit Osteosyntheseschrauben fixiert. Dabei sollte auf einen möglichst spaltfreien Kontakt zwischen dem ortsständigen Knochen und dem Knochenblock geachtet werden. Persistierende Spalten zwischen dem Blocktransplantat und dem darunter liegenden ortsständigen Knochen können mit partikulärem autologem Knochen aufgefüllt werden. Um eine knöcherne Konsolidierung zu ermöglichen, ist eine rotationsstabile Fixation essenziell, wodurch die Insertion mehrerer Schrauben indiziert sein kann. Nach der Glättung scharfer Knochenkanten kann der Block mit einer Membran bedeckt werden. Es folgt der spannungsfreie und speicheldichte Wundverschluss mit einem resorbierbaren Nahtmaterial.
Schalentechnik
Eine Sonderform der präimplantologischen Knochenaugmentation ist die Schalentechnik, mit der als Modifikation der Blocktechnik vestibuläre Resorptionen, aber auch vollständig vertikale Resorptionen korrigiert werden können [Khoury und Hanser, 2015].
In Analogie zur Auflagerungsosteoplastik mit einem in der Regel retromolar gewonnenen Knochenblock wird aus dem Blockmaterial mithilfe einer dünnen diamantierten Trennscheibe/Säge die kortikale Knochenwand in Längsrichtung separiert und damit eine wandartige formstabile Schale an der bukkalen Kammseite mithilfe einer Positionierungsschraube fixiert [Khoury und Hanser, 2015]. In Situationen mit einem vertikalen Defizit können die kortikalen Schalen lingual und vestibulär angebracht werden. Auf diese Weise entsteht ein Zwischenraum zwischen dem lingualen Knochen und der Schale (2/4-Defekt) beziehungsweise zwischen der lingualen und der buccalen Schale (3/4- und 4/4-Defekt), der mit dem residuellen partikulierten autologen Blockmaterial aufgefüllt werden kann.
Die zusätzliche Anwendung eines xenogenen partikulären Knochenersatzmaterials auf die augmentierte Oberfläche („augmentative relining“) kann als Resorptionsschutz dienen und führt zu einem zusätzlichen Zugewinn an Augmentationsvolumen [De Stavola und Tunkel, 2013]. Eine aktuelle klinische Studie weist darauf hin, dass die Anwendung allogener Platten eine mögliche Alternative zu autologen Platten darstellt [Tunkel et al., 2021].
Nach stumpfer Mobilisation der Mundschleimhaut im Bereich des Mundbodens sowie einer Periostschlitzung im Bereich des vestibulären Mukoperiostlappens lässt sich ein speicheldichter und spannungsfreier Wundverschluss mit einem resorbierbaren Nahtmaterial erreichen. Nach einer Einheilungsphase von vier bis fünf Monaten erfolgt der Reentry zur Entfernung der Osteosyntheseschrauben und zur Implantatinsertion.
Interpositionsosteoplastik
Zum vertikalen Knochenaufbau bei starker Atrophie sowohl der buccalen als auch der lingualen Wand des Alveolarfortsatzes (4/4-Defekt-Konfiguration) kann eine Interpositionsosteoplastik (als „Sandwich-Technik“ bekannt) durchgeführt werden [Brandtner et al., 2014; Terheyden et al., 2007]. Dabei werden nach Schnittführung in der Mitte des Alveolarfortsatzes ein Mukoperiostlappen präpariert und der vestibuläre Knochen dargestellt. Das linguale Weichgewebe wird nicht mobilisiert. Nach der Präparation eines kastenförmigen Knochensegments kranial des Verlaufs des N. alveolaris inferior folgt die Mobilisation des Segments nach kranial, wobei der Knochen am lingualen Weichgewebe gestielt bleibt. Eine Restknochenhöhe krestal des N. alveolaris inferior von 4 – 5 mm sollte nicht unterschritten werden, um eine Schädigung des Nervens zu vermeiden.
Eine Interpositionsosteoplastik wird bevorzugt im posterioren Unterkiefer durchgeführt, eine Interposition im Bereich des anterioren Oberkiefers ist ebenfalls möglich, allerdings ist hier das realisierbare vertikale Augmentationsausmaß aufgrund der geringen Elastizität der palatinalen Weichgewebe auf wenige Millimeter beschränkt. Das an der Schleimhaut gestielte krestale Knochenfragment wird mit Osteosyntheseplatten in der Zielposition fixiert und der entstehende Spalt zwischen dem ortsständigen Knochen und dem mobilisierten Segment wird mit Knochenersatzmaterial oder autologem Knochen aufgefüllt [Starch-Jensen und Nielsen, 2020]. Die Verwendung von autologem Knochen oder von Knochenersatzmaterial scheint keinen Einfluss auf den Behandlungs- beziehungsweise Implantaterfolg zu haben [Starch-Jensen und Nielsen, 2020]. Der suffiziente und speicheldichte Wundverschluss erfolgt nach Periostschlitzung vestibulär.
Eine Sonderstellung nimmt der zahnlose atrophe Oberkiefer ein, der sich entsprechend den Resorptionscharakteristika nach Cawood et al. [1988] durch eine zentripetale Resorption mit dem möglichen klinischen Bild einer Pseudoprogenie (Pseudo-Klasse-III-Relation) auszeichnet [Cawood und Howell, 1988]. Durch die Durchführung einer Le-Fort-I-Osteotomie mit dem Einbringen eines Interponats lässt sich die resorptionsbedingte Verlagerung des Oberkieferalveolarkamms korrigieren und ein Knochenangebot herstellen, das die Insertion normal positionierter Implantate zur Gestaltung einer optimalen, festsitzenden Prothetik erlaubt. Als positiver Nebeneffekt wird durch das gesteigerte vertikale Knochenvolumen zusätzlich eine Abstützung der Lippe erreicht, wodurch sich auch extraoral ein positiver Effekt auf die Ästhetik erzielen lässt.
Nach der krestalen Schnittführung von der Region des zweiten Molaren nach kontralateral folgt nach Darstellung der fazialen Kieferhöhlenwand eine vorsichtige Fenestration des Sinus maxillaris zur Elevation der Kieferhöhlenschleimhaut. Und nach Präparation der Kieferhöhlenschleimhaut folgt eine Osteotomie in der Le-Fort-I-Ebene, bevor mittels Meißel die mediale Kieferhöhlenwand und das Nasenseptum getrennt werden. Nach Mobilisation des Oberkiefers mittels Hohlmeißel vom Proc. pterygoideus bds. folgen die vorsichtige kaudale Mobilisation des Oberkiefers entsprechend der Operationsplanung und die Fixation mittels Plattenosteosynthese. Der Osteotomiespalt kann nun mit kortikospongiösen Beckenkammtransplantaten in der Eck- und in der Seitenzahnregion zur Stabilisierung der vertikalen Ebene augmentiert werden. Der Bereich zwischen den Knochenblöcken kann mit partikulärem Knochenersatzmaterial aufgefüllt werden.
Distraktionsosteogenese
Als mögliche weitere Technik zum Ausgleich eines vertikalen Knochendefizits kann die – technisch anspruchsvolle – Technik der Distraktionsosteogenese angewendet werden. Das zugrunde liegende biologische Prinzip besteht dabei in der Induktion von Knochenhartsubstanz in der Folge einer stetigen und langsamen Dehnung eines sich organisierenden Kallus, der sich durch eine gezielte Osteotomie zwischen zwei Knochenfragmenten entwickelt.
Die Distraktionsosteogenese umfasst drei Phasen: die erste Phase nach Distraktor-Applikation und Osteotomie zeichnet sich durch eine Regeneration der Weichgewebe und der Organisation eines Kallus zwischen den Fragmenten aus und umfasst eine Dauer von fünf bis sieben Tagen. In der zweiten Phase folgt die stetige Distraktion von 0,5 – 1 mm/Tag, bis das vertikale Knochendefizit ausgeglichen ist, woran sich die dritte, mehrwöchige Stabilisierungsphase anschließt. Durch die Distraktionsosteogenese kann Knochen guter Qualität im Vergleich zu anderen vertikalen Augmentationstechniken generiert werden, was sich in den langfristigen Daten für Implantatversorgungen beobachten lässt.
Die gerichtete Knochenneubildung ist allerdings durch eine Reihe von Komplikationen gefährdet [Zhao et al., 2018]. Der wirkende Kraftvektor kann bei Disktraktionsrichtungen entgegen oder tangential von Muskel- beziehungsweise bindegewebigen Zügen abweichen, was zu einer erschwerten gezielten Aktivierung des Distraktors führen kann. Weitere Komplikationen sind die Immobilität des zu bewegenden Segments (Transportsegment), die Störung der Okklusion durch die Distraktor-Apparatur, die vorzeitige knöcherne Konsolidierung vor Erreichen der Zieldistanz, der Verlust des Distraktors, eine Infektion, die Perforation der Mukosa, die Fraktur des Unterkiefers oder aber eine Resorption des Transportsegments. Aufgrund der relativ hohen Komplikationsrate in Kombination mit einer hohen Techniksensibilität und der erforderlichen Compliance des Patienten ist der Stellenwert der Distraktionsosteogenese im klinischen Alltag gering.
Einheildauer präimplantologischer Knochenaugmentationen
Die gewählte Wartezeit nach Durchführung des augmentativen Eingriffs sollte ausreichen, um die knöcherne Integration und die Bildung von vitalem Knochen im Augmentationsareal zu erreichen. Die Wahl des optimalen Zeitpunkts ist schwierig. Auf der einen Seite führt eine lange Einheilzeit zu mehr vitalem Knochen im Augmentationsgebiet, allerdings geht dies mit einer erhöhten Resorption und einer möglichen Exposition des Osteosynthesematerials einher. Insbesondere autologe Auflagerungsosteoplastiken zeigen bei einer Wartezeit von vier bis sechs Monaten eine erhebliche Volumenresorption. Hingegen kann eine Wartezeit von unter vier Monaten ebenfalls mit Problemen vergesellschaftet sein, die zu technischen Schwierigkeiten bei der Implantation führen – beispielsweise wenn sich das Augmentat vom Defektareal löst.
Fazit
Je nach Defektkonfiguration und der benötigten Knochenmenge stehen unterschiedliche Techniken und Materialien für die Hartgewebeaugmentation zur Auswahl. Partikuläres Material in Kombination mit einer resorbierbaren Membran zeigt sich bei einem geringen Knochendefizit als ausreichend. Bei einem größeren Knochendefizit kann die Anwendung nicht resorbierbarer Materialien in Kombination mit autolog gewonnenem Knochen nötig sein. Ab einem Knochendefizit von mehr als 5 mm ist die Entnahme von extraoralem Knochen nötig. Die letztlich ausgewählte Technik ist stark von der Expertise des Operateurs abhängig und sollte neben lokalen und systemischen Einflussfaktoren die Compliance des Patienten einbeziehen.
Literaturliste
BAUER, T. W. & MUSCHLER, G. F. 2000. Bone graft materials. An overview of the basic science. Clin Orthop Relat Res, 10-27.
BLUME, O., HOFFMANN, L., DONKIEWICZ, P., WENISCH, S., BACK, M., FRANKE, J., SCHNETTLER, R. & BARBECK, M. 2017. Treatment of Severely Resorbed Maxilla Due to Peri-Implantitis by Guided Bone Regeneration Using a Customized Allogenic Bone Block: A Case Report. Materials (Basel), 10.
BRANDTNER, C., BORUMANDI, F., KRENKEL, C. & GAGGL, A. 2014. A new technique for sandwich osteoplasty with interpositional bone grafts for fixation. Int J Oral Maxillofac Implants, 29, 1164-9.
CARR, A. B., GONZALEZ, R. L. V., JIA, L. & LOHSE, C. M. 2019. Relationship between Selective Serotonin Reuptake Inhibitors and Risk of Dental Implant Failure. J Prosthodont, 28, 252-257.
CAWOOD, J. I. & HOWELL, R. A. 1988. A classification of the edentulous jaws. Int J Oral Maxillofac Surg, 17, 232-6.
CHRCANOVIC, B. R., KISCH, J., ALBREKTSSON, T. & WENNERBERG, A. 2017a. Intake of Proton Pump Inhibitors Is Associated with an Increased Risk of Dental Implant Failure. Int J Oral Maxillofac Implants, 32, 1097-1102.
CHRCANOVIC, B. R., KISCH, J., ALBREKTSSON, T. & WENNERBERG, A. 2017b. Is the intake of selective serotonin reuptake inhibitors associated with an increased risk of dental implant failure? Int J Oral Maxillofac Surg, 46, 782-788.
DAU, M., KAMMERER, P. W., HENKEL, K. O., GERBER, T., FRERICH, B. & GUNDLACH, K. K. 2016. Bone formation in mono cortical mandibular critical size defects after augmentation with two synthetic nanostructured and one xenogenous hydroxyapatite bone substitute - in vivo animal study. Clin Oral Implants Res, 27, 597-603.
DE STAVOLA, L. & TUNKEL, J. 2013. A new approach to maintenance of regenerated autogenous bone volume: delayed relining with xenograft and resorbable membrane. Int J Oral Maxillofac Implants, 28, 1062-7.
HARTMANN, A., HILDEBRANDT, H., SCHMOHL, J. U. & KAMMERER, P. W. 2019. Evaluation of Risk Parameters in Bone Regeneration Using a Customized Titanium Mesh: Results of a Clinical Study. Implant Dent, 28, 543-550.
KHOURY, F. & HANSER, T. 2015. Mandibular bone block harvesting from the retromolar region: a 10-year prospective clinical study. Int J Oral Maxillofac Implants, 30, 688-97.
KLOSS, F. R., OFFERMANNS, V. & KLOSS-BRANDSTATTER, A. 2018. Comparison of allogeneic and autogenous bone grafts for augmentation of alveolar ridge defects-A 12-month retrospective radiographic evaluation. Clin Oral Implants Res, 29, 1163-1175.
LORENZ, J., AL-MAAWI, S., SADER, R. & GHANAATI, S. 2018. Individualized Titanium Mesh Combined With Platelet-Rich Fibrin and Deproteinized Bovine Bone: A New Approach for Challenging Augmentation. J Oral Implantol, 44, 345-351.
MENDOZA-AZPUR, G., GALLO, P., MAYTA-TOVALINO, F., ALVA, R. & VALDIVIA, E. 2018. A Case Series of Vertical Ridge Augmentation Using a Nonresorbable Membrane: A Multicenter Study. Int J Periodontics Restorative Dent, 38, 811-816.
MERLI, M., MOSCATELLI, M., MARIOTTI, G., ROTUNDO, R., BERNARDELLI, F. & NIERI, M. 2014. Bone level variation after vertical ridge augmentation: resorbable barriers versus titanium-reinforced barriers. A 6-year double-blind randomized clinical trial. Int J Oral Maxillofac Implants, 29, 905-13.
MONJE, A., CHAPPUIS, V., MONJE, F., MUNOZ, F., WANG, H. L., URBAN, I. A. & BUSER, D. 2019. The Critical Peri-implant Buccal Bone Wall Thickness Revisited: An Experimental Study in the Beagle Dog. Int J Oral Maxillofac Implants, 34, 1328-1336.
MOTAMEDIAN, S. R., KHOJASTE, M. & KHOJASTEH, A. 2016. Success rate of implants placed in autogenous bone blocks versus allogenic bone blocks: A systematic literature review. Ann Maxillofac Surg, 6, 78-90.
SAGHEB, K., SCHIEGNITZ, E., MOERGEL, M., WALTER, C., AL-NAWAS, B. & WAGNER, W. 2017. Clinical outcome of alveolar ridge augmentation with individualized CAD-CAM-produced titanium mesh. Int J Implant Dent, 3, 36.
SAKKAS, A., SCHRAMM, A., WINTER, K. & WILDE, F. 2018. Risk factors for post-operative complications after procedures for autologous bone augmentation from different donor sites. J Craniomaxillofac Surg, 46, 312-322.
SAKKAS, A., WILDE, F., HEUFELDER, M., WINTER, K. & SCHRAMM, A. 2017. Autogenous bone grafts in oral implantology-is it still a „gold standard“? A consecutive review of 279 patients with 456 clinical procedures. Int J Implant Dent, 3, 23.
SCHIEGNITZ, E., REINICKE, K., SAGHEB, K., KONIG, J., AL-NAWAS, B. & GROTZ, K. A. 2022. Dental implants in patients with head and neck cancer - a systematic review and meta-analysis of the influence of radiotherapy on implant survival. Clin Oral Implants Res.
SHUGAA-ADDIN, B., AL-SHAMIRI, H. M., AL-MAWERI, S. & TARAKJI, B. 2016. The effect of radiotherapy on survival of dental implants in head and neck cancer patients. J Clin Exp Dent, 8, e194-200.
SITTITAVORNWONG, S. & GUTTA, R. 2010. Bone graft harvesting from regional sites. Oral Maxillofac Surg Clin North Am, 22, 317-30, v-vi.
STARCH-JENSEN, T. & NIELSEN, H. B. 2020. Sandwich osteotomy of the atrophic posterior mandible with interpositional autogenous bone block graft compared with bone substitute material: a systematic review and meta-analysis. Br J Oral Maxillofac Surg, 58, e237-e247.
STAVROPOULOS, A., BERTL, K., PIETSCHMANN, P., PANDIS, N., SCHIODT, M. & KLINGE, B. 2018. The effect of antiresorptive drugs on implant therapy: Systematic review and meta-analysis. Clin Oral Implants Res, 29 Suppl 18, 54-92.
TERHEYDEN, H. 2010. Knochenaugmentationen in der Implantologie. . Deutsche Zahnärztliche Zeitung 6
, 320-330.
TERHEYDEN, H., SIMON, B., BEHFAR, L., RIEGER, M. & BEHRENS, E. 2007. Interpositionsplastik des zahnlosen Ober- und Unterkiefers Implantologie, 15, 297–304
TROELTZSCH, M., TROELTZSCH, M., KAUFFMANN, P., GRUBER, R., BROCKMEYER, P., MOSER, N., RAU, A. & SCHLIEPHAKE, H. 2016. Clinical efficacy of grafting materials in alveolar ridge augmentation: A systematic review. J Craniomaxillofac Surg, 44, 1618-1629.
TUNKEL, J., DE STAVOLA, L. & KLOSS-BRANDSTATTER, A. 2021. Alveolar ridge augmentation using the shell technique with allogeneic and autogenous bone plates in a split-mouth design-A retrospective case report from five patients. Clin Case Rep, 9, 947-959.
WAGNER, J., SPILLE, J. H., WILTFANG, J. & NAUJOKAT, H. 2022. Systematic review on diabetes mellitus and dental implants: an update. Int J Implant Dent, 8, 1.
YODA, N., ZHENG, K., CHEN, J., LI, W., SWAIN, M., SASAKI, K. & LI, Q. 2017. Bone morphological effects on post-implantation remodeling of maxillary anterior buccal bone: A clinical and biomechanical study. J Prosthodont Res, 61, 393-402.
ZHAO, K., WANG, F., HUANG, W. & WU, Y. 2018. Clinical Outcomes of Vertical Distraction Osteogenesis for Dental Implantation: A Systematic Review and Meta-Analysis. Int J Oral Maxillofac Implants, 33, 549-564.