Medikamentöse Behandlung eines Gendefekts
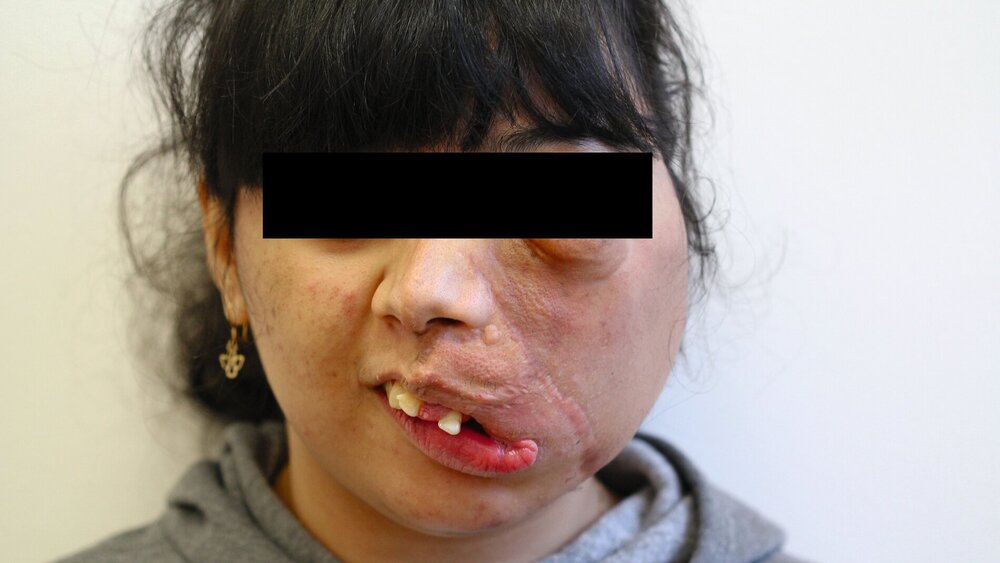
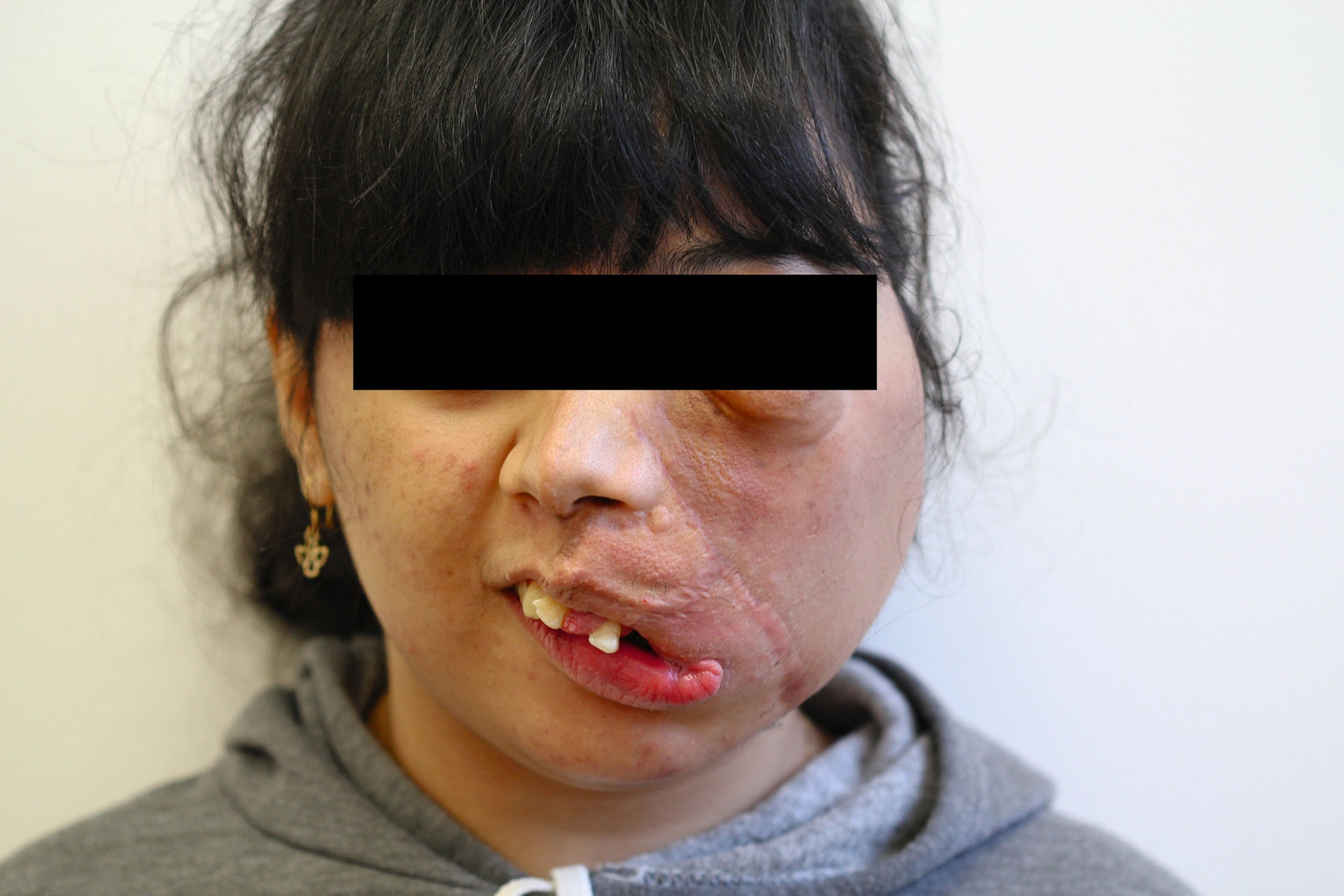
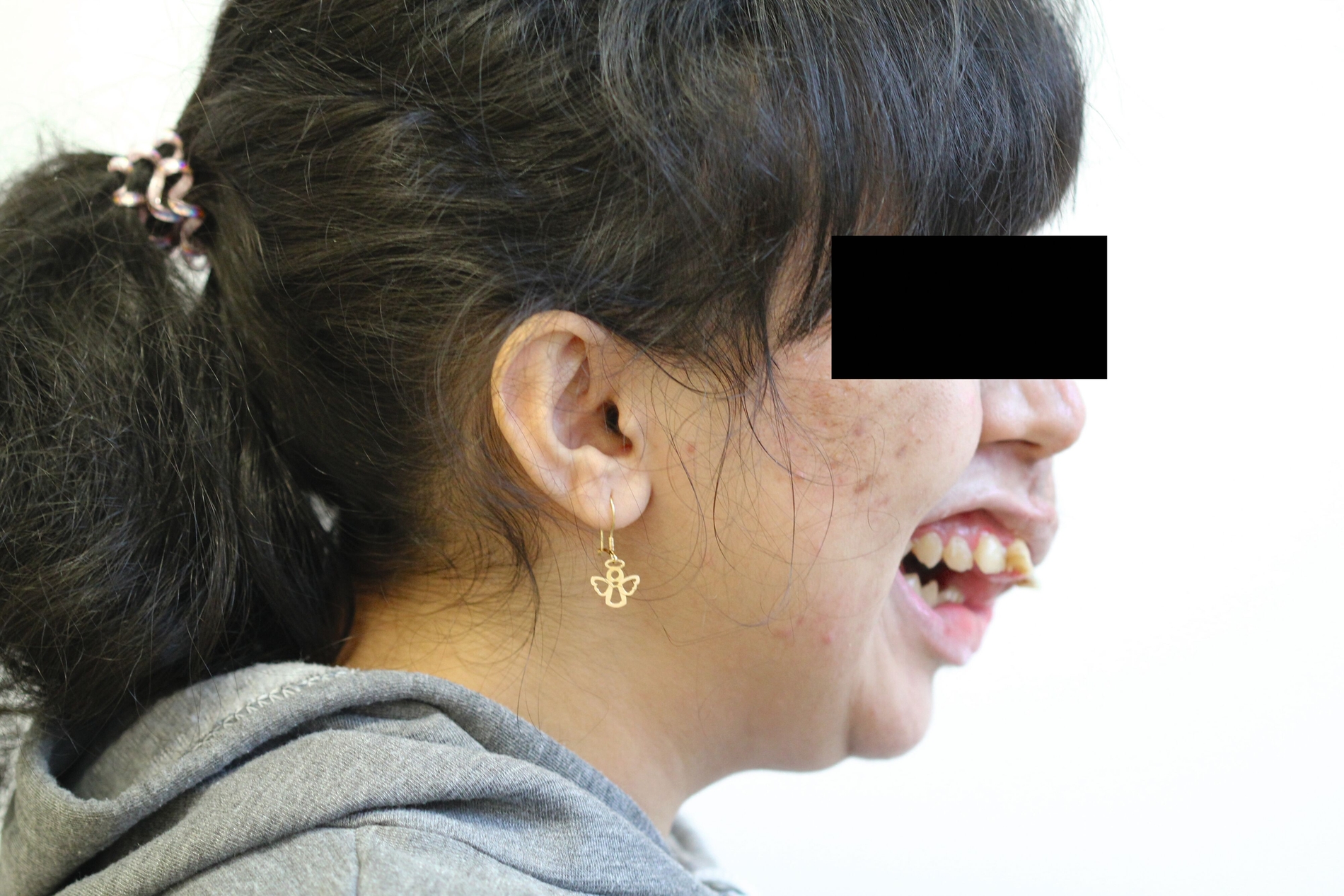
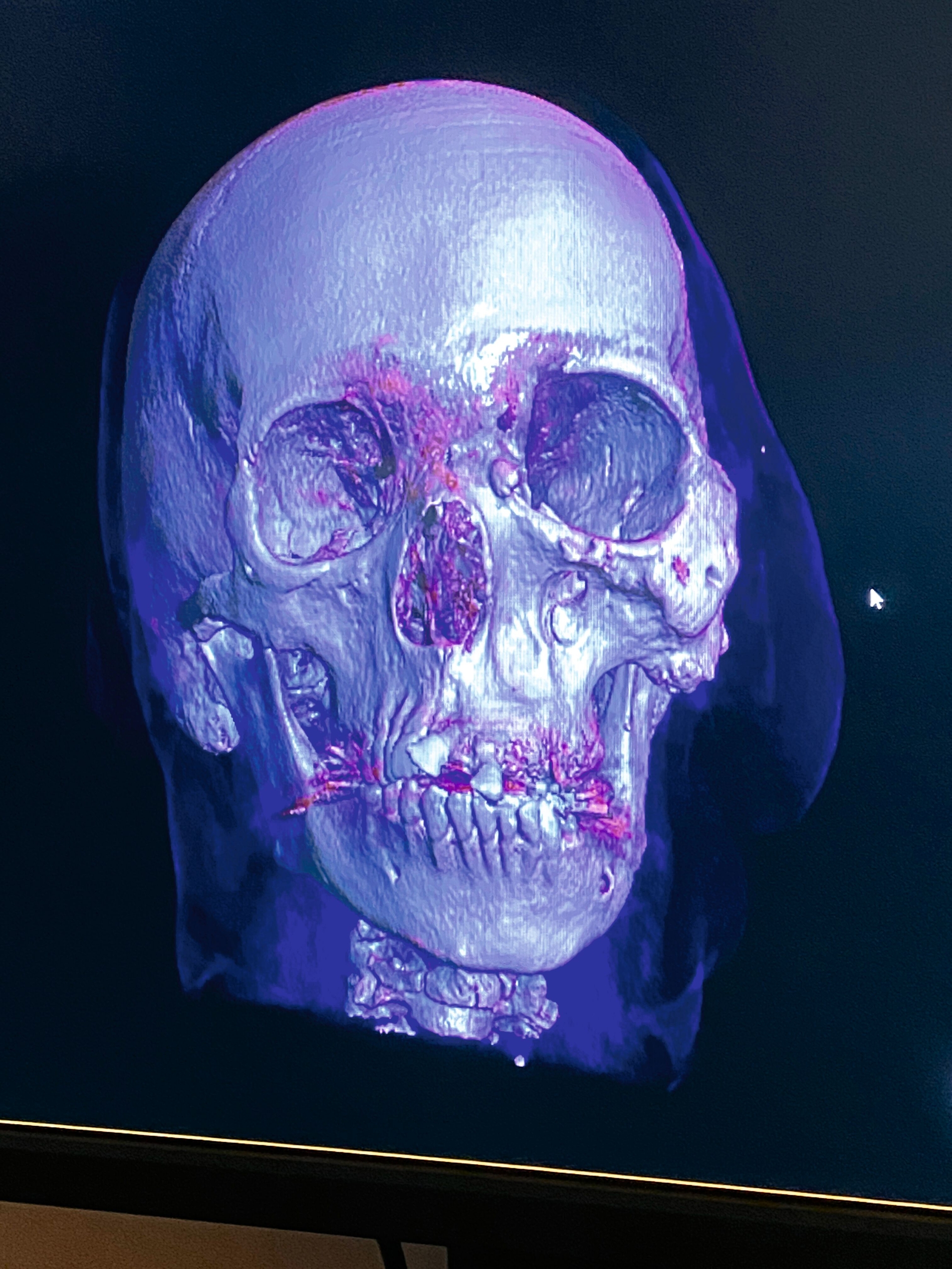
Bei der Diagnostik der Patientin in der Kieferklinik Münster zeigte sich eine Hypertrophie der linken Gesichtshälfte mit einer Skoliose des gesamten Gesichtsschädels (Abbildungen 1a und 1b). Von der Hypertrophie betroffen waren sowohl die knöchernen als auch die Weichgewebe der linken Gesichtshälfte. Die Haut wies Konturunregelmäßigkeiten und generell eine bräunliche Verfärbung auf.
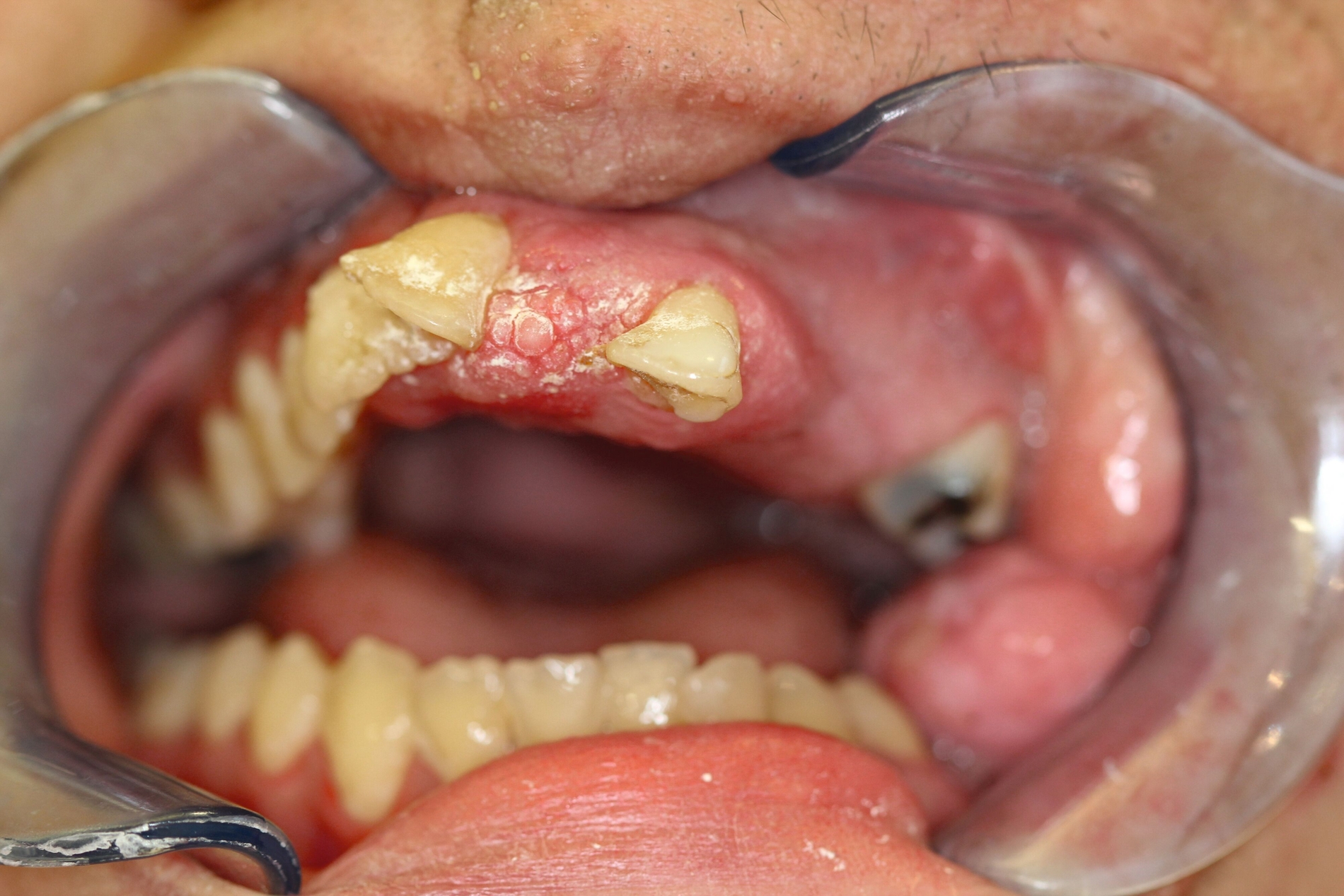
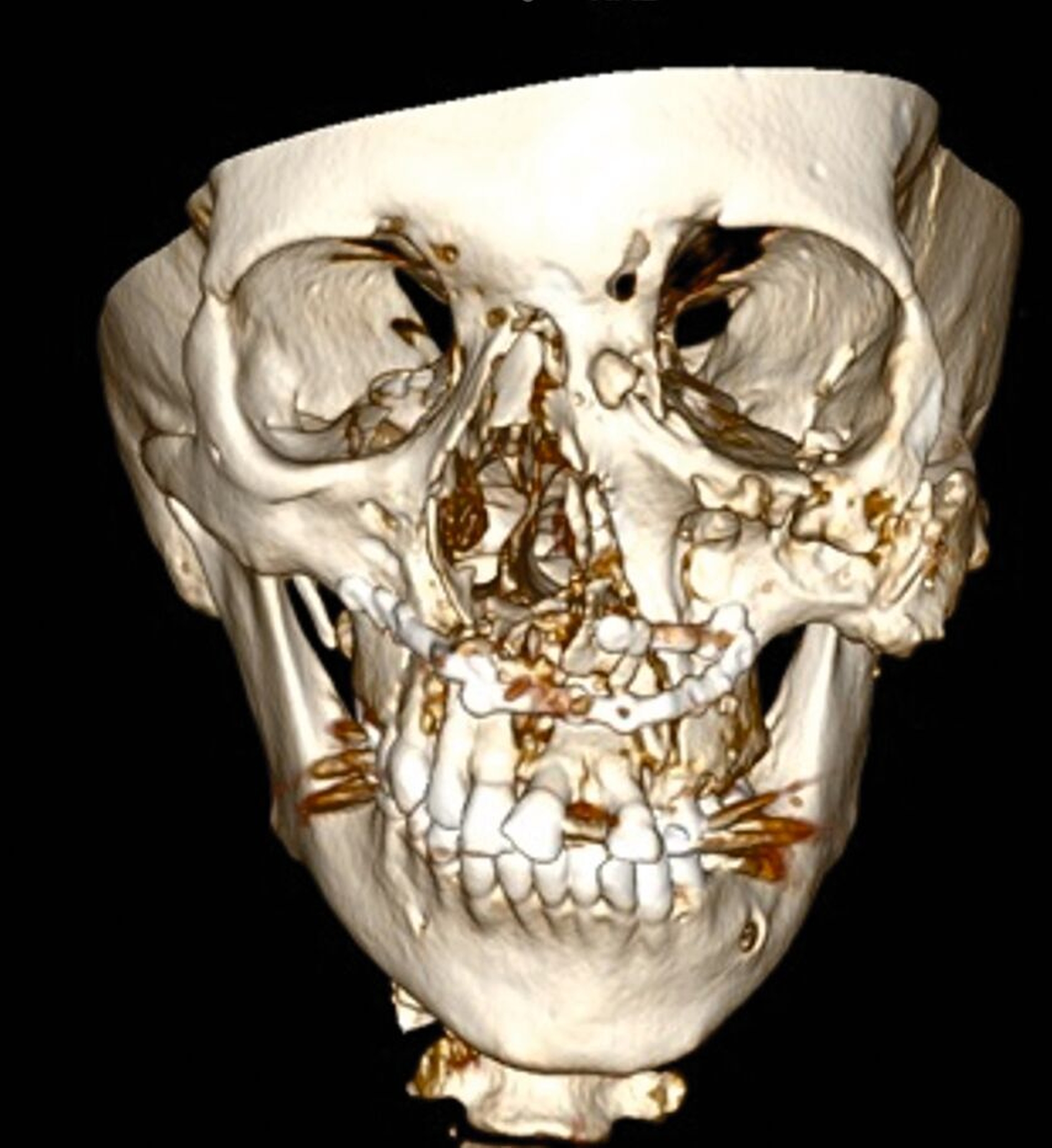
Intraoral zeigten sich stark ausgeprägte Weichgewebstumore im Bereich der linken Wange. In der Kindheit war in ihrem Heimatland Iran eine Operation unklarer Art erfolgt. Aufgrund der komplexen Dysgnathie mit einem Overjet von circa 22 mm war die Kaufähigkeit extrem eingeschränkt (Abbildung 1c). Eine Hyperostose im Bereich des linken Jochbeins und der linken Orbita war einer der weiteren führenden Befunde (Abbildung 2a). Die Ursache der Gesichtsfehlbildung war trotz humangenetischer Beratung nicht bekannt, ein Syndrom aufgrund der klinischen Erscheinung jedoch denkbar.
Geplant wurden mit der Patientin in einer ersten Operation eine Korrektur und Normalisierung der okklusalen/knöchernen Strukturen sowie eine Entfernung der tumorösen intraoralen Weichgewebsmassen und der knöchernen Hypertrophie im Jochbein/Orbitabereich. Ziel war es, der Patientin eine normale Kaufunktion zu ermöglichen. Histologische Untersuchungen der entnommenen Gewebe sollten die Diagnostik komplettieren. In einer zweiten Operation waren die Korrektur und die Reduzierung der Weichgewebsmassen der linken Gesichtshälfte geplant.
Die knöchernen Rekonstruktion wurde vorab virtuell geplant. Estellt wurden ein Intraoralscan der Zahnbögen sowie ein CT des Gesichtsschädels. Nach dem Matching der Zahnbögen mit dem CT-Datensatz erfolgte im zweiten Schritt die virtuelle Planung der Kiefersegmentverlagerungen sowie der Verlagerung des Nasoethmoidalkomplexes (Abbildungen 2) durch den Chirurgen. Für die Positionierung der Kiefersegmente wie auch des Nasoethmoidalkomplexes wurden dann Osteotomie- und Bohrschablonen gedruckt sowie die patientenspezifischen Osteosyntheseplatten hergestellt. Als zusätzliche intraoperative Kontrolle der Genauigkeit der OK-Segmentverlagerungen wurde ein Splint gedruckt (der bei einer solchen Vorgehensweise eigentlich nicht notwendig ist). Die Oberkiefersegmentpositionierung erfolgte mit den PSI-Osteosyntheseplatten, der gedruckte Splint diente der zusätzlichen Kontrolle. Die Knochenresektion im Bereich des Jochbogens und der Orbita erfolgte mit präfabrizierten intra- und extraoralen Sägeguides. Die prä- und postoperativen CT-Scans (Abbildungen 3a und 3b) und das intraoperative Foto zum Ende der Operation (Abbildung 3c) zeigen die Genauigkeit der Umsetzung der geplanten Chirurgie mit einer Normalisierung des Gesichtsskeletts und einer optimierten Okklusion (bei einem extremen Knochenbewegungsmuster von 22 mm Rückverlagerung von Oberkiefersegmenten und 1 cm Nasoethmoidalkomplex-Seitbewegung).
Weitere Diagnostik und Therapie
Sowohl die Weichgewebsmasse als auch die Knochenanteile wurden Formaldehyd-fixiert und in Paraffin eingebettet. Die klassische Histologie ergab keine eindeutige Diagnose. Zur weiteren Diagnostik erfolgte die Extraktion der DNA aus den Proben. Das Next-Generation-Sequencing der DNA ergab einen Mosaik-Gendefekt im PIK3CA-Gen, der die Ursache und das führende diagnostische Kriterium eines Fehlbildungssyndroms (CLOVE-Syndrom) ist. Das CLOVE-Syndrom (Akronym für Congenital Lipomatous Overgrowth, Vascular Malformation, Epidermal Nevi) ist ein sehr seltenes, angeborenes Fehlbildungssyndrom mit den namensgebenden Hauptmerkmalen [Sapp et al., 2007]. Das Syndrom gehört zu den PIK3CA-assoziierten Großwuchssyndromen (PROS), einer Untergruppe der Großwuchssyndrome. Die Häufigkeit wird mit unter 1 zu 1.000.000 angegeben.
Der Erkrankung liegt ein Mosaik postzygotisch aktivierender Mutationen im PIK3CA-Gen auf Chromosom 3 zugrunde, das für die Phosphatidylinositol-3-Kinase kodiert. Für das Enzym wurde ein Medikament (Alpesilib, BYL719) entwickelt, das als Target-Medikament diesen Enzymdefekt deaktiviert. Im Jahr 2018 demonstrierten Grundlagenforscher und Kliniker in einer umfassenden Tier- und Humanstudie am Pariser Kinderkrankenhaus Hôpital Necker–Enfants malades an neunzehn Patienten mit dem CLOVE-Syndrom die Wirksamkeit des Medikaments und veröffentlichten die Ergebnisse in der renommierten Fachzeitschrift „Nature" [Venot et al., 2018]. Bereits in den ersten Tagen der Behandlung zeigten die Patienten – sowohl Neugeborene als auch ältere Patienten – eine dramatische Verbesserung ihres Allgemeinzustands und eine Reduktion von Weichgewebsmassen. Im April 2022 erteilte die US-amerikanische Arzneimittelbehörde FDA aufgrund dieser Untersuchungen die Marktzulassung für Alpelisib [FDA, 2022]. Das Medikament wird in der Regel über circa sechs Monate eingenommen.
Auf Basis der Diagnosestellung bei der Patientin und des Wissens über die Wirksamkeit des spezifischen Medikaments wird nun die weitere Therapie der Patientin verändert werden. Eine medikamentöse Behandlung des Gendefekts wird durchgeführt und kann als zukünftige primäre Therapieoption gewählt werden. Chirurgische Maßnahmen können – in Abhängigkeit vom Erfolg der medikamentösen Therapie – anschließend individuell mit der Patientin besprochen und umgesetzt werden.
Diskussion
Die Erkennung spezifischer Gendefekte und die Behandlung des Patienten mit einem hochspezifischen Antidot wird in der Literatur auch mit dem Begriff der „personalisierten Medizin“ verbunden. Dieser Bereich umfasst im weiteren Sinne die Genommedizin und die Bio- und Informationstechnologie [Reddy et al., 2019]. Dabei wird versucht, mithilfe großer Mengen von Patientendaten (Health-Care- und Genomdaten) und Genomdaten von Erregern ein optimales Therapie-Matching zu determinieren. In einem engeren Sinn bezieht sich der Begriff „personalisierte Medizin“ jedoch auf gezielte Target-Medikamente für einzelne Personen und Erkrankungen – zum Beispiel in der Tumortherapie.
Im Bereich der Zahnmedizin ist jede Behandlung schon immer hoch individuell und damit personalisiert gewesen. Dies betrifft insbesondere alle Maßnahmen der konservativen, der prothetischen und der kieferorthopädischen Zahnheilkunde. Das liegt an der einzigartigen Spezifität der dentalen und okklusalen Phänotypie einer Person, die deswegen heute noch einen zentralen Stellenwert in der Forensik zur Identifizierung hat. Die zahnmedizinischen medikamentösen Therapien sind bisher dagegen kaum individualspezifisch.
Der Einsatz moderner Technologien eröffnet nicht nur neue Möglichkeiten in der patientenspezifischen zahnärztlichen und chirurgischen Behandlung, sondern auch in der gezielten Krankheitserkennung und dadurch möglichen individuellen medikamentösen Behandlung von Patienten. Während die digital basierte patientenindividuelle Behandlung sich sowohl in der Zahnmedizin [Samaranayake, 2012; Joda und Zitzmann, 2022] als auch in der MKG-Chirurgie (virtuelle Operationsplanung, Einsatz von Bohrschablonen, patientenspezifische Implantate [Kerkfeld et al., 2022]) etabliert hat, steckt die individualisierte medikamentöse Therapie erst in ihren Anfängen. Für Zahnärzte, Kieferorthopäden und MKG-Chirurgen ist das Wissen über diese neuen medikamentösen Möglichkeiten sehr hilfreich, da sie in der interdisziplinären Zusammenarbeit häufig beteiligt sind.
Literaturliste
Elemento O: The future of precision medicine: towards a more predictive personalized medicine. Emerg Top Life Sci. 2020 Sep 8;4(2):175-177.
FDA, 2022: www.fda.gov/drugs/resources-information-approved-drugs/fda-approves-alpelisib-pik3ca-related-overgrowth-spectrum.
Ho D, Quake SR, McCabe ERB, Chng WJ, Chow EK, Ding X, Gelb BD, Ginsburg GS, Hassenstab J, Ho CM, Mobley WC, Nolan GP, Rosen ST, Tan P, Yen Y, Zarrinpar A.: Enabling Technologies for Personalized and Precision Medicine. Trends Biotechnol. 2020 May;38(5):497-518.
Jeyang259, 2023: en.wikipedia.org/wiki/File:Personalized_Cancer_Therapy.png, Abruf am 24.07.2023, Veröffentlicht unter CC-Lizenz: creativecommons.org/licenses/by-sa/4.0/deed.de.
Joda T, Zitzmann NU: Personalized workflows in reconstructive dentistry-current possibilities and future opportunities. Clin Oral Investig. 2022 Jun;26(6):4283-4290.
Kerkfeld V et al.: Genomic aspects for the diagnosis of craniofacial disorders. In Meyer U. (Ed.), Fundamentals of Craniofacial Malformations. Springer 2021.
Kerkfeld V, Schorn L, Depprich R, Lommen J, Wilkat M, Kübler N, Rana M, Meyer U.: Simultaneous PSI-Based Orthognathic and PEEK Bone Augmentation Surgery Leads to Improved Symmetric Facial Appearance in Craniofacial Malformations. J Pers Med. 2022 Oct 5;12(10):1653.
Meyer U (Ed.): Fundamentals of Craniofacial Malformations. Springer, 2020.
Morganti S, Tarantino P, Ferraro E, D'Amico P, Duso BA, Curigliano G.: Next Generation Sequencing (NGS): A Revolutionary Technology in Pharmacogenomics and Personalized Medicine in Cancer. Adv Exp Med Biol. 2019;1168:9-30.
Reddy MS, Shetty SR, Vannala V.: Embracing Personalized Medicine in Dentistry J Pharm Bioallied Sci. 2019 May; 11(Suppl 2): S92–S96.
Samaranayake L.: Dentistry in an era of personalized medicine. J Investig Clin Dent. 2012 Aug;3(3):161-2.
J. C. Sapp, J. T. Turner, J. M. van de Kamp, F. S. van Dijk, R. B. Lowry, L. G. Biesecker: Newly delineated syndrome of congenital lipomatous overgrowth, vascular malformations, and epidermal nevi (CLOVE syndrome) in seven patients. In: American journal of medical genetics. Part A. Band 143A, Nummer 24, Dezember 2007, S. 2944–2958.
Superchi C, Brion Bouvier F, Gerardi C, Carmona M, San Miguel L, Sánchez-Gómez LM, Imaz-Iglesia I, Garcia P, Demotes J, Banzi R, Porcher R; PERMIT Group Study designs for clinical trials applied to personalised medicine: a scoping review. BMJ Open. 2022 May 6;12(5):e052926.
Venot Q, Blanc T, Rabia SH, Berteloot L, Ladraa S, Duong JP, Blanc E, Johnson SC, Hoguin C, Boccara O, Sarnacki S, Boddaert N, Pannier S, Martinez F, Magassa S, Yamaguchi J, Knebelmann B, Merville P, Grenier N, Joly D, Cormier-Daire V, Michot C, Bole-Feysot C, Picard A, Soupre V, Lyonnet S, Sadoine J, Slimani L, Chaussain C, Laroche-Raynaud C, Guibaud L, Broissand C, Amiel J, Legendre C, Terzi F, Canaud G.: Targeted therapy in patients with PIK3CA-related overgrowth syndrome. Nature. 2018 Jun;558(7711):540-546.