Die Stabilisierung von Gingivagewebe reduziert die Entzündung
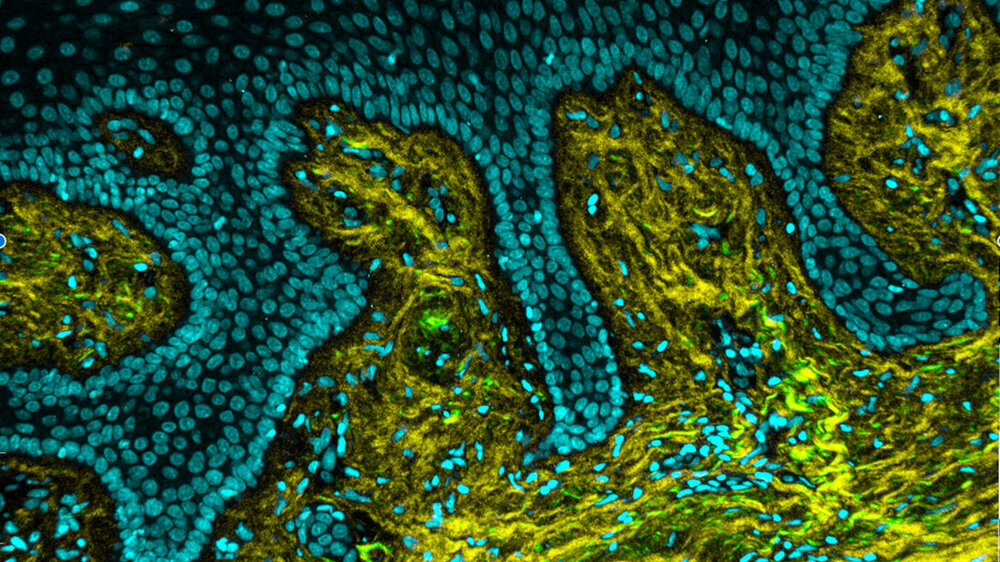
Die inflammatorischen Prozesse einer Parodontitis schädigen unter anderem die extrazelluläre Matrix der Gingiva, die das Stützgewebe des Zahnfleischs bildet. Die Folge ist eine „Erweichung“ des Gewebes. Neue Forschungsergebnisse unter der Leitung von Kyle H. Vining und Hardik Makkar von der zahnmedizinischen Fakultät der Universität Pennsylvania zeigen, wie die physikalischen Eigenschaften des Zahnfleischgewebes die Gesundheit und Erkrankung des Parodonts beeinflussen.
Destruktiver Rückkopplungsmechanismus
Mit der Erweichung des Gewebes, erklärt Makkar, Postdoktorand in Vinings Labor, gerieten die Zellen in einen verstärkten Entzündungszustand, der den Gewebeabbau weiter anregt und einen destruktiven Rückkopplungsmechanismus in Gang setzt, wobei sich Gewebeschädigung und Entzündung gegenseitig verstärken. Der Prozess lässt sich jedoch auch stoppen – allein durch mechanische Intervention: „Wenn wir diese Gewebe experimentell versteifen, geht die Entzündungsreaktion zurück“, sagt Makkar.
Um zu untersuchen, wie die mechanische Umgebung das Zellverhalten beeinflusst, nutzte das Team ein „einstellbares“ Hydrogel aus natürlichen Biopolymeren, das einer Art Wackelpudding ähnelt. „Die Steifigkeit des Hydrogels lässt sich so anpassen, dass sie die Eigenschaften des menschlichen Zahnfleisches nachbildet – von der Festigkeit gesunden Gewebes bis hin zu den weichen Eigenschaften erkrankten Gewebes“, erklärt Makkar. Zunächst kapselten die Forscher Gingivafibroblasten – den vorherrschenden Zelltyp im Bindegewebe des Zahnfleisches, der für die Sekretion und Aufrechterhaltung der extrazellulären Matrix verantwortlich ist – in dieses Hydrogelsystem ein, um zu testen, ob Veränderungen der Gewebesteifigkeit diese Zellen dazu veranlassen, die für Parodontitis charakteristische Entzündungsreaktion zu verschlimmern. Ergebnis: Das „erweichte“ Gewebe triggert den Entzündungszustand.
Stabile Stützgewebe machen Zellen resilienter
In einem zweiten Schritt untersuchten nun die Wissenschaftler, ob sich der Prozess auch mechanisch stoppen lässt. Mithilfe von Enzymen erhöhten sie experimentell die Steifigkeit von menschlichen Gewebeproben aus dem Zahnfleisch. Dabei zeigte sich, dass die versteiften Gewebe eine deutlich geringere Entzündungsreaktion zeigten, wenn sie mikrobiellen Pathogenen ausgesetzt wurden. „Wir konnten zeigen, dass allein die Wiederherstellung der physikalischen Steifigkeit des Gewebes die Reaktion der Zellen auf Infektionen grundlegend verändern kann“, sagt Makkar.
Team will Füllstoff zur Gewebeversteifung entwickeln
Die vorliegende Arbeit trage zu einem besseren Verständnis der Mechanismen bei, die der Entzündungsreaktion bei Parodontitis zugrunde liegen, sagt Vining, Assistenzprofessor im Fachbereich Präventive und Restaurative Wissenschaften der Penn Dental Medicine und im Fachbereich Materialwissenschaft und Werkstofftechnik der Penn Engineering an der Universität Pennsylvania. Die Ergebnisse könnten aber auch den Weg für neue, auf Biomaterialien basierende Therapien ebnen, die die derzeitigen Behandlungen ergänzen, welche ausschließlich auf mikrobielle Ursachen abzielen.
„Wir planen die Entwicklung eines injizierbaren Füllstoffs“, sagt er. „Wenn Sie also an einer unkontrollierten Parodontitis leiden und das Gewebe selbst nach einer professionellen Zahnreinigung noch geschwächt ist, könnten wir den Füllstoff injizieren, um die Heilung zu fördern.“
H. Makkar, N. Tran, Y.-C. Chen, KIKo, RGWells und KHVining, „Matrix Stiffness Governs Fibroblasts’ Regulation of Gingival Immune Homeostasis“, Advanced Materials 38, Nr. 15 (2026): e20717.